铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1)Cu在周期表中位于___________ 区,Cu2+价电子排布式为___________ 。
(2)邻氨基吡啶( )的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为
)的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为___________ ;1mol 中σ键的数目为
中σ键的数目为___________ 。邻氨基吡啶的铜配合物结构简式如下图所示,C原子轨道杂化类型为___________ 。
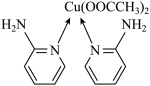
(3)向CuSO4溶液中加入过量氨水再加少许乙醇可以析出蓝色晶体[Cu(NH3)4]SO4∙H2O。
①NH3分子中H-N-H键角为107°,在[Cu(NH3)4]2+中H-N-H键角近似109.5°,键角变大的原因是___________ 。
②NF3与NH3均为三角锥形分子,NF3分子中的氮原子不易与Cu2+形成配离子,请从电负性角度分析其原因是___________ 。
(1)Cu在周期表中位于
(2)邻氨基吡啶(
 )的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为
)的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为 中σ键的数目为
中σ键的数目为
(3)向CuSO4溶液中加入过量氨水再加少许乙醇可以析出蓝色晶体[Cu(NH3)4]SO4∙H2O。
①NH3分子中H-N-H键角为107°,在[Cu(NH3)4]2+中H-N-H键角近似109.5°,键角变大的原因是
②NF3与NH3均为三角锥形分子,NF3分子中的氮原子不易与Cu2+形成配离子,请从电负性角度分析其原因是
更新时间:2023-07-05 15:44:06
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】某些过渡元素的相关化合物在化工、医药、材料等领域有着极为广泛的应用。回答下列问题:
(1)现有铜锌元素的3种微粒:①锌:[Ar]3d104s1;②铜:[Ar]3d104s1;③铜:[Ar]3d10,失去一个电子需要的最低能量由大到小的顺序是___________(填字母)。
(2)砷化镉(Cd3As2)是一种验证三维量子霍尔效应的材料。
①砷与卤素可形成多种卤化物,从电子云重叠方式判断AsCl3中的化学键属于___________ 键;砷酸的酸性弱于硒酸,从分子结构的角度解释原因___________ 。
②Cd2+与NH3形成配离子[Cd(NH3)4]2+中,配体的空间构型为___________ ,画出配离子的结构式___________ (不考虑立体构型)。
(3)铬(Cr)、钼(Mo)、钨(W)位于同一副族相邻周期,且原子序数依次增大。
①基态铬原子、钼原子的核外电子排布特点相同,则基态钼原子的价层电子排布图为___________ 。
②已知 CrO5中铬元素为最高价态,氧元素有 价和
价和 价,画出其结构式:
价,画出其结构式:___________ 。
③钨和碳能形成耐高温、耐磨材料碳化钨,其晶胞结构如下图所示,则碳化钨的化学式为___________ ,六棱柱的底边长为a cm,高为b cm,设阿伏加德罗常数的值为NA,则碳化钨晶体的密度是___________ g·cm-3(列出计算表达式)。

(1)现有铜锌元素的3种微粒:①锌:[Ar]3d104s1;②铜:[Ar]3d104s1;③铜:[Ar]3d10,失去一个电子需要的最低能量由大到小的顺序是___________(填字母)。
| A.①②③ | B.③①② | C.③②① | D.①③② |
(2)砷化镉(Cd3As2)是一种验证三维量子霍尔效应的材料。
①砷与卤素可形成多种卤化物,从电子云重叠方式判断AsCl3中的化学键属于
②Cd2+与NH3形成配离子[Cd(NH3)4]2+中,配体的空间构型为
(3)铬(Cr)、钼(Mo)、钨(W)位于同一副族相邻周期,且原子序数依次增大。
①基态铬原子、钼原子的核外电子排布特点相同,则基态钼原子的价层电子排布图为
②已知 CrO5中铬元素为最高价态,氧元素有
 价和
价和 价,画出其结构式:
价,画出其结构式:③钨和碳能形成耐高温、耐磨材料碳化钨,其晶胞结构如下图所示,则碳化钨的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氯吡苯脲是一种经国家批准使用的植物生长调节剂,其结构简式如图所示。

(1)下列方法中,可用于测量氯吡苯脲相对分子质量的是____。
(2)基态O原子价层电子轨道表示式不能表示为 ,因为这违背了
,因为这违背了_____ 。
A.构造原理 B.泡利不相容原理 C.洪特规则
(3)氯吡苯脲的组成元素中,属于第二周期的元素,其第一电离能由大到小的顺序为_____ 。(用元素符号表示)
(4)氯元素基态原子的电子排布式为_____ 。其原子核外电子占据的最高能级的电子云轮廓图为_____ 形。
(5)氮原子最外层电子中两种自旋状态的电子数之比为:_____ 。氮元素在元素周期表中属于_____ 区元素。
(6)和碳原子相比,氮原子的电负性更_____ (填“大”或“小”),从原子结构角度解释其原因:_____ 。
(7)查文献可知,可用异氰酸苯酯与2-氯-4-氨基吡啶反应,生成氯吡苯脲,其反应方程式为:

①该反应的反应类型为_____ 。
②反应过程中,每生成1个氯吡苯脲,断裂_____ 个 键,断裂
键,断裂_____ 个 键。
键。

(1)下列方法中,可用于测量氯吡苯脲相对分子质量的是____。
| A.质谱 | B.红外光谱 | C.核磁共振氢谱 | D.原子发射光谱 |
 ,因为这违背了
,因为这违背了A.构造原理 B.泡利不相容原理 C.洪特规则
(3)氯吡苯脲的组成元素中,属于第二周期的元素,其第一电离能由大到小的顺序为
(4)氯元素基态原子的电子排布式为
(5)氮原子最外层电子中两种自旋状态的电子数之比为:
(6)和碳原子相比,氮原子的电负性更
(7)查文献可知,可用异氰酸苯酯与2-氯-4-氨基吡啶反应,生成氯吡苯脲,其反应方程式为:

①该反应的反应类型为
②反应过程中,每生成1个氯吡苯脲,断裂
 键,断裂
键,断裂 键。
键。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】半导体芯片的关键材料是我国优先发展的新材料。经过半个多世纪的发展,硅基材料的半导体器件性能已经接近其物理极限,以碳化硅、氮化镓等为代表的第二代半导体材料成为当今热点。回答如下问题:
(1)材料所涉及的四种元素中,原子半径最大的是_______ (填元素符号,下同),这四种元素中第一电离能最大的是_______ ,基态Si原子的电子占据的轨道数目是_______ 个。
(2)原硅酸根SiO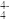 的空间构型是
的空间构型是_______ ,其中Si的价层电子对数目为_______ 、杂化轨道类型为_______ 。
(3)材料所涉及的四种元素对应的单质中,熔沸点最低的是_______ ,原因是_______ 。
(4)GaN被誉为21世纪引领5G时代的基石材料,是目前全球半导体研究的前沿和热点。有一种氮化镓的六方晶胞结构如图所示,请在图中构建一个以Ga原子为中心的四面体结构(涂成◎)。

(5)材料密度是制作芯片的重要参数之一,已知Si的共价半径是125pm。求每立方厘米体积的单晶硅中硅的原子数目为_______ (保留2位有效数字)。
(1)材料所涉及的四种元素中,原子半径最大的是
(2)原硅酸根SiO
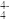 的空间构型是
的空间构型是(3)材料所涉及的四种元素对应的单质中,熔沸点最低的是
(4)GaN被誉为21世纪引领5G时代的基石材料,是目前全球半导体研究的前沿和热点。有一种氮化镓的六方晶胞结构如图所示,请在图中构建一个以Ga原子为中心的四面体结构(涂成◎)。

(5)材料密度是制作芯片的重要参数之一,已知Si的共价半径是125pm。求每立方厘米体积的单晶硅中硅的原子数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】离子液体被认为是21世纪理想的绿色溶剂,是指室温或者接近室温时呈液态,而本身由阴、阳离子构成的化合物。氯代1-丁基-3-甲基咪唑离子液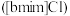 可以与
可以与 混合形成离子液体;
混合形成离子液体;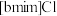 也可以转化成其他离子液体,下图是
也可以转化成其他离子液体,下图是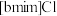 与
与 离子交换反应合成离子液体
离子交换反应合成离子液体 的流程:
的流程:

(1)请画出基态Ga原子的价电子排布图_____ ;同周期元素中基态原子未成对电子数与硼(B)原子相同的有_____ (填元素符号)。
(2)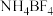 中N原子的杂化方式为
中N原子的杂化方式为_____ ,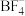 的空间构型为
的空间构型为_____ , 中几种元素电负性由大到小的顺序为
中几种元素电负性由大到小的顺序为_____ 。
(3)已知分子中的大 键可以用
键可以用 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则
键中的电子数,则 中大
中大 键可以表示为
键可以表示为_____ 。
(4) 熔点为
熔点为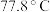 ,则
,则 的晶体类型为
的晶体类型为_____ , 和
和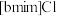 混合形成离子液体的过程中会存在以下转化:
混合形成离子液体的过程中会存在以下转化: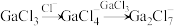 ,请画出
,请画出 的结构式
的结构式_____ 。
(5)某种 的晶胞结构如图所示,O2−以六方最密方式堆积,
的晶胞结构如图所示,O2−以六方最密方式堆积, 在其八面体空隙中(注:未全部标出,如:
在其八面体空隙中(注:未全部标出,如: 在1、2、3、4、5、6构成的八面体体心)。
在1、2、3、4、5、6构成的八面体体心)。
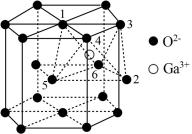
①该晶胞中O2−的配位数为_____ 。
②已知氧离子半径为acm,晶胞的高为bcm,NA代表阿伏加德罗常数的值,该晶体的密度为_____ g·cm−3(用含 和NA的代数式表示)。
和NA的代数式表示)。
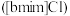 可以与
可以与 混合形成离子液体;
混合形成离子液体;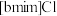 也可以转化成其他离子液体,下图是
也可以转化成其他离子液体,下图是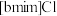 与
与 离子交换反应合成离子液体
离子交换反应合成离子液体 的流程:
的流程:
(1)请画出基态Ga原子的价电子排布图
(2)
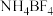 中N原子的杂化方式为
中N原子的杂化方式为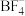 的空间构型为
的空间构型为 中几种元素电负性由大到小的顺序为
中几种元素电负性由大到小的顺序为(3)已知分子中的大
 键可以用
键可以用 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则
键中的电子数,则 中大
中大 键可以表示为
键可以表示为(4)
 熔点为
熔点为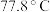 ,则
,则 的晶体类型为
的晶体类型为 和
和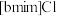 混合形成离子液体的过程中会存在以下转化:
混合形成离子液体的过程中会存在以下转化: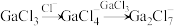 ,请画出
,请画出 的结构式
的结构式(5)某种
 的晶胞结构如图所示,O2−以六方最密方式堆积,
的晶胞结构如图所示,O2−以六方最密方式堆积, 在其八面体空隙中(注:未全部标出,如:
在其八面体空隙中(注:未全部标出,如: 在1、2、3、4、5、6构成的八面体体心)。
在1、2、3、4、5、6构成的八面体体心)。
①该晶胞中O2−的配位数为
②已知氧离子半径为acm,晶胞的高为bcm,NA代表阿伏加德罗常数的值,该晶体的密度为
 和NA的代数式表示)。
和NA的代数式表示)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】完成下列问题。
Ⅰ.电负性的概念是由美国化学家鲍林提出的,用来描述不同元素的原子对键合电子吸引力的大小,可用一定数值x来表示。下面是某些短周期元素的x值:
(1)通过分析x值变化规律,确定Mg的x值范围:___________<x(Mg)<___________。___________
(2)指出下列两种化合物中氧元素的化合价:HClO___________ ,HFO___________ 。有机物结构式为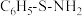 ,其中S-N中,共用电子对偏向
,其中S-N中,共用电子对偏向___________ 。
(3)成键的两原子相应元素x数值的差值为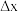 ,当
,当 时,一般为离子键,
时,一般为离子键, 时,一般为共价键,则
时,一般为共价键,则 中化学键类型是
中化学键类型是___________ 。
(4)预测元素周期表中,x值最小的元素位于___________ 周期___________ 族(放射性元素除外)。
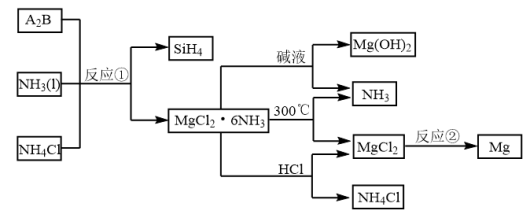
Ⅱ.下图中反应①是制备 的一种方法,其副产物是优质的镁资源。
的一种方法,其副产物是优质的镁资源。
(5)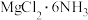 中所含元素的简单离子半径由小到大的顺序(氢元素的简单离子只考虑H+):
中所含元素的简单离子半径由小到大的顺序(氢元素的简单离子只考虑H+):___________ 。
(6)A2B的化学式为___________ 。上图中可以循环使用的物质有___________ (化学式)。
(7)一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料___________ 。
(8)为实现燃煤脱硫,煤中加入浆状 ,使燃烧产生的
,使燃烧产生的 转化为稳定的镁化合物。该反应的化学方程式:
转化为稳定的镁化合物。该反应的化学方程式:___________ 。
Ⅰ.电负性的概念是由美国化学家鲍林提出的,用来描述不同元素的原子对键合电子吸引力的大小,可用一定数值x来表示。下面是某些短周期元素的x值:
| 元素 | Li | Be | B | C | N | O | F | Na | Al | Si | P | S | Cl |
| x值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.0 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(2)指出下列两种化合物中氧元素的化合价:HClO
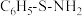 ,其中S-N中,共用电子对偏向
,其中S-N中,共用电子对偏向(3)成键的两原子相应元素x数值的差值为
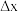 ,当
,当 时,一般为离子键,
时,一般为离子键, 时,一般为共价键,则
时,一般为共价键,则 中化学键类型是
中化学键类型是(4)预测元素周期表中,x值最小的元素位于
Ⅱ.下图中反应①是制备
 的一种方法,其副产物是优质的镁资源。
的一种方法,其副产物是优质的镁资源。
(5)
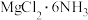 中所含元素的简单离子半径由小到大的顺序(氢元素的简单离子只考虑H+):
中所含元素的简单离子半径由小到大的顺序(氢元素的简单离子只考虑H+):(6)A2B的化学式为
(7)一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料
(8)为实现燃煤脱硫,煤中加入浆状
 ,使燃烧产生的
,使燃烧产生的 转化为稳定的镁化合物。该反应的化学方程式:
转化为稳定的镁化合物。该反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】铁、钴、镍位于元素周期表第四周期Ⅷ族,具有相似的性质,它们的单质及化合物在现代工业生产中有着广泛应用。请回答下列问题:
(1)基态镍原子的核外电子占据的最高能层的符号是_________ ,占据该能层电子的电子云轮廓图形状为_________ 。
(2)硫化钴可用作有机化合物的氢化催化剂。钴的基态原子中未成对电子个数为________ ;电负性:硫元素_________ (填“大于”或“小于”)钴元素;基态硫原子的核外电子排布式为_________ 。
(3)铁元素能与CO形成Fe(CO)5等金属羰基配合物。与CO互为等电子体的分子和离子分别为_________ 和_________ (各举一种,填化学式);在CO分子中,σ键与π键数目之比为_________ 。
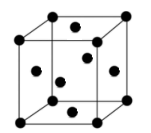
(4)下图是金属镍的晶胞结构示意图,其晶胞参数为a nm,则金属镍原子的配位数为_________ ;镍原子半径为_________ nm;晶体密度为_________ g·cm-3(阿伏加 德罗常数的值用NA表示,写出简化后的计算式即可)。
(1)基态镍原子的核外电子占据的最高能层的符号是
(2)硫化钴可用作有机化合物的氢化催化剂。钴的基态原子中未成对电子个数为
(3)铁元素能与CO形成Fe(CO)5等金属羰基配合物。与CO互为等电子体的分子和离子分别为
(4)下图是金属镍的晶胞结构示意图,其晶胞参数为a nm,则金属镍原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】共价晶体是由原子直接通过共价键形成的空间网状结构的晶体,因其具有高熔、沸点,硬度大,耐磨等优良特性而具有广泛的用途。
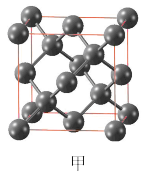
(1)晶体硅是良好的半导体材料,被广泛用于信息技术和能源科学等领域。晶体硅是与金刚石结构类似的晶体(其晶胞如图甲所示),硅晶体的1个晶胞中含_______ 个Si原子,在晶体硅的空间网状结构中最小环为_______ 元环,每个最小环独立含有_______ 个Si原子,含 原子的晶体硅中Si-Si键的数目为
原子的晶体硅中Si-Si键的数目为_______ (设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
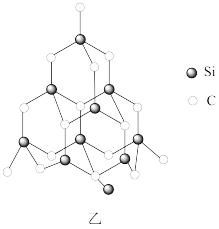
(2)金刚砂(SiC)也与金刚石具有相似的晶体结构(如图乙所示),在金刚砂的空间网状结构中,碳原子、硅原子交替以共价单键相结合。
①金刚砂、金刚石、晶体硅的熔点由低到高的顺序是_______ (均用化学式表示)。
②在金刚砂的结构中,一个硅原子结合了_______ 个碳原子,其中的键角是_______ 。
③金刚砂的结构中含有C、Si原子以共价键结合形成的环,其中一个最小的环上独立含有__ 个C-Si键。
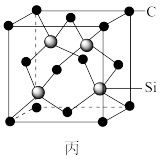
④金刚砂的晶胞结构如图丙所示,在SiC中,每个C原子周围最近且等距的C原子数目为_______ 。
(1)晶体硅是良好的半导体材料,被广泛用于信息技术和能源科学等领域。晶体硅是与金刚石结构类似的晶体(其晶胞如图甲所示),硅晶体的1个晶胞中含
 原子的晶体硅中Si-Si键的数目为
原子的晶体硅中Si-Si键的数目为 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
(2)金刚砂(SiC)也与金刚石具有相似的晶体结构(如图乙所示),在金刚砂的空间网状结构中,碳原子、硅原子交替以共价单键相结合。

①金刚砂、金刚石、晶体硅的熔点由低到高的顺序是
②在金刚砂的结构中,一个硅原子结合了
③金刚砂的结构中含有C、Si原子以共价键结合形成的环,其中一个最小的环上独立含有
④金刚砂的晶胞结构如图丙所示,在SiC中,每个C原子周围最近且等距的C原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】[Cu(NH3)4]SO4·H2O 晶体制备:
(1)制备过程:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到___________ 色的透明溶液;再加入适量乙醇,将析出[Cu(NH3)4]SO4·H2O 晶体。请解释加入乙醇后析出晶体的原因___________ 。
(2)写出沉淀溶解得透明溶液的离子方程式___________ 。
(3)以配位键形式表示[Cu(NH3)4]2+的结构___________ ,1 mol[Cu(NH3)4]2+含有___________ 个σ键。
(4)[Cu (NH3)4]SO4 中,存在的化学键类型有___________ (填选项)。
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
(5)从结构的角度分析 NH3比 NF3的键角大的原因:___________ 。
(1)制备过程:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到
(2)写出沉淀溶解得透明溶液的离子方程式
(3)以配位键形式表示[Cu(NH3)4]2+的结构
(4)[Cu (NH3)4]SO4 中,存在的化学键类型有
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
(5)从结构的角度分析 NH3比 NF3的键角大的原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】Cu—Mn—Al合金为磁性形状记忆合金材料之一,可用来制作各种新型的换能器、驱动器、敏感元件和微电子机械操纵系统。
(1)下列状态的铝中,最外层电离出一个电子所需能量最小的是______ (填标号)。
A. B.
B. 
C. D.
D. 
(2)AlCl3是某些有机反应的催化剂,如苯与乙酰氯反应的部分历程为:

①乙酰氯分子中碳原子的杂化类型为____ 。
②乙酰氯分子中∠CCCl___ 120°(填“>”、“=”或“<”),判断理由是_______ 。
③ 的空间构型为
的空间构型为________ 。
(3)温度不高时气态氯化铝为二聚分子(其结构如图所示)。

写出Al2Cl6的结构式并标出配位键______ 。
(4)Cu—Mn—合金的晶胞如图a所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,图b是沿立方格子对角面取得的截图。
①若A原子的坐标参数为(0,0,0),C为(1,1,1),则B原子的坐标参数为_____ 。
②由晶胞可知该合金的化学式为_____ 。
③已知r(Cu)≈r(Mn)=127pm,r(Al)=143pm,则Cu原子之间的最短核间距离为____ pm。
④该晶胞的密度为_____ g·cm-3。(列出计算式即可,阿伏加 德罗常数用NA表示)

(1)下列状态的铝中,最外层电离出一个电子所需能量最小的是
A.
 B.
B. 
C.
 D.
D. 
(2)AlCl3是某些有机反应的催化剂,如苯与乙酰氯反应的部分历程为:

①乙酰氯分子中碳原子的杂化类型为
②乙酰氯分子中∠CCCl
③
 的空间构型为
的空间构型为(3)温度不高时气态氯化铝为二聚分子(其结构如图所示)。

写出Al2Cl6的结构式并标出配位键
(4)Cu—Mn—合金的晶胞如图a所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,图b是沿立方格子对角面取得的截图。
①若A原子的坐标参数为(0,0,0),C为(1,1,1),则B原子的坐标参数为
②由晶胞可知该合金的化学式为
③已知r(Cu)≈r(Mn)=127pm,r(Al)=143pm,则Cu原子之间的最短核间距离为
④该晶胞的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】2019年6月6日,工信部正式向四大运营商颁发了5G商用牌照,揭示了我国5G元年的起点。通信用锂离子电池般需要体积小、重量轻、高温性能突出、可高倍率充放电、绿色环保等众多优点。请回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Fe原子的价电子排布式为___ 基态Co原子核外电子的空间运动状态有_______ 种。
(2)PO43-的空间构型是______ ,写出与其互为等电子体的一种阴离子______ ,基态P原子的第一电离能为什么比基态S原子的第一电离能大:______ 。
(3)现有化学式为Co(NH3)5Cl3的配合物,1mol 该物质最多可以与2molAgNO3反应,则该配合物中钴的配位数为______ , 配体中N的杂化方式为_____ ,1mol 该配合物中含δ键数目为______ NA。
(4)FeO是离子晶体,其晶格能可通过下图的Bom-Haber循环计算得到。气态电中性基态原子获得一个电子变为气态一价负离子放出的能量叫做第一电子亲和能,由图可知O原子的第一电子亲和能为_____ kJ·mol-1, FeO晶格能为_____ kJ·mol-1。

(5)单质锂晶体的结构如下图,晶胞中锂的配位数为____ ,晶胞的空间利用率为____ (用含有n的表达式即可),若晶胞边长为a pm, NA为阿伏加 德罗常数,则金属锂的密度为_____ g cm-3。(写出计算式)

(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Fe原子的价电子排布式为
(2)PO43-的空间构型是
(3)现有化学式为Co(NH3)5Cl3的配合物,1mol 该物质最多可以与2molAgNO3反应,则该配合物中钴的配位数为
(4)FeO是离子晶体,其晶格能可通过下图的Bom-Haber循环计算得到。气态电中性基态原子获得一个电子变为气态一价负离子放出的能量叫做第一电子亲和能,由图可知O原子的第一电子亲和能为

(5)单质锂晶体的结构如下图,晶胞中锂的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁是人体必需的微量元素,在人类生产和生活中也有重要作用。
(1)①有机物甲所含的元素中,电负性最小的是___________ (填元素符号,下同),第一电离能最大的是___________ 。

②血红蛋白中的铁处于基态时,其最高能级中的单电子数为___________ 。
③血红蛋白中N原子的杂化方式为___________ 。
(2)FeCl3中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的FeCl3的结构式为___________ ,其中Fe的配位数为___________ 。
(3)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示。

这类磷酸根离子的化学式可用通式表示为___________ (用n代表P原子数)。
(4)铁及其化合物的晶体种类较多。
①Fe的一种晶体结构如甲、乙所示,若按甲中虚线方向切乙,得到的切面图正确的是___________ (填序号)。

A. B.
B. C.
C. D.
D.
②Fe和N可组成一种过渡金属氮化物,其晶胞如图所示。六棱柱底边边长为x cm,高为y cm,NA为阿伏加德罗常数的值,则晶胞密度为___________ g·cm-3 (列出计算式即可)。

(1)①有机物甲所含的元素中,电负性最小的是

②血红蛋白中的铁处于基态时,其最高能级中的单电子数为
③血红蛋白中N原子的杂化方式为
(2)FeCl3中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的FeCl3的结构式为
(3)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示。

这类磷酸根离子的化学式可用通式表示为
(4)铁及其化合物的晶体种类较多。
①Fe的一种晶体结构如甲、乙所示,若按甲中虚线方向切乙,得到的切面图正确的是

A.
 B.
B. C.
C. D.
D.
②Fe和N可组成一种过渡金属氮化物,其晶胞如图所示。六棱柱底边边长为x cm,高为y cm,NA为阿伏加德罗常数的值,则晶胞密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】纯碱和硅酸钠都属于碳族元素的含氧酸盐,性质既相似又不同。回答下列问题:
(1)纯碱中碳原子的杂化方式为_______ 。基态碳原子中未成对电子有_______ 个。
(2)某硅氧离子的空间结构示意图如图所示(虚线不表示共价键)。Si-O键的键角为_______ , 该硅氧离子的化学式为_______ 。该硅氧离子的钠盐溶液中存在的微粒间作用力类型有_______ (选填序号)。
A.范德华力 B.氢键 C.离子键 D.共价键

(3)硅烷数量、种类比烷烃_______ (填“多”或“少”);酸性: H2CO3_______ H2SiO3(填“>”、“<”或“=”),试解释酸性强弱的原因_______ 。
(4)单质硅的晶胞结构如图所示,已知单质硅的密度为ρg·cm-3,若NA是阿伏加德罗常数的值,则Si- Si 键的键长为_______ nm。(用含 N、ρ的代数式表示,列式即可,不用计算)

(1)纯碱中碳原子的杂化方式为
(2)某硅氧离子的空间结构示意图如图所示(虚线不表示共价键)。Si-O键的键角为
A.范德华力 B.氢键 C.离子键 D.共价键

(3)硅烷数量、种类比烷烃
(4)单质硅的晶胞结构如图所示,已知单质硅的密度为ρg·cm-3,若NA是阿伏加德罗常数的值,则Si- Si 键的键长为

您最近一年使用:0次



