下列“实验现象”和“结论”的因果关系有错误的是。
| 选项 | 操作 | 现象 | 结论 |
| A | 相同温度下,测定等浓度的 和 和 溶液的pH 溶液的pH | 前者pH比后者大 | 非金属性:S>C |
| B | 火柴梗上滴少量的浓硫酸 | 火柴梗变黑 | 浓硫酸具有强氧化性 |
| C | 将20℃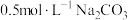 溶液加热到60℃,用pH传感器测定pH 溶液加热到60℃,用pH传感器测定pH | 溶液的pH逐渐减小 |  改变与水解平衡移动共同作用的结果 改变与水解平衡移动共同作用的结果 |
| D | 取一支试管装入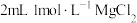 溶液,先滴加 溶液,先滴加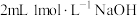 溶液,再滴加几滴 溶液,再滴加几滴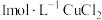 溶液 溶液 | 先生成白色沉淀,后沉淀变为蓝色 | 溶度积: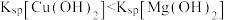 |
| A.A | B.B | C.C | D.D |
更新时间:2023-08-09 09:26:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】由下列实验现象得出的结论正确的是
| 操作及现象 | 结论 | |
| A | 向盛有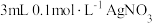 溶液的试管中加入 溶液的试管中加入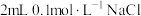 溶液产生白色沉淀,再加入几滴 溶液产生白色沉淀,再加入几滴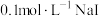 溶液,有黄色沉淀生成 溶液,有黄色沉淀生成 | 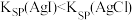 |
| B | 通过电解发生反应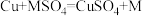 | 金属性: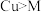 |
| C |  溶液中滴加 溶液中滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 | 白色沉淀成分是 |
| D | 测定等物质的量浓度的 和 和 溶液的 溶液的 值,前者大 值,前者大 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验目的对应的实验方案、现象和结论都正确的是
| 选项 | 实验目的 | 实验方案 | 现象和结论 |
| A | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 有气体生成,固体粉末为Na2O2 |
| B | 比较AgCl和AgI的Ksp相对大小 | 向等体积饱和AgCl溶液和饱和AgI溶液中分别滴加等量的浓AgNO3溶液(过量) | 得到沉淀n(AgCl)>n(AgI),则Ksp(AgCl)>Ksp(AgI) |
| C | 比较Cl2、Br2、I2的氧化性强弱 | 向KBr、KI混合溶液中依次加入少量新制氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色,证明氧化性:Cl2>Br2>I2 |
| D | 比较H2CO3与CH3COOH的酸性强弱 | 用pH计测定溶液pH:①NaHCO3溶液②CH3COONa溶液 | pH:①>②,证明H2CO3的酸性弱于CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 溶液中加入HCl无现象,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中有SO |
| B | Agl沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比Agl更难溶 |
| C | 向CH3CH2X中加入少量AgNO3溶液,加热 | 有浅黄色沉淀生成 | CH3CH2X中含有Br- |
| D | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热, | 没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化学与工农业生产、生活密切相关,下列叙述不正确的是
| A.氢气燃烧放热多且产物无污染,是理想的绿色能源 |
| B.为除去锅炉中的水垢,可用适量稀硫酸处理,快速且不挥发酸性气体 |
| C.冰在室温下自动熔化成水,是熵、焓都增大的过程 |
| D.以草木灰肥田,既可以为农作物提供营养元素,还可以有效降低土壤的酸度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】元素周期表VIA族元素又称为氧族元素,包含氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po)、鉝(Lv)六种元素,其中钋、鉝为金属,碲为准金属,氧、硫、硒是典型的非金属元素。下列有关硒元素的推测不正确的是
| A.最高化合价为+6 | B.原子半径比硫的大 |
| C.硒化氢的热稳定性比硫化氢强 | D.最高价氧化物的水化物的酸性比硫的弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍,Q与Z位于不同的主族。下列说法正确的是
| A.非金属性:Q<Y | B.简单离子半径:Q<X |
| C.原子序数为82的元素与Y位于同一主族 | D.最高价含氧酸的酸性:Z<Q |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于过氧化钠和水反应的实验现象说法不正确的是
| A.产生了使带火星木条复燃的气体 |
| B.向反应后的溶液中滴入酚酞,溶液立即变红且红色不消失 |
| C.向包裹过氧化钠固体的棉花上滴水,棉花燃烧,说明反应放热 |
| D.向反应后的溶液中加入几粒二氧化锰,有气泡放出 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | A、B两支试管中分别加入10mL5%的H2O2溶液,在A试管中加入1mLFeCl3溶液,在B试管中加入1mL蒸馏水 | A试管中产生气泡更快 | FeCl3是H2O2分解的催化剂 |
| B | 室温下,向10mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀,再滴加2滴0.1mol/LFeCl3溶液 | 有红褐色沉淀生成 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| C | 将5mL0.1mol/LFeCl3溶液与2mL0.1mol/LKI溶液混合于试管中充分反应后,滴加几滴KSCN溶液,振荡 | 溶液变为 血红色 | Fe3+与I-的反应有一定的限度 |
| D | 向NaCl、NaI的混合溶液中滴入少量稀AgNO3溶液 | 有黄色沉淀 生成 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 与H+离子数之和大于NA
与H+离子数之和大于NA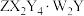 是一种白色晶体,不溶于水,用于陶瓷上釉等.W、X、Y、Z原子序数依次增加且和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,
是一种白色晶体,不溶于水,用于陶瓷上釉等.W、X、Y、Z原子序数依次增加且和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,
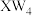 的键角大于
的键角大于