近期我国学者研制出低成本的电解“水制氢”催化剂——镍掺杂的磷化钴三元纳米片电催化剂(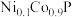 )。回答下列问题:
)。回答下列问题:
(1)P在元素周期表中的位置为___________ ,Ni原子价层电子排布式为___________ 。
(2)Co形成的一种配合物结构如下: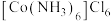
①配合物中提供孤对电子的原子是___________ ;配位数是___________ 。
②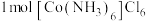 中含有
中含有 键的数目为
键的数目为___________ 。
③N、P属于同主族元素, 的沸点高于
的沸点高于 的沸点的原因是
的沸点的原因是___________ 。
④ 和
和 中氮原子的杂化方式是
中氮原子的杂化方式是___________ , 中键角
中键角___________ (填写“大于”、“小于”或“等于”) 中键角。
中键角。
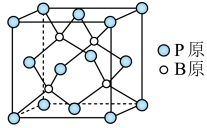
(3)磷化硼是一种备受关注的耐磨涂料,其晶体中磷原子作面心立方最密堆积,硼原子填入四面体空隙中(如图)。已知磷化硼的晶胞边长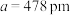 ,已知磷化硼晶体密度为
,已知磷化硼晶体密度为 ,
,
___________ (不必化简),P原子的配位数是___________ 。
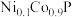 )。回答下列问题:
)。回答下列问题:(1)P在元素周期表中的位置为
(2)Co形成的一种配合物结构如下:
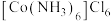
①配合物中提供孤对电子的原子是
②
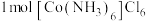 中含有
中含有 键的数目为
键的数目为③N、P属于同主族元素,
 的沸点高于
的沸点高于 的沸点的原因是
的沸点的原因是④
 和
和 中氮原子的杂化方式是
中氮原子的杂化方式是 中键角
中键角 中键角。
中键角。(3)磷化硼是一种备受关注的耐磨涂料,其晶体中磷原子作面心立方最密堆积,硼原子填入四面体空隙中(如图)。已知磷化硼的晶胞边长
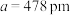 ,已知磷化硼晶体密度为
,已知磷化硼晶体密度为 ,
,

更新时间:2023-08-14 14:31:24
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期。已知B元素L层电子数为K层上的2倍,D的原子核外存8种运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子。请回答下列问题:
(1)写出D原子基态的价层电子排布图:________ 。
(2)下列说法错误的是____________ (填序号)。
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点: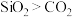
B.电负性:
C. 与
与 互为等电子体,结构相似,化学性质相似
互为等电子体,结构相似,化学性质相似
D.稳定性: ,是因为水分子间存在氢键的缘故
,是因为水分子间存在氢键的缘故
(3)F离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点。向元素F的硫酸盐溶液中通入过量的气体X(X由C、A两种元素形成的含有10个电子的微粒)可生成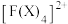 ,该离子的结构式为
,该离子的结构式为____________ (用相关元素符号表示)。
(4)某化合物与F(Ⅰ)(Ⅰ表示元素F的化合价为+1价)结合形成如图所示的离子,该离子中碳原子的杂化方式是_______ 。
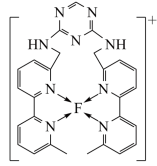
(5)已知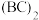 是直线型分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则
是直线型分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则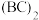 中σ键和π键的个数比为
中σ键和π键的个数比为____ 。
(6)C元素最高价含氧酸与硫酸酸性强度相近,原因是_______ 。
(7)B单质的一种同素异形体的晶胞如图所示:
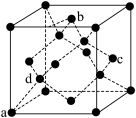
则一个晶胞中所含B原子个数为_____ ;其中原子坐标参数为: ,
,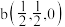 ,
, ,则c点原子的坐标参数为
,则c点原子的坐标参数为______ 。(坐标系如图)
(8)D与F形成离子个数比为1:1的化合物晶胞与 类似,D离子的配位数是
类似,D离子的配位数是________ ;设该晶胞的棱长为a pm,则该晶体的密度为________  (用相关字母表示,已知阿伏加 德罗常数为NA)
(用相关字母表示,已知阿伏加 德罗常数为NA)
(1)写出D原子基态的价层电子排布图:
(2)下列说法错误的是
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点:
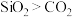
B.电负性:

C.
 与
与 互为等电子体,结构相似,化学性质相似
互为等电子体,结构相似,化学性质相似D.稳定性:
 ,是因为水分子间存在氢键的缘故
,是因为水分子间存在氢键的缘故(3)F离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点。向元素F的硫酸盐溶液中通入过量的气体X(X由C、A两种元素形成的含有10个电子的微粒)可生成
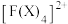 ,该离子的结构式为
,该离子的结构式为(4)某化合物与F(Ⅰ)(Ⅰ表示元素F的化合价为+1价)结合形成如图所示的离子,该离子中碳原子的杂化方式是

(5)已知
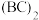 是直线型分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则
是直线型分子,并有对称性,且分子中每个原子最外层都达到8电子稳定结构,则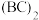 中σ键和π键的个数比为
中σ键和π键的个数比为(6)C元素最高价含氧酸与硫酸酸性强度相近,原因是
(7)B单质的一种同素异形体的晶胞如图所示:

则一个晶胞中所含B原子个数为
 ,
,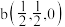 ,
, ,则c点原子的坐标参数为
,则c点原子的坐标参数为
(8)D与F形成离子个数比为1:1的化合物晶胞与
 类似,D离子的配位数是
类似,D离子的配位数是 (用相关字母表示,已知阿伏加 德罗常数为NA)
(用相关字母表示,已知阿伏加 德罗常数为NA)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】(1)氯化铁溶液用于检验食用香精乙酰乙酯时,会生成紫色配合物,其配离子结构如图所示。
①此配合物中,基态铁离子的价电子排布式为________________ 。
②此配合物中碳原子的杂化轨道类型有________________ 。
③此配离子中含有的化学键有____________ (填字母)。
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键 G.σ键 H.π键
④氯化铁在常温下是固体,熔点为 306℃,沸点为 315℃,在 300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断氯化铁的晶体类型为________________ 。
(2)基态A 子的价电子排布式为3s23p5,铜与A 形成化合物的晶胞如图所示(黑球代表铜原子)。
①该化合物的化学式为________________ ,A原子的配位数是______________ 。
②该化合物难溶于水,但易溶于氨水,其原因可能是_______ ;与NH3 互为等电子体的分子有_______ (写化学式,一种即可)。 NH3 的键角大于H2O的键角的主要原因是_________________ 。
③已知该化合物晶体的密度为ρg·cm-3,阿伏伽德罗常数的值为 NA,则该晶体中 Cu 原子和A 原子之间的最短距离为________________ pm(列出计算表达式即可)。

①此配合物中,基态铁离子的价电子排布式为
②此配合物中碳原子的杂化轨道类型有
③此配离子中含有的化学键有
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键 G.σ键 H.π键
④氯化铁在常温下是固体,熔点为 306℃,沸点为 315℃,在 300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断氯化铁的晶体类型为
(2)基态A 子的价电子排布式为3s23p5,铜与A 形成化合物的晶胞如图所示(黑球代表铜原子)。

①该化合物的化学式为
②该化合物难溶于水,但易溶于氨水,其原因可能是
③已知该化合物晶体的密度为ρg·cm-3,阿伏伽德罗常数的值为 NA,则该晶体中 Cu 原子和A 原子之间的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】生物质能是一种洁净、可再生的能源。.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
⑴上述反应的催化剂含有Cu、Zn、AI等元素。写出基态Cu原子的核外电子排布式:___________ 。
⑵根据等电子原理.写出CO分子的电子式:______________ 。
(3)甲醇催化氧化可得到甲醛,甲醇的沸点比甲醛的高,其主要原因是___________________ 。
(4)胆矾结构示意图可简单表示如下,回答下列问题。
①胆矾晶体中存在的作用力有:__________________
②胆钒晶体溶于水呈蓝色,滴加少量氨水之后得到蓝色沉淀。再滴加氨水,沉淀又逐渐溶解。请写出蓝色沉淀溶解的离子方程式:_________________ 。
⑴上述反应的催化剂含有Cu、Zn、AI等元素。写出基态Cu原子的核外电子排布式:
⑵根据等电子原理.写出CO分子的电子式:
(3)甲醇催化氧化可得到甲醛,甲醇的沸点比甲醛的高,其主要原因是
(4)胆矾结构示意图可简单表示如下,回答下列问题。
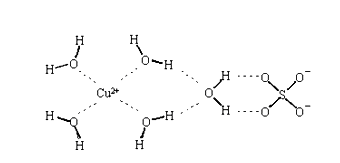
①胆矾晶体中存在的作用力有:
②胆钒晶体溶于水呈蓝色,滴加少量氨水之后得到蓝色沉淀。再滴加氨水,沉淀又逐渐溶解。请写出蓝色沉淀溶解的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】卤族元素竖跨6个周期,该族元素与人们的日常生活和工农业生产有着密切的联系。回答下列问题:
(1) (Ts)为原子序数最大的卤族元素,其基态原子的价层电子排布式为
(Ts)为原子序数最大的卤族元素,其基态原子的价层电子排布式为_______ ,与其不相邻周期的某种元素基态原子的核外电子排布式为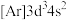 ,则该元素在元素周期表中的位置为
,则该元素在元素周期表中的位置为_______ 。
(2)路易斯毒气是氯乙烯氯砷的俗称,由美国人Lewis在1918年发明,是一种战争中常用的化学武器(毒气),结构简式可表示为 。
。 分子中含
分子中含_______  键,其中As的杂化类型是
键,其中As的杂化类型是_______ 。
(3)实验测得 蒸气以双聚分子(
蒸气以双聚分子( )的形式存在,其中所含化学键类型有
)的形式存在,其中所含化学键类型有_______ (填字母)。
a.共价键b.离子键c.配位键
某双核阳离子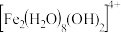 的结构如图所示,试解释其中
的结构如图所示,试解释其中 键角大于单个水分子中的
键角大于单个水分子中的 键角的原因:
键角的原因:_______ 。

(4) 在太阳能电池方面具有较广的应用空间,其晶胞结构如图所示。
在太阳能电池方面具有较广的应用空间,其晶胞结构如图所示。

若晶胞中大黑球代表 ,则小黑球代表
,则小黑球代表_______ (填“Pb”或“I”);若 晶体的密度为
晶体的密度为 ,则阿伏加德罗常数的值NA=
,则阿伏加德罗常数的值NA=_______ (用含a、d的代数式表示)。
(1)
 (Ts)为原子序数最大的卤族元素,其基态原子的价层电子排布式为
(Ts)为原子序数最大的卤族元素,其基态原子的价层电子排布式为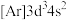 ,则该元素在元素周期表中的位置为
,则该元素在元素周期表中的位置为(2)路易斯毒气是氯乙烯氯砷的俗称,由美国人Lewis在1918年发明,是一种战争中常用的化学武器(毒气),结构简式可表示为
 。
。 分子中含
分子中含 键,其中As的杂化类型是
键,其中As的杂化类型是(3)实验测得
 蒸气以双聚分子(
蒸气以双聚分子( )的形式存在,其中所含化学键类型有
)的形式存在,其中所含化学键类型有a.共价键b.离子键c.配位键
某双核阳离子
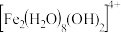 的结构如图所示,试解释其中
的结构如图所示,试解释其中 键角大于单个水分子中的
键角大于单个水分子中的 键角的原因:
键角的原因:
(4)
 在太阳能电池方面具有较广的应用空间,其晶胞结构如图所示。
在太阳能电池方面具有较广的应用空间,其晶胞结构如图所示。
若晶胞中大黑球代表
 ,则小黑球代表
,则小黑球代表 晶体的密度为
晶体的密度为 ,则阿伏加德罗常数的值NA=
,则阿伏加德罗常数的值NA=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)Cu+在基态时的价电子排布式为__________________ 。
(2)砷、硒是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度加以解释___________________________ 。
(3)GaAs熔点1238℃,难溶于溶剂。其晶体类型为_____________ 。
(4)AsF3的空间构型是:______________ 。
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为________ 。
②[B(OH)4]-的结构式为____________________ 。
(6)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅:若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是_______________________ (用化学式表示)。
②立方氮化硼(BN)晶体的结构与金刚石相似,硬度与金刚石相当,立方氮化硼的密度是ρ g·㎝-3,,则晶胞边长为___________ 。(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(1)Cu+在基态时的价电子排布式为
(2)砷、硒是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度加以解释
(3)GaAs熔点1238℃,难溶于溶剂。其晶体类型为
(4)AsF3的空间构型是:
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为
②[B(OH)4]-的结构式为
(6)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅:若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是
②立方氮化硼(BN)晶体的结构与金刚石相似,硬度与金刚石相当,立方氮化硼的密度是ρ g·㎝-3,,则晶胞边长为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】科幻电影《阿凡达》中外星人流的是蓝色的血液,其实血液的颜色主要是由血蛋白中含有的金属元素决定的,如含铁元素的为常见红色血液、含铜元素的为蓝色血液、含钒元素的为绿色血液等,铜、铁、钒在科学研究和工农业生产中有许多用途。回答下列问题:
(1)基态V的核外电子排布式为_______ 。
(2) 溶液常用作农业杀菌剂,溶液中存在
溶液常用作农业杀菌剂,溶液中存在 。该离子中存在的化学键有
。该离子中存在的化学键有_______ (填字母)。
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
(3) 与氨基吡啶形成的配合物(结构如图1)是很好的磁性材料。该配合物分子中碳与氧原子间形成的
与氨基吡啶形成的配合物(结构如图1)是很好的磁性材料。该配合物分子中碳与氧原子间形成的 键和π键的个数比为
键和π键的个数比为_______ ,其中C原子的杂化轨道类型为_______ 。

(4)铜的氧化物、氮化物都广泛应用于光信息存储和高速集成电路领域。
①Cu、O、N的电负性由大到小的顺序为_______ 。
②已知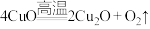 ,从铜离子的价层电子结构角度分析,高温下能转化生成
,从铜离子的价层电子结构角度分析,高温下能转化生成 的主要原因是
的主要原因是_______ 。
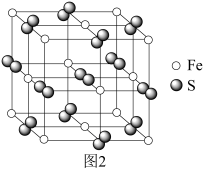
(5)铁与硫能形成多种化合物,某种化合物的晶胞结构如图2所示。该化合物的化学式是_______ ;若该晶胞边长为 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为_______  。
。
(1)基态V的核外电子排布式为
(2)
 溶液常用作农业杀菌剂,溶液中存在
溶液常用作农业杀菌剂,溶液中存在 。该离子中存在的化学键有
。该离子中存在的化学键有A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
(3)
 与氨基吡啶形成的配合物(结构如图1)是很好的磁性材料。该配合物分子中碳与氧原子间形成的
与氨基吡啶形成的配合物(结构如图1)是很好的磁性材料。该配合物分子中碳与氧原子间形成的 键和π键的个数比为
键和π键的个数比为
(4)铜的氧化物、氮化物都广泛应用于光信息存储和高速集成电路领域。
①Cu、O、N的电负性由大到小的顺序为
②已知
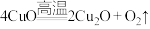 ,从铜离子的价层电子结构角度分析,高温下能转化生成
,从铜离子的价层电子结构角度分析,高温下能转化生成 的主要原因是
的主要原因是(5)铁与硫能形成多种化合物,某种化合物的晶胞结构如图2所示。该化合物的化学式是
 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】钛被称为继铁、铝之后的第三金属,性能优越,广泛用于航天航空等领域,有人说“21世纪将是钛的世纪”。冶炼金属钛的主要原料为钛铁矿(主要成分FeTiO3,含FeO、Fe2O3等杂质),其冶炼过程如图所示,除了得到金属钛,还可以得到副产物绿矾(FeSO4·7H2O)。
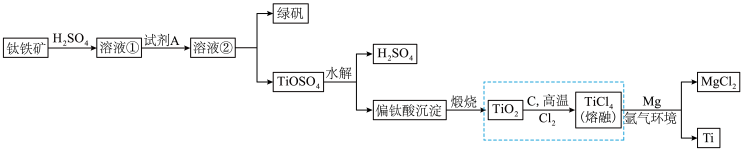
(1)Ti在元素周期表中的位置为___________ , 的键角
的键角___________ H2O分子的键角(填 “>”“<”或“=”)。
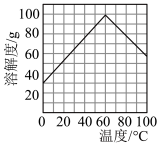
(2)试剂A为___________ 。已知绿矾的溶解度随温度变化的曲线如图所示,从溶液②获得绿矾的操作方法为___________ 、过滤、洗涤、干燥。
(3)已知常温下,Ksp[Fe(OH)2]=8×10-16,若溶液②中c(Fe2+)=0.5mol/L,为防止生成Fe(OH)2沉淀,溶液的pH不超过___________ (lg2=0.3)。
(4)TiOSO4水解生成偏钛酸(H2TiO3)沉淀的化学方程式为___________ 。
(5)TiCl4的水解程度很大,可以利用其稀溶液制备纳米级TiO2·xH2O,该反应的化学方程式为___________ 。

(1)Ti在元素周期表中的位置为
 的键角
的键角(2)试剂A为

(3)已知常温下,Ksp[Fe(OH)2]=8×10-16,若溶液②中c(Fe2+)=0.5mol/L,为防止生成Fe(OH)2沉淀,溶液的pH不超过
(4)TiOSO4水解生成偏钛酸(H2TiO3)沉淀的化学方程式为
(5)TiCl4的水解程度很大,可以利用其稀溶液制备纳米级TiO2·xH2O,该反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】碳、氮和磷元素是几乎所有的生物体中均含有的生命元素。回答下列问题:
(1)叠氮酸(HN3)是一种弱酸,在水中能微弱电离出H+和 ,分子中的大Π键可用符号
,分子中的大Π键可用符号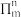 表示,其中m代表参与形成大Π键的原子数,n代表参与形成大Π键的电子数(如苯分子中的大Π键可表示为
表示,其中m代表参与形成大Π键的原子数,n代表参与形成大Π键的电子数(如苯分子中的大Π键可表示为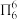 ,则
,则 中的大Π键应表示为
中的大Π键应表示为__________________ 。
(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以 和
和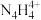 两种离子的形式存在。
两种离子的形式存在。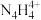 中N原子均为sp3杂化,请推测
中N原子均为sp3杂化,请推测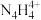 的结构式:
的结构式:_______________________ 。
(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因:____________________________ 。
(4)ATP(三磷酸腺苷)是一种高能磷酸化合物,在细胞中,它与ADP的相互转化实现贮能和放能,从而保证了细胞各项生命活动的能量供应。ATP的结构简式如图1所示。
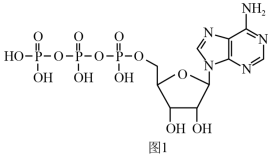 分子中属于sp2杂化的N原子有
分子中属于sp2杂化的N原子有_______________ 个。
(5)某种磁性氮化铁的晶胞结构如图2所示。

①基态Fe原子的电子排布式为______________________ 。
②该化合物的化学式为___________________________ 。
③若晶胞底边长为anm,高为cnm,NA为阿伏加 德罗常数的值,则该磁性氮化铁的晶体密度为__________________ g.cm-3(用含a、c、NA的代数式表示)。
(1)叠氮酸(HN3)是一种弱酸,在水中能微弱电离出H+和
 ,分子中的大Π键可用符号
,分子中的大Π键可用符号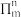 表示,其中m代表参与形成大Π键的原子数,n代表参与形成大Π键的电子数(如苯分子中的大Π键可表示为
表示,其中m代表参与形成大Π键的原子数,n代表参与形成大Π键的电子数(如苯分子中的大Π键可表示为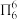 ,则
,则 中的大Π键应表示为
中的大Π键应表示为(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以
 和
和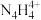 两种离子的形式存在。
两种离子的形式存在。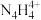 中N原子均为sp3杂化,请推测
中N原子均为sp3杂化,请推测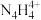 的结构式:
的结构式:(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因:
(4)ATP(三磷酸腺苷)是一种高能磷酸化合物,在细胞中,它与ADP的相互转化实现贮能和放能,从而保证了细胞各项生命活动的能量供应。ATP的结构简式如图1所示。
 分子中属于sp2杂化的N原子有
分子中属于sp2杂化的N原子有(5)某种磁性氮化铁的晶胞结构如图2所示。

①基态Fe原子的电子排布式为
②该化合物的化学式为
③若晶胞底边长为anm,高为cnm,NA为阿伏加 德罗常数的值,则该磁性氮化铁的晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】腺嘌呤核苷和腺嘌呤核苷酸是生产核酸类药物的中间体,结构如图所示。

(1)磷酸分子中σ键与π键之比为___________ 。
(2)已知基态N、O原子的第一电离能(I1)分别为1402kJ/mol和1314kJ/mol,I1(N)>I1(O),原因是___________ 。
(3)下列不同状态的碳原子中,失去一个电子需要吸收能量最多的是___________(填标号)。
(4)从实验测得不同物质中氧-氧之间的键长和键能的数据:
说明同种原子形成共价键,___________ ,键长越长,键能越小。
(5)GaN(相对分子质量为M)是新型半导体材料,该晶体的一种晶胞结构与金刚石晶胞(如图所示)相似,其晶胞可看作金刚石晶胞内部的碳原子被N原子替代,顶点和面心的碳原子被Ga原子替代,晶胞参数为acm,沿Z轴从上往下俯视的晶胞投影图如下图所示:

①若图中原子1的分数坐标是( ,
, ,
, ),则原子5的分数坐标是
),则原子5的分数坐标是___________ 。
②晶胞结构中原子1、5之间的距离为___________ cm。(用含a的式子表示)
③设阿伏加德罗常数的值为NA,则GaN晶体的密度为___________  (用含M的式子表示)
(用含M的式子表示)

(1)磷酸分子中σ键与π键之比为
(2)已知基态N、O原子的第一电离能(I1)分别为1402kJ/mol和1314kJ/mol,I1(N)>I1(O),原因是
(3)下列不同状态的碳原子中,失去一个电子需要吸收能量最多的是___________(填标号)。
A. | B.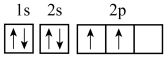 |
C. | D.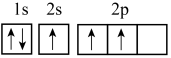 |
 | O2 | |
键长(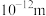 ) ) | 149 | 121 |
键能( ) ) | 126 | 494 |
(5)GaN(相对分子质量为M)是新型半导体材料,该晶体的一种晶胞结构与金刚石晶胞(如图所示)相似,其晶胞可看作金刚石晶胞内部的碳原子被N原子替代,顶点和面心的碳原子被Ga原子替代,晶胞参数为acm,沿Z轴从上往下俯视的晶胞投影图如下图所示:

①若图中原子1的分数坐标是(
 ,
, ,
, ),则原子5的分数坐标是
),则原子5的分数坐标是②晶胞结构中原子1、5之间的距离为
③设阿伏加德罗常数的值为NA,则GaN晶体的密度为
 (用含M的式子表示)
(用含M的式子表示)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】将汽车尾气中含有的CO利用不仅能有效利用资源.还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)图l是某同学画出CO分子中碳原子的核外电子排布图。

请判断该排布图____ (填“正确”或“错误”) ,理由是________ (若判断正确,该空不用回答)。
(2)写出两种与CO互为等电子体的离子________ 。
(3)往硫酸铜溶液中通入过量的NH3,可生成配离子[Cu(NH3 )4]2+,但NF3不易与Cu2+形成配离子,其原因是_________ ,在配离子[Cu(NH3 )4]2+中所含配位键是通过配体分子的_____ 给出孤电子对,____ 接受电子对形成。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是______ ;在甲醇分子中碳原子轨道的杂化类型为_____ 。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图2所示。
①在该晶胞中,Cu+的配位数是_____ 。
②若该晶胞的边长为apm,则Cu2O的密度为_____ g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(1)图l是某同学画出CO分子中碳原子的核外电子排布图。

请判断该排布图
(2)写出两种与CO互为等电子体的离子
(3)往硫酸铜溶液中通入过量的NH3,可生成配离子[Cu(NH3 )4]2+,但NF3不易与Cu2+形成配离子,其原因是
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图2所示。
①在该晶胞中,Cu+的配位数是
②若该晶胞的边长为apm,则Cu2O的密度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量Fe3O4、FeO、CoO、Al2O3)为原料制备Mn2O3的工艺流程如图。
已知:氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
(1)MnOOH中Mn的化合价为______ 价。
(2)向“沉淀池I”中加入MnO2,MnO2的作用是______ ,在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为______ (当溶液中某离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全)。
(3)MnSO4转化为MnOOH的离子方程式为_______ 。
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为______ 。
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。______ 。
②已知:MnS晶体的密度为ρg•cm-3,NA为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为______ pm(列出计算式即可)。
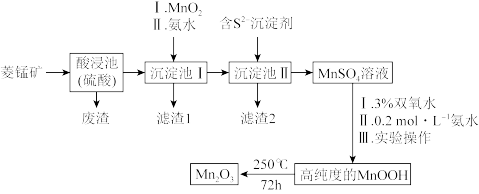
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
(1)MnOOH中Mn的化合价为
(2)向“沉淀池I”中加入MnO2,MnO2的作用是
(3)MnSO4转化为MnOOH的离子方程式为
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。

②已知:MnS晶体的密度为ρg•cm-3,NA为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】已知A、B、C、D、E、F、G都是周期表中前四周期的元素,他们的原子序数依次增大。其中A原子的L层有2个未成对电子。D是电负性最大的元素,E与F同主族,E的二价阳离子与C的阴离子具有相同的电子层结构。G3+离子3d轨道电子为半满状态。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
⑴A、B、C的第一电离能由小到大的顺序为_____________ 。D的核外有____ 种运动状态不同的电子。
⑵A的最简单氢化物属于______ (填“极性分子”和“非极性分子”)。AH3+离子空间构型是________ ,其中心原子采取______ 杂化。
⑶G和M (质子数为25)两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态G2+再失去一个电子难。其原因是____________ ;
⑷晶体熔点:EC____ FC (填“ > ”、“<”或“=”),原因是_______________ 。
(5)H2S和C元素的一种氢化物(分子式为H2C2)的主要物理性质比较如下:
h2s和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因___________ 。
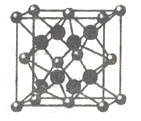
(6)FD2晶胞如图,已知DF核间距为a pm,则该晶体密度ρ=______ g•㎝-3(用带a、NA的算式表示,不必化简)
⑴A、B、C的第一电离能由小到大的顺序为
⑵A的最简单氢化物属于
⑶G和M (质子数为25)两元素的部分电离能数据列于下表:
| 元素 | M | G | |
| 电离能 (kJ•mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态G2+再失去一个电子难。其原因是
⑷晶体熔点:EC
(5)H2S和C元素的一种氢化物(分子式为H2C2)的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| h2s | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
h2s和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因
(6)FD2晶胞如图,已知DF核间距为a pm,则该晶体密度ρ=
您最近一年使用:0次



