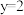利用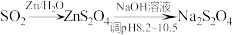 转化制取连二亚硫酸钠(
转化制取连二亚硫酸钠( )的装置如图。下列说法不正确的是
)的装置如图。下列说法不正确的是
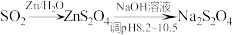 转化制取连二亚硫酸钠(
转化制取连二亚硫酸钠( )的装置如图。下列说法不正确的是
)的装置如图。下列说法不正确的是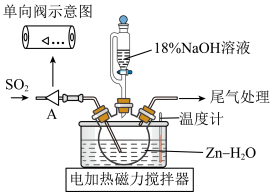
| A.单向阀的作用是防倒吸 |
B.先通入 至悬浊液变澄清,再打开滴液漏斗旋塞 至悬浊液变澄清,再打开滴液漏斗旋塞 |
C.NaOH溶液不宜加入过多的原因是防止 水解 水解 |
| D.上述反应液经过滤,在冷却搅拌下加入一定量NaCl的作用是提高产率 |
更新时间:2023-08-14 18:18:06
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】关于下列常温下的水溶液的说法正确的是
A.向水中加入 溶液仍显中性,水的电离平衡不移动 溶液仍显中性,水的电离平衡不移动 |
B.加水稀释亚硫酸( )溶液, )溶液, 始终不变 始终不变 |
| C.将pH=3的醋酸与pH=11的NaOH溶液等体积混合后溶液呈中性 |
D.相同 的溶质的物质的量浓度: 的溶质的物质的量浓度: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】20℃时,0.1 mol • L-1 NH4Al(SO4)2溶液的pH随温度变化的关系如曲线Ⅰ所示,下列说法中正确的是
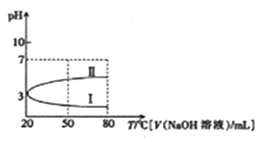
| A.0.1mol·L-1的NH4Al(SO4)2溶液中c(NH4+)大于等浓度的NH4HSO4溶液中的c(NH4+) |
| B.0.1mol·L-1的NH4Al(SO4)2溶液中:2c(SO42-)-c(NH4+)-3c(Al3+)=10-3mol·L-1 |
| C.向100mL0.1mol·L-1的NH4Al(SO4)2溶液中逐渐滴加80mL0.05mol·L-1NaOH溶液时,溶液pH的变化如曲线Ⅱ |
| D.升高温度,NH4Al(SO4)2溶液的pH减小,是因为促进了NH4Al(SO4)2的电离 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】25℃,某混合溶液中c(A-)+c(HA)=0.01mol/L,改变溶液的pH,1gc(HA)、1gc(A-)、lgc(H+)和1gc(OH-)随pH变化的关系如图所示。Ka为HA的电离常数。
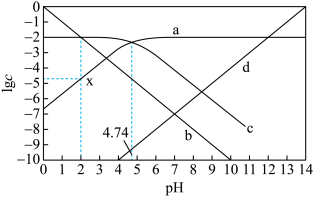
下列叙述错误的是

下列叙述错误的是
| A.pH=10时,c(A-)﹥c(OH-)﹥c(HA) |
| B.0.01mol/LNaA溶液的pH约等于线c与线d交点处的横坐标值 |
| C.pH由7到14的变化过程中,A-的水解程度始终增大 |
| D.HA电离常数的数量级为10-5,图中点x的纵坐标值为-4.74 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】溶液中存在: 、
、 。已知25℃时
。已知25℃时 或
或 浓度的负对数(
浓度的负对数(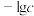 )与pH的关系如图,下列说法不正确的是
)与pH的关系如图,下列说法不正确的是

 、
、 。已知25℃时
。已知25℃时 或
或 浓度的负对数(
浓度的负对数(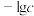 )与pH的关系如图,下列说法不正确的是
)与pH的关系如图,下列说法不正确的是
A.据图可计算 约为 约为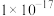 |
B. 时溶液中 时溶液中 |
C.调节 饱和溶液pH至6,R元素仍主要以 饱和溶液pH至6,R元素仍主要以 存在 存在 |
D.向0.5L、 的溶液中通入0.2mol HCl,R元素在溶液中的主要存在形式仍为 的溶液中通入0.2mol HCl,R元素在溶液中的主要存在形式仍为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
真题
解题方法
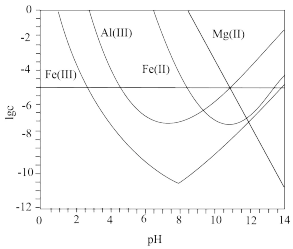
【推荐2】锂辉石是锂的重要来源,其焙烧后的酸性浸出液中含有 和
和 杂质离子,可在0~14范围内调节
杂质离子,可在0~14范围内调节 对其净化(即相关离子浓度
对其净化(即相关离子浓度 )。
)。 时,
时, 与
与 关系见下图(碱性过强时
关系见下图(碱性过强时 和
和 会部分溶解)。下列说法正确的是
会部分溶解)。下列说法正确的是
 和
和 杂质离子,可在0~14范围内调节
杂质离子,可在0~14范围内调节 对其净化(即相关离子浓度
对其净化(即相关离子浓度 )。
)。 时,
时, 与
与 关系见下图(碱性过强时
关系见下图(碱性过强时 和
和 会部分溶解)。下列说法正确的是
会部分溶解)。下列说法正确的是
A. 可被净化的 可被净化的 区间最大 区间最大 |
B.加入适量 ,可进一步提升净化程度 ,可进一步提升净化程度 |
C.净化的先后顺序: |
D.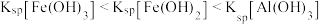 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列实验操作正确的是( )
| A.洗净的容量瓶可以放进烘箱中烘干 |
| B.用带磨口玻璃瓶塞的玻璃保存NaOH溶液 |
| C.用苯萃取溴水中的溴时,溴的苯溶液从分液漏斗的下口放出 |
| D.用二硫化碳清洗残留在试管壁上少量的硫粉 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】工业碳酸钠纯度约为98%,其中含有Mg2+、Fe2+、Cl-和SO 等杂质,提纯工艺流程如下:
等杂质,提纯工艺流程如下:
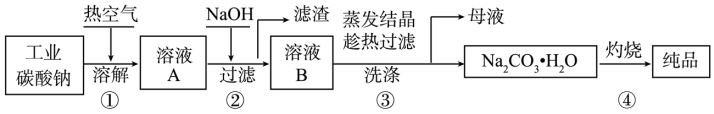
下列说法不正确的是
 等杂质,提纯工艺流程如下:
等杂质,提纯工艺流程如下:
下列说法不正确的是
| A.步骤①,通入热空气可加快溶解速率 |
B.步骤②,产生滤渣的离子反应为: |
C.步骤③,趁热过滤时温度控制不当会使 中混有 中混有 等杂质 等杂质 |
| D.步骤④,灼烧时用到的主要仪器有铁坩埚、泥三角、三脚架、酒精灯 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】冰晶石(Na3AlF6)微溶于水,工业上用萤石(CaF2含量为96%)、二氧化硅为原料,采用氟硅酸钠法制备冰晶石,其工艺流程如图:
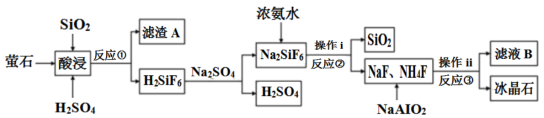
据此分析,下列观点不正确的是

据此分析,下列观点不正确的是
| A.滤渣A的主要成分是CaSO4 |
| B.上述流程中,所涉反应均为非氧化还原反应 |
| C.“操作i”可用硅酸盐质设备进行分离 |
| D.流程中可循环使用的物质除H2SO4、SiO2外,滤液B经浓缩后也能循环使用 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】以非水溶性钾长石(K2OAl2O36SiO2)为原料提取Al2O3、K2CO3等物质的流程如图:

下列说法错误的是

下列说法错误的是
| A.“浸液”中金属阳离子主要有K+、Na+、Al3+ |
B.“碱化”反应为:OH-+HCO =CO =CO +H2O +H2O |
| C.“过滤”所需玻璃仪器:普通漏斗、烧杯、玻璃棒 |
| D.Na2CO3、CO2可在流程中循环利用 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】MgCl2-6NH3,具有极好的可逆吸、放氨特性,是一种优良的储氨材料。实验室用无水MgCl2制备MgCl2-6NH3的装置图如下:

已知:(1)与Mg2+结合能力:H2O>NH3>HOCH2CH2OH>CH3OH;
(2)相关物质的性质见上表。
下列说法不正确的是

| 溶剂 溶解性 | 氨气 | 氯化镁 | 六氨氯化镁 |
| 水 | 易溶 | 易溶 | 易溶 |
| 甲醇(沸点65℃) | 易溶 | 易溶 | 难溶 |
| 乙二醇(沸点197℃) | 易溶 | 易溶 | 难溶 |
(2)相关物质的性质见上表。
下列说法不正确的是
| A.球形干燥管中盛装碱石灰,作用是尾气处理 |
| B.在空气中直接加热MgCl2-6H2O晶体得不到纯的无水MgCl2 |
| C.冰水浴有利于MgCl2-6NH3结晶析出 |
| D.洗涤MgCl2-6NH3晶体时可以选择甲醇 |
您最近一年使用:0次

 是一元弱酸,难溶盐
是一元弱酸,难溶盐 的悬浊液中,
的悬浊液中, 不发生水解。实验发现,
不发生水解。实验发现, 时,
时, 、
、 的关系如图所示:
的关系如图所示:
 表示
表示 的关系
的关系