按要求回答下列问题:
(1)KHSO4溶液显______ 性(填“酸”“碱”或“中”)。其原因是(用电离方程式表示):_______ 。
(2)KHCO3溶液显______ 性(填“酸”“碱”或“中”),其原因是(用离子方程式表示):_______ 。
(3)将上述两溶液混合,离子反应方程式为_______ 。
(1)KHSO4溶液显
(2)KHCO3溶液显
(3)将上述两溶液混合,离子反应方程式为
更新时间:2023/08/27 20:22:44
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】有下列物质:①Ba(OH)2固体;②熔融的KHSO4;③浓HNO3;④稀硫酸;⑤CO2;⑥铜;⑦氨水;⑧蔗糖晶体;⑨NaHCO3固体,⑩纯醋酸(CH3COOH)。
(1)上述状态 下的物质可导电的是___________ (填序号,下同);属于电解质的是___________ 。
(2)写出②的电离方程式:___________ 。
(3)写出向①的水溶液中通入少量⑤的离子方程式:___________ 。
(4)写出⑦和⑨反应的离子方程式:___________ 。
(5)向①溶液中滴加⑨溶液,当Ba2+恰好沉淀完全时,溶液显___________ (填“酸”碱”或“中”)性。
(6)如图所示为实验室制备氢氧化铁胶体的装置,请回答下列问题:
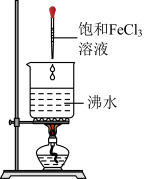
①证明已经制得Fe(OH)3胶体的实验现象是___________ ;
②Fe(OH)3胶体提纯的方法是___________ (填名称),请写出制备Fe(OH)3胶体的离子方程式:___________ 。
(1)上述状态 下的物质可导电的是
(2)写出②的电离方程式:
(3)写出向①的水溶液中通入少量⑤的离子方程式:
(4)写出⑦和⑨反应的离子方程式:
(5)向①溶液中滴加⑨溶液,当Ba2+恰好沉淀完全时,溶液显
(6)如图所示为实验室制备氢氧化铁胶体的装置,请回答下列问题:

①证明已经制得Fe(OH)3胶体的实验现象是
②Fe(OH)3胶体提纯的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求完成下列方程式的书写:
(1)写出下列物质的电离方程式:
① HCl:___________________________________________________
② NaOH:___________________________________________________
(2)写出下列反应的离子方程式:
① NaOH与HCl反应:___________________________________________
② Na2CO3与CaCl2反应:___________________________________________
(1)写出下列物质的电离方程式:
① HCl:
② NaOH:
(2)写出下列反应的离子方程式:
① NaOH与HCl反应:
② Na2CO3与CaCl2反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有下列10种物质:① ;②
;② 固体;③熔融
固体;③熔融 ;④饱和
;④饱和 溶液;⑤铜;⑥
溶液;⑤铜;⑥ ;⑦
;⑦ ;⑧稀硫酸;⑨蔗糖;⑩NaOH固体。请回答下列问题:
;⑧稀硫酸;⑨蔗糖;⑩NaOH固体。请回答下列问题:
(1)上述物质中,非电解质有______ (填标号,下同);电解质有______ ;能导电的有______ 。
(2)②溶于水的电离方程式为______ ;③的电离方程式为______ 。
(3)分析⑥溶于水后能导电的原因:______ 。
(4)利用④可制得 胶体,用聚光手电筒照射
胶体,用聚光手电筒照射 胶体时,在垂直于光线的方向可观察到
胶体时,在垂直于光线的方向可观察到______ ; 胶体的粒子具有
胶体的粒子具有______ 性,因此可用 胶体净水。
胶体净水。
 ;②
;② 固体;③熔融
固体;③熔融 ;④饱和
;④饱和 溶液;⑤铜;⑥
溶液;⑤铜;⑥ ;⑦
;⑦ ;⑧稀硫酸;⑨蔗糖;⑩NaOH固体。请回答下列问题:
;⑧稀硫酸;⑨蔗糖;⑩NaOH固体。请回答下列问题:(1)上述物质中,非电解质有
(2)②溶于水的电离方程式为
(3)分析⑥溶于水后能导电的原因:
(4)利用④可制得
 胶体,用聚光手电筒照射
胶体,用聚光手电筒照射 胶体时,在垂直于光线的方向可观察到
胶体时,在垂直于光线的方向可观察到 胶体的粒子具有
胶体的粒子具有 胶体净水。
胶体净水。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】写出下列各步转化的离子方程式:CuO CuCl2
CuCl2 Cu(OH)2
Cu(OH)2 CuSO4。
CuSO4。
①_____ ;②_____ ;③_____ 。
 CuCl2
CuCl2 Cu(OH)2
Cu(OH)2 CuSO4。
CuSO4。①
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】有以下几种物质:①锌丝;②CO2;③75%酒精溶液;④稀盐酸;⑤H2SO4;⑥NaOH固体;⑦熔融KNO3。
(1)以上物质属于单质的是____ (填序号,下同),属于电解质的是____ ,属于非电解质的是_____ 。
(2)①与⑤的稀溶液反应的化学方程式为____ 。
(3)写出硝酸银溶液与④反应的离子方程式是____ 。
(4)在发生离子反应的反应物或生成物中,一定存在的是____ (填字母)。
(5)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表____ 。
(6)根据酸能电离出H+的数目可将酸分为一元酸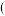 如HCl、二元酸(如H2CO3)、三元酸如(H3PO4),二元酸能与碱反应生成一种正盐(如Na2CO3)和一种酸式盐(如NaHCO3);三元酸能与碱反应生成一种正盐(如Na3PO4)和两种酸式盐(如NaH2PO4、NaH2PO4)。
如HCl、二元酸(如H2CO3)、三元酸如(H3PO4),二元酸能与碱反应生成一种正盐(如Na2CO3)和一种酸式盐(如NaHCO3);三元酸能与碱反应生成一种正盐(如Na3PO4)和两种酸式盐(如NaH2PO4、NaH2PO4)。
①H2SO3是二元酸,写出它与Ba(OH)2反应生成的酸式盐的方程式____ 。
②H3PO3能与KOH反应生成两种盐,则H3PO3是____ 元酸,生成的正盐的方程式_____ 。
(1)以上物质属于单质的是
(2)①与⑤的稀溶液反应的化学方程式为
(3)写出硝酸银溶液与④反应的离子方程式是
(4)在发生离子反应的反应物或生成物中,一定存在的是
| A.单质 | B.氧化物 | C.酸 | D.化合物 |
(6)根据酸能电离出H+的数目可将酸分为一元酸
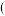 如HCl、二元酸(如H2CO3)、三元酸如(H3PO4),二元酸能与碱反应生成一种正盐(如Na2CO3)和一种酸式盐(如NaHCO3);三元酸能与碱反应生成一种正盐(如Na3PO4)和两种酸式盐(如NaH2PO4、NaH2PO4)。
如HCl、二元酸(如H2CO3)、三元酸如(H3PO4),二元酸能与碱反应生成一种正盐(如Na2CO3)和一种酸式盐(如NaHCO3);三元酸能与碱反应生成一种正盐(如Na3PO4)和两种酸式盐(如NaH2PO4、NaH2PO4)。①H2SO3是二元酸,写出它与Ba(OH)2反应生成的酸式盐的方程式
②H3PO3能与KOH反应生成两种盐,则H3PO3是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”字样。
(1)“石灰干燥剂”的主要成分生石灰的化学式为___________ 。
(2)按物质的性质分类,生石灰属于___________ (填序号)。
①金属氧化物②碱性氧化物③碱④化合物⑤盐
生石灰与盐酸反应的离子方程式为___________ 。
(3)生石灰可作干燥剂的理由是___________ (用化学方程式表示)。
(4)某同学将浓硫酸、氢氧化钠固体、生石灰等物质划分为一类,该同学的分类依据为________。
(1)“石灰干燥剂”的主要成分生石灰的化学式为
(2)按物质的性质分类,生石灰属于
①金属氧化物②碱性氧化物③碱④化合物⑤盐
生石灰与盐酸反应的离子方程式为
(3)生石灰可作干燥剂的理由是
(4)某同学将浓硫酸、氢氧化钠固体、生石灰等物质划分为一类,该同学的分类依据为________。
| A.酸类 | B.碱类 | C.氧化物 | D.干燥剂 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】用离子方程式表示下列反应:
(1)某可溶性盐的化学式XmYn(是最简结构m≠n),将一定量的该盐溶于足量的水中,若测得溶液的pH为3,该盐水解的离子方程式可能为___________ 。若测得溶液的pH为11,则该盐与水反应的离子方程式可能为___________ 。
(2)NH4Cl溶液与Na反应___________ 。
(3)AlCl3溶液与NaAlO2溶液反应___________ 。
(4)CuSO4溶液与Na2S溶液反应___________ 。
(5)NaHSO4溶液与NaHCO3溶液反应___________ 。
(6)FeCl3溶液与NaI溶液反应___________ 。
(1)某可溶性盐的化学式XmYn(是最简结构m≠n),将一定量的该盐溶于足量的水中,若测得溶液的pH为3,该盐水解的离子方程式可能为
(2)NH4Cl溶液与Na反应
(3)AlCl3溶液与NaAlO2溶液反应
(4)CuSO4溶液与Na2S溶液反应
(5)NaHSO4溶液与NaHCO3溶液反应
(6)FeCl3溶液与NaI溶液反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】描述弱电解质电离情况可以用电离度和电离平衡常数表示,表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)
表1
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是________ (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是________ (填字母序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈________ (选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是_____________________________ 。
(3)物质的量之比为1∶1的NaCN和HCN的混合溶液,其pH >7,该溶液中离子浓度从大到小的排列为________________________ 。
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3·H2O | 1.8×10-5 |
表1
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈
(3)物质的量之比为1∶1的NaCN和HCN的混合溶液,其pH >7,该溶液中离子浓度从大到小的排列为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电离常数是研究弱电解质的重要工具,25℃时一些酸的电离常数如下表所示。
请回答:
(1)浓度相同的阴离子在水溶液中结合H+的能力:
_______  (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
(2)25℃时,pH相同的NaClO和 两种溶液的浓度大小:
两种溶液的浓度大小: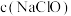
_______  (填“<”、“>”或“=”)。。
(填“<”、“>”或“=”)。。
(3)硫酸在水溶液中是强酸,在冰醋酸中部分电离,写出硫酸在冰醋酸中的电离方程式_______ 。
(4)向NaClO溶液中通入少量的 气体,写出发生反应的离子方程式
气体,写出发生反应的离子方程式_______ 。
(5)25℃时, 的水解平衡常数
的水解平衡常数
_______ (结果保留2位有效数字)。
| 化学式 |  |  | HClO |
电离常数( ) ) |  | 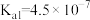 、 、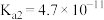 |  |
(1)浓度相同的阴离子在水溶液中结合H+的能力:

 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。(2)25℃时,pH相同的NaClO和
 两种溶液的浓度大小:
两种溶液的浓度大小: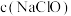
 (填“<”、“>”或“=”)。。
(填“<”、“>”或“=”)。。(3)硫酸在水溶液中是强酸,在冰醋酸中部分电离,写出硫酸在冰醋酸中的电离方程式
(4)向NaClO溶液中通入少量的
 气体,写出发生反应的离子方程式
气体,写出发生反应的离子方程式(5)25℃时,
 的水解平衡常数
的水解平衡常数
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】海水中富含镁,可经过通入氨气沉淀、过滤、酸溶、结晶及脱水等步骤得到无水氯化镁,最后电解得到金属镁。
(1)MgCl2溶液显酸性,其水解的离子方程式为_________________________________________ 。
(2)除去MgCl2酸性溶液中少量FeCl2的方法是____________________________________ 。
(3)如何通过MgCl2·6H2O加热得到无水MgCl2_________________________________________ 。
(4)泡沫灭火器的工作原理(用化学方程式表示)_________________________________________ 。
(5)同浓度的下列溶液:①(NH4)2SO4 ②NH4Cl ③Na2CO3 ④NaHCO3,其中pH 由大到小的顺序是_________ 。(填序号)
(1)MgCl2溶液显酸性,其水解的离子方程式为
(2)除去MgCl2酸性溶液中少量FeCl2的方法是
(3)如何通过MgCl2·6H2O加热得到无水MgCl2
(4)泡沫灭火器的工作原理(用化学方程式表示)
(5)同浓度的下列溶液:①(NH4)2SO4 ②NH4Cl ③Na2CO3 ④NaHCO3,其中pH 由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有SO32-、NH4+、Al3+、Na+、SO42-、AlO2-、Fe3+、HCO3-、Cl-等离子,请按要求填空:
(1)在水溶液中,离子水解呈碱性的是________ 。
(2)在水溶液中,离子水解呈酸性的是________ 。
(3)既能在酸性较强的溶液里大量存在,又能在碱性较强的溶液里大量存在的离子有________ 。
(4)既不能在酸性较强的溶液里大量存在,又不能在碱性较强的溶液里大量存在的离子有________ 。
(1)在水溶液中,离子水解呈碱性的是
(2)在水溶液中,离子水解呈酸性的是
(3)既能在酸性较强的溶液里大量存在,又能在碱性较强的溶液里大量存在的离子有
(4)既不能在酸性较强的溶液里大量存在,又不能在碱性较强的溶液里大量存在的离子有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】有下列物质:①NaOH②HCl③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩ ,回答下列问题:
,回答下列问题:
(1)上述物质的水溶液显酸性的是___________ ;其中水解显酸性的是___________ 。
(2)上述物质的水溶液显碱性的是___________ ;其中水解显碱性的是___________ 。
(3)上述物质的水溶液存在电离平衡的是___________ 。(不包括水的电离平衡)
(4)上述物质促进水的电离的是___________ 。
(5)上述物质抑制水的电离的是___________ 。
(6)上述物质的水溶液可能存在沉淀溶解平衡的是___________ 。
 ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩ ,回答下列问题:
,回答下列问题:(1)上述物质的水溶液显酸性的是
(2)上述物质的水溶液显碱性的是
(3)上述物质的水溶液存在电离平衡的是
(4)上述物质促进水的电离的是
(5)上述物质抑制水的电离的是
(6)上述物质的水溶液可能存在沉淀溶解平衡的是
您最近一年使用:0次



