—定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为 ):
):
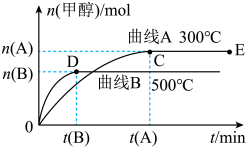
根据题意完成下列问题:
(1)反应达到平衡时,平衡常数表达式
_____ ,升高温度,K值_____ (填“增大”“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率
_____ 。
(3)在其他条件不变的情况下,将处于E点的体系体积压缩到原来的 ,下列有关该体系的说法正确的是_____。
,下列有关该体系的说法正确的是_____。
(4)据研究,反应过程中起催化作用的为 ,反应物CO的还原性会造成催化剂损耗,而反应体系中提高
,反应物CO的还原性会造成催化剂损耗,而反应体系中提高 浓度有利于维持催化剂
浓度有利于维持催化剂 的量不变,请结合相关的方程式从平衡移动的角度分析原因
的量不变,请结合相关的方程式从平衡移动的角度分析原因_____ 。
 ):
):

根据题意完成下列问题:
(1)反应达到平衡时,平衡常数表达式

(2)在500℃,从反应开始到平衡,氢气的平均反应速率

(3)在其他条件不变的情况下,将处于E点的体系体积压缩到原来的
 ,下列有关该体系的说法正确的是_____。
,下列有关该体系的说法正确的是_____。| A.氢气的浓度减少 | B.正反应速率加快,逆反应速率也加快 |
| C.甲醇的物质的量增加 | D.重新平衡时 增大 增大 |
 ,反应物CO的还原性会造成催化剂损耗,而反应体系中提高
,反应物CO的还原性会造成催化剂损耗,而反应体系中提高 浓度有利于维持催化剂
浓度有利于维持催化剂 的量不变,请结合相关的方程式从平衡移动的角度分析原因
的量不变,请结合相关的方程式从平衡移动的角度分析原因
22-23高一下·上海徐汇·期末 查看更多[2]
更新时间:2023-07-18 12:19:42
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)某温度时,在10 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如下表中数据
①体系中发生反应的化学方程式是__________________________________________________
②该反应在0~5 min时间内产物Z的平均反应速率:______________________ ;
③该反应达到平衡时反应物X的转化率α等于________ 。
(2)在密闭容器里,通入x mol H2(g)和y mol I2(g),发生反应:H2(g)+I2(g) 2HI(g) ΔH <0。改变下列条件,反应速率将如何改变?(选填“增大”“减小”或“不变”)
2HI(g) ΔH <0。改变下列条件,反应速率将如何改变?(选填“增大”“减小”或“不变”)
①升高温度________ ;
②加入催化剂________ ;
③充入更多的H2________ ;
④保持容器中压强不变,充入氖气________ ;
⑤保持容器容积不变,通入氖气________ ;
⑥保持压强不变,充入2x mol H2(g)和2y mol I2(g)________ 。
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 2.00 | 0.00 |
| 1 | 0.90 | 1.80 | 0.20 |
| 3 | 0.75 | 1.50 | 0.50 |
| 5 | 0.65 | 1.30 | 0.70 |
| 9 | 0.55 | 1.10 | 0.90 |
| 10 | 0.55 | 1.10 | 0.90 |
| 14 | 0.55 | 1.10 | 0.90 |
②该反应在0~5 min时间内产物Z的平均反应速率:
③该反应达到平衡时反应物X的转化率α等于
(2)在密闭容器里,通入x mol H2(g)和y mol I2(g),发生反应:H2(g)+I2(g)
 2HI(g) ΔH <0。改变下列条件,反应速率将如何改变?(选填“增大”“减小”或“不变”)
2HI(g) ΔH <0。改变下列条件,反应速率将如何改变?(选填“增大”“减小”或“不变”)①升高温度
②加入催化剂
③充入更多的H2
④保持容器中压强不变,充入氖气
⑤保持容器容积不变,通入氖气
⑥保持压强不变,充入2x mol H2(g)和2y mol I2(g)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)氨为重要化工原料,有广泛用途。合成氨中的氢气可由下列反应制取:
a.CH4(g)+H2O(g) CO(g)+3H2(g) △H=+216.4KJ/mol
CO(g)+3H2(g) △H=+216.4KJ/mol
b.CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2kJ/mol
CO2(g)+H2(g) △H=-41.2kJ/mol
则反应CH4(g)+2H2O(g) CO2(g)+4H2(g) △H=
CO2(g)+4H2(g) △H=______
(2)乙醇是酒精饮料的主要成分,由葡萄糖发酵生成,反应的化学方程式为:C6H12O6(aq)→2C2H5OH(aq)+2CO2(g),当C6H12O6减少的速率为0.23mol•L-1•h-1时,C2H5OH增加的速率是__
(3)1mol CH4(l)完全燃烧生成CO2(g)与H2O(1),放出热量889.6kJ,写出反应的热化学方程式_________ 。
a.CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=+216.4KJ/mol
CO(g)+3H2(g) △H=+216.4KJ/molb.CO(g)+H2O(g)
 CO2(g)+H2(g) △H=-41.2kJ/mol
CO2(g)+H2(g) △H=-41.2kJ/mol则反应CH4(g)+2H2O(g)
 CO2(g)+4H2(g) △H=
CO2(g)+4H2(g) △H=(2)乙醇是酒精饮料的主要成分,由葡萄糖发酵生成,反应的化学方程式为:C6H12O6(aq)→2C2H5OH(aq)+2CO2(g),当C6H12O6减少的速率为0.23mol•L-1•h-1时,C2H5OH增加的速率是
(3)1mol CH4(l)完全燃烧生成CO2(g)与H2O(1),放出热量889.6kJ,写出反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】作为一种绿色消毒剂,H2O2 在公共卫生事业中发挥了重要的作用。已知反应:H2O2(l)= H2O(1)+  O2(g) ΔH= -98 kJ·mol-1 K= 2.88×1020
O2(g) ΔH= -98 kJ·mol-1 K= 2.88×1020
回答问题:
向H2O2稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起_________ 作用。某组实验数据如下:
0-30 min H2O2反应的平均速率v=_____ mol ·L·min-1
 O2(g) ΔH= -98 kJ·mol-1 K= 2.88×1020
O2(g) ΔH= -98 kJ·mol-1 K= 2.88×1020回答问题:
向H2O2稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
c(H2O2)/mol ·L-1 | 0.70 | 0.49 | 0.35 | 0.25 | 0.17 | 0.12 |
0-30 min H2O2反应的平均速率v=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。

请回答下列问题:
(1)在“图1”中,曲线____ 填“a”或“b”)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应CO(g)+2H2(g) CH3OH(g)的△H=
CH3OH(g)的△H= _________________________ 。
(2)下列说法正确的是( )
A.起始充入的CO的物质的量为1mol
B.增加CO的浓度,H2的转化率会增大
C.容器中压强恒定时,反应达到平衡状态
(3)从反应开始到建立平衡,υ(CO)=_______ ;达到平衡时,c(H2)= ____ ,该温度下CO(g)+2H2(g)  CH3OH(g)的化学平衡常数为
CH3OH(g)的化学平衡常数为______________ 。达到平衡后若保持其它条件不变,将容器体积压缩为0.5L,则平衡___________ 移动 (填“正向”、“逆向”或“不”)。
 CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
请回答下列问题:
(1)在“图1”中,曲线
 CH3OH(g)的△H=
CH3OH(g)的△H= (2)下列说法正确的是
A.起始充入的CO的物质的量为1mol
B.增加CO的浓度,H2的转化率会增大
C.容器中压强恒定时,反应达到平衡状态
(3)从反应开始到建立平衡,υ(CO)=
 CH3OH(g)的化学平衡常数为
CH3OH(g)的化学平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】中国科学家用金属钠和 在一定条件下制得了金刚石:
在一定条件下制得了金刚石: (金刚石)
(金刚石)
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式____ ,若 ,则
,则________ (选填序号)。
a.反应肯定达到平衡 b.反应可能达到平衡 c.反应肯定未达平衡
(2)若反应在10L密闭容器、常压下进行,5min内,测得金刚石的质量增加了6g,该时间段内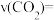
________ ,若反应温度由890℃升高到1860℃,则容器内气体的平均相对分子质量将________ (选填“增大”、“减小”或“不变”)。
(3)反应中还有石墨生成,已知: ,若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是
,若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是________ 反应(填“吸热”或“放热”)。
 在一定条件下制得了金刚石:
在一定条件下制得了金刚石: (金刚石)
(金刚石)| 钠 |  | 金刚石 | 石墨 | |
| 熔点(℃) | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 882.9 | 1850(分解产生 ) ) | —— | 4250 |
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式
 ,则
,则a.反应肯定达到平衡 b.反应可能达到平衡 c.反应肯定未达平衡
(2)若反应在10L密闭容器、常压下进行,5min内,测得金刚石的质量增加了6g,该时间段内
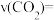
(3)反应中还有石墨生成,已知:
 ,若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是
,若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】二氧化碳催化加氢合成乙烯是综合利用 CO2 的热点研究领域。回答下列问题:
(1)CO2 催化加氢生成C2H4和水的反应中,产物的物质的量之比n(C2H4):n(H2O)=_______ 。当反应达到平衡时,若增大压强,则 n(C2H4) _______ (填 “变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成 n(CO2):n(H2)=1:3,在体系压强为 0.1 MPa,反应达到平衡时,四种组分的物质的量分数 x 随温度 T 的变化如图所示:

图中,表示 C2H4、CO2 变化的曲线分别是_______ 、_______ 。 CO2 催化加氢合成 C2H4 反应的△H _______ 0 (填“大于” 或“小于”)。
(3)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成 C3H6、C3H8、C4H8 等低碳烃。若在 一定温度和压强条件下,要提高反应速率和乙烯选择性,应当使用合适的_______ 等,此时,活化能会_______ ,单位体积内活化分子百分数_______ ,单位体积内有效碰撞次数_______ 。
(1)CO2 催化加氢生成C2H4和水的反应中,产物的物质的量之比n(C2H4):n(H2O)=
(2)理论计算表明,原料初始组成 n(CO2):n(H2)=1:3,在体系压强为 0.1 MPa,反应达到平衡时,四种组分的物质的量分数 x 随温度 T 的变化如图所示:

图中,表示 C2H4、CO2 变化的曲线分别是
(3)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成 C3H6、C3H8、C4H8 等低碳烃。若在 一定温度和压强条件下,要提高反应速率和乙烯选择性,应当使用合适的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:
 ,其化学平衡常数K与温度T的关系如表所示:
,其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
(1)写出化学平衡常数K的表达式___________ 。
(2)试比较 、
、 的大小,
的大小,
___________  (填“>”“<”或“=”);
(填“>”“<”或“=”);
(3)400℃时,反应 的化学平衡常数为
的化学平衡常数为___________ ,当测得 、
、 和
和 物质的量分别为3mol、2mol和1mol时,则该反应的
物质的量分别为3mol、2mol和1mol时,则该反应的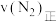
___________ 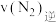 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)根据化学反应速率和化学平衡理论,联系合成氨的生产实际,你认为下列说法不正确的是___________。

 ,其化学平衡常数K与温度T的关系如表所示:
,其化学平衡常数K与温度T的关系如表所示:| T/℃ | 200 | 300 | 400 |
| K |  |  | 0.5 |
(1)写出化学平衡常数K的表达式
(2)试比较
 、
、 的大小,
的大小,
 (填“>”“<”或“=”);
(填“>”“<”或“=”);(3)400℃时,反应
 的化学平衡常数为
的化学平衡常数为 、
、 和
和 物质的量分别为3mol、2mol和1mol时,则该反应的
物质的量分别为3mol、2mol和1mol时,则该反应的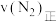
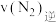 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)根据化学反应速率和化学平衡理论,联系合成氨的生产实际,你认为下列说法不正确的是___________。
| A.化学反应速率理论可指导怎样在一定时间内快出产品 |
| B.勒夏特列原理可指导怎样使用有限原料多出产品 |
| C.催化剂的使用是提高产品产率的有效方法 |
| D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】反应M(l)+N(l) E(l)+F(l)分别在相同压强和348K、343K、338K条件下进行,起始时均按M与N的物质的量比1:1投料,测得α(M)随时间t的变化关系如图所示。
E(l)+F(l)分别在相同压强和348K、343K、338K条件下进行,起始时均按M与N的物质的量比1:1投料,测得α(M)随时间t的变化关系如图所示。

已知:v正=k正·x(M)∙x(N),v逆=k逆·x(E)∙x(F),其中v正、v逆分别为正、逆反应的反应速率,k正、k逆分别为正、逆反应的速率常数,x为各组分的物质的量分数。回答下列问题:
(1)348K时,以物质的量分数表示的化学平衡常数Kx=________ (保留2位有效数字)。该温度下,分别按M与N物质的量之比1:1、1:2和2:1进行初始投料,则达到平衡后,初始投料比为________ 时,M的转化率最大;与按1:1投料相比,按2:1投料时化学平衡常数Kx________ 。(填“增大”“减小”或“不变”)。
(2)A、B、C、D四点中,v正最大的是________ 点,v逆最大的是________ 点。
(3)在曲线①、②、③中,正、逆反应的速率常数值k正-k逆最大的曲线是________ 。
 E(l)+F(l)分别在相同压强和348K、343K、338K条件下进行,起始时均按M与N的物质的量比1:1投料,测得α(M)随时间t的变化关系如图所示。
E(l)+F(l)分别在相同压强和348K、343K、338K条件下进行,起始时均按M与N的物质的量比1:1投料,测得α(M)随时间t的变化关系如图所示。
已知:v正=k正·x(M)∙x(N),v逆=k逆·x(E)∙x(F),其中v正、v逆分别为正、逆反应的反应速率,k正、k逆分别为正、逆反应的速率常数,x为各组分的物质的量分数。回答下列问题:
(1)348K时,以物质的量分数表示的化学平衡常数Kx=
(2)A、B、C、D四点中,v正最大的是
(3)在曲线①、②、③中,正、逆反应的速率常数值k正-k逆最大的曲线是
您最近一年使用:0次
【推荐3】反应Fe(s)+CO2(g) FeO(s)+CO(g) △H1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) △H1,平衡常数为K1;反应Fe(s)+H2O(g)  FeO(s)+H2(g) △H2,平衡常数为K2,在不同温度时,K1、K2的值如下表:
FeO(s)+H2(g) △H2,平衡常数为K2,在不同温度时,K1、K2的值如下表:
(1)反应CO2(g)+H2(g) CO(g)+H2O(g) △H, 平衡常数K,则△H=
CO(g)+H2O(g) △H, 平衡常数K,则△H=_____ (用△H1和△H2表示),K=______ (用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g) CO(g)+ H2O(g)是
CO(g)+ H2O(g)是_____ 反应(填 “吸热”或“放热")。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+ CO2(g) FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图1所示:
FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图1所示:
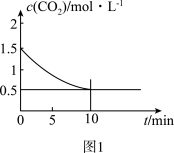
该条件下反应的平衡常数为_____ ;若铁粉足量,CO2的起始浓度为2.0 mol/L,则平衡时CO2的浓度为____ mol/L。
(3)一定温度下,可逆反应CO(g)+2H2(g)= CH3OH(g) △H<0 达到平衡,将容器的容积压缩到原来的 ,在其它条件不变的情况下,对平衡体系产生的影响是
,在其它条件不变的情况下,对平衡体系产生的影响是_______ 。
A.c(H2)减小 B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加 D.重新平衡时 减小
减小
 FeO(s)+CO(g) △H1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) △H1,平衡常数为K1;反应Fe(s)+H2O(g)  FeO(s)+H2(g) △H2,平衡常数为K2,在不同温度时,K1、K2的值如下表:
FeO(s)+H2(g) △H2,平衡常数为K2,在不同温度时,K1、K2的值如下表:| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
 CO(g)+H2O(g) △H, 平衡常数K,则△H=
CO(g)+H2O(g) △H, 平衡常数K,则△H= CO(g)+ H2O(g)是
CO(g)+ H2O(g)是(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+ CO2(g)
 FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图1所示:
FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图1所示:
该条件下反应的平衡常数为
(3)一定温度下,可逆反应CO(g)+2H2(g)= CH3OH(g) △H<0 达到平衡,将容器的容积压缩到原来的
 ,在其它条件不变的情况下,对平衡体系产生的影响是
,在其它条件不变的情况下,对平衡体系产生的影响是A.c(H2)减小 B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加 D.重新平衡时
 减小
减小
您最近一年使用:0次



