锂离子电池的应用很广泛,某种锂电池的正极材料为钴酸锂,该材料可以由海水(含较大浓度的LiCI及少量MgCl2、CaCl2、MnCl2等)为原料制备,其工艺流程如图所示:
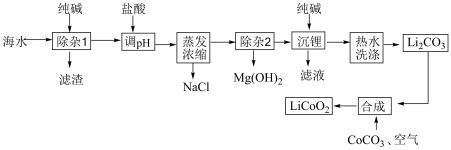
已知:①在常温下几种难溶物质的溶度积常数如表
②Li2CO3微溶于热水,可溶于冷水。回答下列问题:
(1)“除杂1”步骤中除去的杂质离子为Mg2+和_____ 。
(2)“调pH”的目的是_____ 。
(3)金属镁可以通过电解熔融MgC12得到,写出由Mg(OH)2沉淀制MgCl2固体的具体操作_____ 。
(4)20℃时碳酸锂在水中的溶解度为1.295g,饱和溶液密度为1.0148g/cm3,其中Li2CO3的物质的量浓度为_____ 。(结果保留2位有效数字)
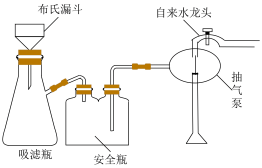
(5)“热水洗涤”的目的是_____ 。在实验室里洗涤Li2CO3时会采用如图所示装置,该装置较于普通过滤装置的优点为_____ 。
(6)“合成”工序需要高温条件,并放出能使澄清石灰水变浑浊的气体,写出该反应的化学方程式_____ 。

已知:①在常温下几种难溶物质的溶度积常数如表
| 物质 | Li2CO3 | MgCO3 | CaCO3 | MnCO3 | Mg(OH)2 |
| K | 2.5×10-2 | 6.8×10-6 | 3.4×10-9 | 2.3×10-11 | 5.6×10-12 |
(1)“除杂1”步骤中除去的杂质离子为Mg2+和
(2)“调pH”的目的是
(3)金属镁可以通过电解熔融MgC12得到,写出由Mg(OH)2沉淀制MgCl2固体的具体操作
(4)20℃时碳酸锂在水中的溶解度为1.295g,饱和溶液密度为1.0148g/cm3,其中Li2CO3的物质的量浓度为
(5)“热水洗涤”的目的是

(6)“合成”工序需要高温条件,并放出能使澄清石灰水变浑浊的气体,写出该反应的化学方程式
更新时间:2023-09-22 18:21:10
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
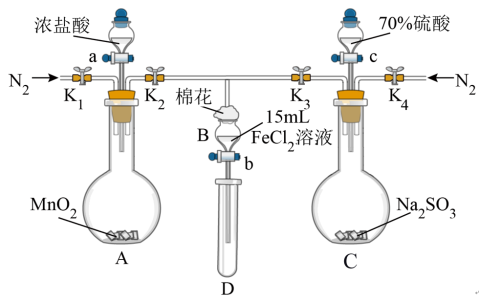
【推荐1】为验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是__________________________ 。
(2)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是__________________________ 。
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式__________________________ 。
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为__________________________ 。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示.他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是_____ (填“甲”、“乙”或“丙”)。
(6)将B中的FeCl2溶液换成100mLFeBr2溶液并向其中通入2.24LCl2(标准状况下),若溶液中有1/2的Br﹣被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为____ 。

实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是
(2)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示.他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有Fe2+ |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42﹣ |
| 丙 | 有Fe3+无Fe2+ | 有SO42﹣ |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】Ⅰ.完成下列问题
(1)市售浓盐酸的密度为1.180 g/mL,物质的量浓度为 11.64 mol/L,此浓盐酸的质量分数为_______ ;若将100g此盐酸加水稀释至5.82mol/L,则加入水的质量_______ 100g。(填“大于”、“等于”或“小于”);
Ⅱ.某同学在实验室中用此浓盐酸与MnO2为原料制取纯净干燥的Cl2,装置如下图:
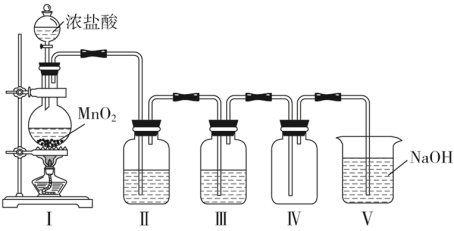
(2)装置Ⅰ中盛装浓盐酸的仪器名称为_______ ;圆底烧瓶中发生反应的离子方程式为_______ ;此反应中HCl体现出性质有_______ 和 _______ 。若生成标准状况下22.4L Cl2,被氧化的HCl分子数是_______ 。
(3)Ⅱ和Ⅲ中盛装的试剂分别是_______ 和_______ 。
(4)氯气的水溶液为氯水,Cl2与H2O反应的离子方程式为_______ ;
(5)如图是数字化实验得到的光照过程中氯水的pH变化情况。对此,下列有关说法正确的是_______
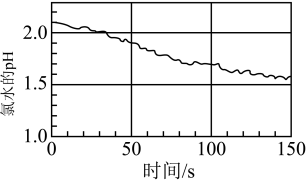
(6)装置Ⅴ中NaOH溶液的作用是吸收尾气,其中发生反应的化学方程式为 _______ 。
(1)市售浓盐酸的密度为1.180 g/mL,物质的量浓度为 11.64 mol/L,此浓盐酸的质量分数为
Ⅱ.某同学在实验室中用此浓盐酸与MnO2为原料制取纯净干燥的Cl2,装置如下图:

(2)装置Ⅰ中盛装浓盐酸的仪器名称为
(3)Ⅱ和Ⅲ中盛装的试剂分别是
(4)氯气的水溶液为氯水,Cl2与H2O反应的离子方程式为
(5)如图是数字化实验得到的光照过程中氯水的pH变化情况。对此,下列有关说法正确的是_______

| A.光照使氯水中的次氯酸分解为盐酸,溶液的酸性增强 |
| B.随着对氯水光照时间的延长,氯水的漂白性将增强 |
| C.随着对氯水光照时间的延长,溶液中Cl-的浓度不断减小 |
| D.随着对氯水光照时间的延长,氯水颜色逐渐变浅 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下。

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(l)实验室用18.4mol/L的浓硫酸配制225mL4.8mol/L的H2SO4溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要__________________ 。
(2)酸浸时,为了提高浸取率除了增大酸的浓度外还可采取的措施有______ (答出一点即可)。
(3)H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式______ 。
(4)常温下,部分阳离子以氮氧化物形式沉淀时,溶液的pH如下:
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-溶液的pH不能超过8,其理由_______ 。
(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液Ⅱ中的金属阳离子是____________ 。
(6)写出上述流程中用Na2SO3进行还原时发生反应的化学方程式_______ ,在实验室进行过滤操作时,为了加快过滤速率,可以采取的措施为_________ (写一种方法即可).

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(l)实验室用18.4mol/L的浓硫酸配制225mL4.8mol/L的H2SO4溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要
(2)酸浸时,为了提高浸取率除了增大酸的浓度外还可采取的措施有
(3)H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式
(4)常温下,部分阳离子以氮氧化物形式沉淀时,溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ |
| 开始沉淀时的pH | 2.7 | — | — |
| 沉淀完全时的pH | 3.7 | 11.1 | 8 |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-溶液的pH不能超过8,其理由
(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液Ⅱ中的金属阳离子是
(6)写出上述流程中用Na2SO3进行还原时发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】某科学研究小组设计以辉钼矿(MoS2、CuFeS2、Cu2S及SiO2等)为原料制备少量钼酸铵的工艺流程如下:

已知:①“焙砂”中有MoO3、CuSO4、CuMoO4、Fe2O3、Fe2(SO4)3、SiO2。
②“氨浸”时,铜元素转化为[Cu(NH3)4](OH)2(深蓝色),钼元素转化为(NH4)2MoO4。
③[Cu(NH3)4](OH)2=[Cu(NH3)4]2++2OH—。
回答下列问题:
(1)为了使辉钼矿充分焙烧,需要采取的措施是_______ (写出一种)。
(2)焙烧过程中MoS2转化成MoO3的化学方程式为_______ 。
(3)反应CuFeS2+O2=CuSO4+Fe2O3+Fe2(SO4)3(未配平)氧化剂与还原剂物质的量比为_______
(4)“氨浸”时发生多个反应,其中CuMoO4被浸取的化学方程式为_______ 。
(5)“滤渣1”的成分有SiO2、_______ (填化学式)。
(6)“沉铜”是在80℃时进行的,发生反应的离子方程式为_______
(7)已知a克辉钼矿中含铜质量分数为8%,若“沉铜”工序得到b克沉淀物,则沉铜率为_______ (用含a、b的代数式表示)。

已知:①“焙砂”中有MoO3、CuSO4、CuMoO4、Fe2O3、Fe2(SO4)3、SiO2。
②“氨浸”时,铜元素转化为[Cu(NH3)4](OH)2(深蓝色),钼元素转化为(NH4)2MoO4。
③[Cu(NH3)4](OH)2=[Cu(NH3)4]2++2OH—。
回答下列问题:
(1)为了使辉钼矿充分焙烧,需要采取的措施是
(2)焙烧过程中MoS2转化成MoO3的化学方程式为
(3)反应CuFeS2+O2=CuSO4+Fe2O3+Fe2(SO4)3(未配平)氧化剂与还原剂物质的量比为
(4)“氨浸”时发生多个反应,其中CuMoO4被浸取的化学方程式为
(5)“滤渣1”的成分有SiO2、
(6)“沉铜”是在80℃时进行的,发生反应的离子方程式为
(7)已知a克辉钼矿中含铜质量分数为8%,若“沉铜”工序得到b克沉淀物,则沉铜率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】铟(In)是一种稀散金属,常与其他金属矿石伴生,回收氧化锌烟尘(主要成分是ZnO,还含少量PbO、FeS、FeSiO3、 In2O3、 In2S3等)中的金属铟的工艺流程如下:
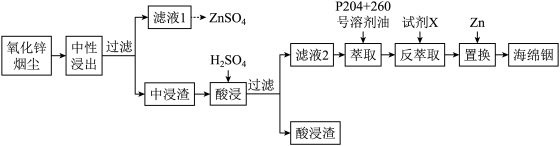
已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
回答下列问题:
(1)In2O3中In的化合价是_______________________ 。
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为____________________________________________ 。
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为 ,该反应的离子方程式为
,该反应的离子方程式为____________________ 。
③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为_________________ 。
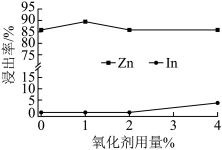
④“中浸渣”的主要成分为In(OH)3、________________ 。 (写化学式)
(3)萃取时,发生反应In3+ +3H2A2 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。
①反萃取时,宜选用的试剂X为_____________________ (写化学式)
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有_________________________ 。
(4)“置换”后的滤液可返回________________________ (填“滤液 1”或“滤液2”)中利用。
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉___ _kg (结果保留1位小数)

已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
金属离子 | Fe3+ | Fe2+ | In3+ |
开始沉淀pH(离子浓度为0.1mol·L-1时) | 1.3 | 6 | 3 |
完全沉淀pH | 2.7 | 8 | 4.3 |
(1)In2O3中In的化合价是
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为
 ,该反应的离子方程式为
,该反应的离子方程式为③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为

④“中浸渣”的主要成分为In(OH)3、
(3)萃取时,发生反应In3+ +3H2A2
 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。①反萃取时,宜选用的试剂X为
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有
(4)“置换”后的滤液可返回
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4•7H2O的流程如图:
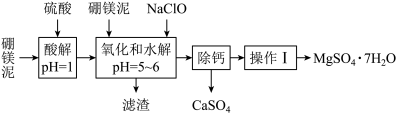
根据题意回答下列问题:
(1)实验中需用1.0mol•L-1的硫酸240mL,若用18.4mol•L-1的浓硫酸来配制,所需的仪器除了烧杯、量筒、玻璃棒,还需的玻璃仪器是_____ 。
(2)加入的NaClO可与Mn2+反应:Mn2++ClO—+H2O=MnO2↓+2H++Cl—,还有一种阳离子也会被NaClO氧化,该反应的离子方程式为_____ 。
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外,还有_____ 。
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:_____ 。
(5)已知MgSO4、CaSO4的溶解度如表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据表中数据,简要说明操作步骤:_____ 。“操作1”是将滤液继续_____ 、过滤、洗涤,便得到了MgSO4•7H2O。
(6)实验中提供的硼镁泥共10g,得到的MgSO4•7H2O为17.22g,则MgSO4•7H2O的产率为_____ 。

根据题意回答下列问题:
(1)实验中需用1.0mol•L-1的硫酸240mL,若用18.4mol•L-1的浓硫酸来配制,所需的仪器除了烧杯、量筒、玻璃棒,还需的玻璃仪器是
(2)加入的NaClO可与Mn2+反应:Mn2++ClO—+H2O=MnO2↓+2H++Cl—,还有一种阳离子也会被NaClO氧化,该反应的离子方程式为
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外,还有
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:
(5)已知MgSO4、CaSO4的溶解度如表:
| 温度/℃ | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(6)实验中提供的硼镁泥共10g,得到的MgSO4•7H2O为17.22g,则MgSO4•7H2O的产率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】以菱镁矿 主要成分为
主要成分为 ,含少量
,含少量
 为原料制备高纯氧化镁的实验流程如下:
为原料制备高纯氧化镁的实验流程如下:

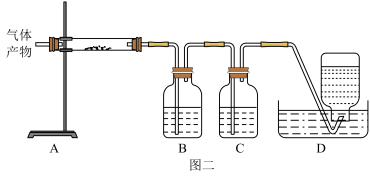
 滤液P中含有的阳离子有
滤液P中含有的阳离子有 ______ 。
 过程Ⅱ中发生的氧化还原反应的离子方程式是
过程Ⅱ中发生的氧化还原反应的离子方程式是 ______ 。
 已知:
已知:
过程Ⅲ中加入 调节溶液pH约为4,其目的是
调节溶液pH约为4,其目的是 ______ 。
 过程Ⅳ在
过程Ⅳ在 煅烧
煅烧 ,发生多个反应,产物除MgO外,还有
,发生多个反应,产物除MgO外,还有 、
、 、CO、S等气体产物,利用右图装置判断煅烧产生的气体。
、CO、S等气体产物,利用右图装置判断煅烧产生的气体。
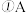 中试管壁附着有淡黄色固体,该固体的化学式是
中试管壁附着有淡黄色固体,该固体的化学式是 ______ 。
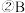 中盛放的溶液是
中盛放的溶液是 填字母
填字母
______ 。
 溶液
溶液  溶液
溶液  稀硝酸
稀硝酸  溶液
溶液
 写出
写出 煅烧
煅烧 ,产生气体产物是S 和CO的化学方程式
,产生气体产物是S 和CO的化学方程式 ______ 。
 主要成分为
主要成分为 ,含少量
,含少量
 为原料制备高纯氧化镁的实验流程如下:
为原料制备高纯氧化镁的实验流程如下: 

 滤液P中含有的阳离子有
滤液P中含有的阳离子有  过程Ⅱ中发生的氧化还原反应的离子方程式是
过程Ⅱ中发生的氧化还原反应的离子方程式是  已知:
已知:  |  |  | |
| 开始沉淀的pH |  | 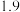 | 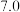 |
| 沉淀完全的pH | 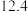 |  |  |
过程Ⅲ中加入
 调节溶液pH约为4,其目的是
调节溶液pH约为4,其目的是  过程Ⅳ在
过程Ⅳ在 煅烧
煅烧 ,发生多个反应,产物除MgO外,还有
,发生多个反应,产物除MgO外,还有 、
、 、CO、S等气体产物,利用右图装置判断煅烧产生的气体。
、CO、S等气体产物,利用右图装置判断煅烧产生的气体。 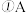 中试管壁附着有淡黄色固体,该固体的化学式是
中试管壁附着有淡黄色固体,该固体的化学式是 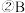 中盛放的溶液是
中盛放的溶液是 填字母
填字母
 溶液
溶液  溶液
溶液  稀硝酸
稀硝酸  溶液
溶液  写出
写出 煅烧
煅烧 ,产生气体产物是S 和CO的化学方程式
,产生气体产物是S 和CO的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】某工厂采用如下工艺处理镍钴矿硫酸浸取液(含 、
、 、
、 、
、 、
、 和
和 ),实现镍、钴、镁元素的回收。
),实现镍、钴、镁元素的回收。
(1)工业上用一定浓度的硫酸浸取已粉碎的镍钴矿并不断搅拌,提高浸取速率的方法为____________ (答出一条即可)。
(2)“氧化”时,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸( ),其中
),其中 元素的化合价为
元素的化合价为______ 。
(3)已知: 的电离方程式为
的电离方程式为 、
、
①“氧化”时,先通入足量混合气,溶液中的正二价铁元素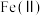 被
被 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为______ ;再加入石灰乳,所得滤渣中主要成分是 、
、______ 。
②通入混合气中 的体积分数与
的体积分数与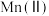 氧化率随时间的变化关系如图所示,若混合气中不添加
氧化率随时间的变化关系如图所示,若混合气中不添加 ,相同时间内
,相同时间内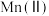 氧化率较低的原因是
氧化率较低的原因是____________ ; 的体积分数高于9.0%时,相同时间内
的体积分数高于9.0%时,相同时间内 氧化率开始降低的原因是
氧化率开始降低的原因是____________ 。 溶液进行“钴镍分离”,写出“钴镍分离”反应生成
溶液进行“钴镍分离”,写出“钴镍分离”反应生成
 沉淀的离子方程式:
沉淀的离子方程式:______ 。
②若“镍钴分离”后溶液中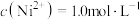 ,加入
,加入 溶液“沉镍”后的滤液中
溶液“沉镍”后的滤液中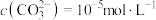 ,则沉镍率=
,则沉镍率=______ 。[已知: ,沉镍率=
,沉镍率=
 、
、 、
、 、
、 、
、 和
和 ),实现镍、钴、镁元素的回收。
),实现镍、钴、镁元素的回收。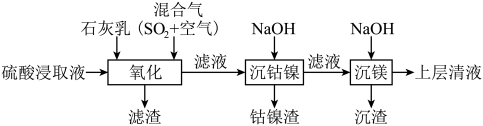
(1)工业上用一定浓度的硫酸浸取已粉碎的镍钴矿并不断搅拌,提高浸取速率的方法为
(2)“氧化”时,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(
 ),其中
),其中 元素的化合价为
元素的化合价为(3)已知:
 的电离方程式为
的电离方程式为 、
、
①“氧化”时,先通入足量混合气,溶液中的正二价铁元素
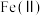 被
被 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为 、
、②通入混合气中
 的体积分数与
的体积分数与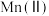 氧化率随时间的变化关系如图所示,若混合气中不添加
氧化率随时间的变化关系如图所示,若混合气中不添加 ,相同时间内
,相同时间内 氧化率较低的原因是
氧化率较低的原因是 的体积分数高于9.0%时,相同时间内
的体积分数高于9.0%时,相同时间内 氧化率开始降低的原因是
氧化率开始降低的原因是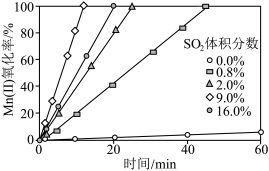
 溶液进行“钴镍分离”,写出“钴镍分离”反应生成
溶液进行“钴镍分离”,写出“钴镍分离”反应生成 沉淀的离子方程式:
沉淀的离子方程式:②若“镍钴分离”后溶液中
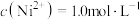 ,加入
,加入 溶液“沉镍”后的滤液中
溶液“沉镍”后的滤液中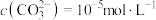 ,则沉镍率=
,则沉镍率= ,沉镍率=
,沉镍率=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】食品级焦亚硫酸钠( )常用作饼干和蛋糕的漂白剂和膨化剂,在空气中易被氧化,受热易分解。实验室制备少量
)常用作饼干和蛋糕的漂白剂和膨化剂,在空气中易被氧化,受热易分解。实验室制备少量 的实验流程如下:
的实验流程如下:

回答下列问题:
(1)步骤I制取并收集干燥的 ,所用装置如图所示:
,所用装置如图所示:

①按气流方向连接各仪器口,顺序为a___________ (填标号)。
②装置C的作用是___________ ,装置E中试剂是______________________ 。
(2)步骤II发生反应的化学方程式为______________________ ;该步骤加热时采取的方式为___________ 。
(3)操作III:低温蒸发、___________ 、洗涤;其中洗涤 时依次用饱和
时依次用饱和 水溶液、无水乙醇。饱和
水溶液、无水乙醇。饱和 水溶液洗涤的目的是
水溶液洗涤的目的是_________________________________ 。
(4)实验制得的 固体中含有少量
固体中含有少量 杂质,其可能的原因是
杂质,其可能的原因是______________________ 。
(5) 纯度测定:取
纯度测定:取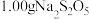 样品溶于水配成
样品溶于水配成 溶液,取
溶液,取 该溶液,用
该溶液,用 的碘标准溶液滴定至终点,消耗
的碘标准溶液滴定至终点,消耗 标准溶液。样品中
标准溶液。样品中 的质量分数为
的质量分数为___________ (假设其他杂质不反应,滴定过程中发生反应的离子方程式为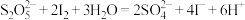 )。
)。
 )常用作饼干和蛋糕的漂白剂和膨化剂,在空气中易被氧化,受热易分解。实验室制备少量
)常用作饼干和蛋糕的漂白剂和膨化剂,在空气中易被氧化,受热易分解。实验室制备少量 的实验流程如下:
的实验流程如下:
回答下列问题:
(1)步骤I制取并收集干燥的
 ,所用装置如图所示:
,所用装置如图所示:
①按气流方向连接各仪器口,顺序为a
②装置C的作用是
(2)步骤II发生反应的化学方程式为
(3)操作III:低温蒸发、
 时依次用饱和
时依次用饱和 水溶液、无水乙醇。饱和
水溶液、无水乙醇。饱和 水溶液洗涤的目的是
水溶液洗涤的目的是(4)实验制得的
 固体中含有少量
固体中含有少量 杂质,其可能的原因是
杂质,其可能的原因是(5)
 纯度测定:取
纯度测定:取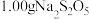 样品溶于水配成
样品溶于水配成 溶液,取
溶液,取 该溶液,用
该溶液,用 的碘标准溶液滴定至终点,消耗
的碘标准溶液滴定至终点,消耗 标准溶液。样品中
标准溶液。样品中 的质量分数为
的质量分数为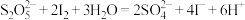 )。
)。
您最近一年使用:0次
【推荐1】分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图所示:
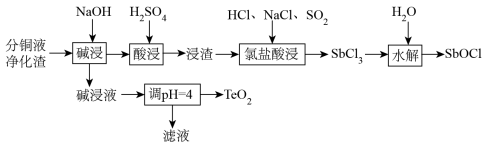
已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有 、
、 。
。
②“酸浸”时,锑元素反应生成难溶的 浸渣。
浸渣。
回答下列问题:
(1)As位于第四周期VA族,基态As的价层电子排布式为___________ 。
(2)“碱浸”时, 与NaOH反应的离子方程式为
与NaOH反应的离子方程式为___________ 。
(3)向碱浸液加入盐酸调节pH=4,有 析出,分离出
析出,分离出 的操作是
的操作是___________ 。滤液中As元素最主要的存在形式为___________ (常温下, 的各级电离常数为:
的各级电离常数为: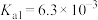 、
、 、
、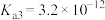 )。
)。
A. B.
B.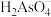 C.
C. D.
D.
(4)① 中,Sb的化合价为
中,Sb的化合价为___________ 。
②“氯盐酸浸”时,通入 的目的是
的目的是___________ 。
(5)“水解”时,生成SbOCl的化学方程式为___________ 。
(6) 可用作电子元件材料,熔点为733℃,其熔点远高于
可用作电子元件材料,熔点为733℃,其熔点远高于 的原因为
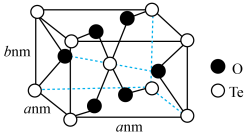
的原因为___________ 。 晶胞是长方体结构(如图所示),碲的配位数为
晶胞是长方体结构(如图所示),碲的配位数为___________ 。已知 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________  (列出计算表达式)
(列出计算表达式)

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有
 、
、 。
。②“酸浸”时,锑元素反应生成难溶的
 浸渣。
浸渣。回答下列问题:
(1)As位于第四周期VA族,基态As的价层电子排布式为
(2)“碱浸”时,
 与NaOH反应的离子方程式为
与NaOH反应的离子方程式为(3)向碱浸液加入盐酸调节pH=4,有
 析出,分离出
析出,分离出 的操作是
的操作是 的各级电离常数为:
的各级电离常数为: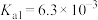 、
、 、
、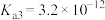 )。
)。A.
 B.
B.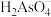 C.
C. D.
D.
(4)①
 中,Sb的化合价为
中,Sb的化合价为②“氯盐酸浸”时,通入
 的目的是
的目的是(5)“水解”时,生成SbOCl的化学方程式为
(6)
 可用作电子元件材料,熔点为733℃,其熔点远高于
可用作电子元件材料,熔点为733℃,其熔点远高于 的原因为
的原因为 晶胞是长方体结构(如图所示),碲的配位数为
晶胞是长方体结构(如图所示),碲的配位数为 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 (列出计算表达式)
(列出计算表达式)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
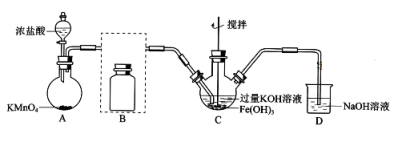
①A为氯气发生装置。A中反应方程式是___________ (锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。___________
③C中得到紫色固体和溶液。写出生成K2FeO4的离子方程式___________
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。
证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
i.由方案I中溶液变红可知a中含有___________ 离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由___________ 产生(用方程式表示)。
ii.方案II可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是___________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2___________ FeO (填“>”或“<”),而方案II实验表明,Cl2和FeO
(填“>”或“<”),而方案II实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
③资料表明,酸性溶液中的氧化性FeO >MnO
>MnO ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO >MnO
>MnO 。若能,请说明理由:若不能,进一步设计实验方案。理由或方案:
。若能,请说明理由:若不能,进一步设计实验方案。理由或方案:___________ 。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。A中反应方程式是
②将除杂装置B补充完整并标明所用试剂。
③C中得到紫色固体和溶液。写出生成K2FeO4的离子方程式
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。
证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案I | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案II | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。 |
ii.方案II可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案II实验表明,Cl2和FeO
(填“>”或“<”),而方案II实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是③资料表明,酸性溶液中的氧化性FeO
 >MnO
>MnO ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO >MnO
>MnO 。若能,请说明理由:若不能,进一步设计实验方案。理由或方案:
。若能,请说明理由:若不能,进一步设计实验方案。理由或方案:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】磷酸铝(AlPO4)是一种用途广泛的材料,可在玻璃生产过程中充当助熔剂,作陶瓷或牙齿的黏合剂等。以磷硅渣[主要成分为Ca3(PO4)2、Al2O3、SiO2和V2O5等]为原料制备磷酸铝的工艺流程如图所示:

请回答下列问题:
(1)浸渣中含有SiO2,试写出SiO2的一种重要用途__ ;酸浸中磷元素主要转化为H3PO4,该反应的化学方程式为__ 。
(2)生石灰除了调节pH外,另一作用是__ 。
(3)滤液中钒元素以V3O93-形式存在,V3O93-易水解为[VO3(OH)]2-,该水解反应的离子方程式为__ 。
(4)碱浸时,粗磷酸铝转化为可溶性溶质,则可溶性溶质分别是__ (填化学式)。
(5)实验测得pH、反应温度与时间对碱浸时固相中P、Al含量w%的影响如图所示:


则最优反应条件是__ 。
(6)在物质的量浓度分别为0.01mol·L-1的CaCl2和AlCl3的混合溶液中加入等体积的Na3PO4溶液,若A13+恰好沉淀完全,即溶液中c(A13+)=1.0×10-5mol·L-1,此时AlPO4沉淀中__ (填“是”或“否”)混有Ca3(PO4)2。[已知AlPO4、Ca3(PO4)2的Ksp分别为6.3×10-19、2.0×10-29]

请回答下列问题:
(1)浸渣中含有SiO2,试写出SiO2的一种重要用途
(2)生石灰除了调节pH外,另一作用是
(3)滤液中钒元素以V3O93-形式存在,V3O93-易水解为[VO3(OH)]2-,该水解反应的离子方程式为
(4)碱浸时,粗磷酸铝转化为可溶性溶质,则可溶性溶质分别是
(5)实验测得pH、反应温度与时间对碱浸时固相中P、Al含量w%的影响如图所示:


则最优反应条件是
(6)在物质的量浓度分别为0.01mol·L-1的CaCl2和AlCl3的混合溶液中加入等体积的Na3PO4溶液,若A13+恰好沉淀完全,即溶液中c(A13+)=1.0×10-5mol·L-1,此时AlPO4沉淀中
您最近一年使用:0次



