主族元素A、B、C、D、E、F、G、H在元素周期表中的相对位置如图所示。已知上述8种元素的原子最外层电子数之和等于47,C与H的质子数之和为43.请回答下列问题:
(1)G在元素周期表中位于第_____ 周期第_____ 族。
(2)在C、D、G的最简单氢化物中,最不稳定的是_____ (填化学式),常温下,B的最简单氢化物的水溶液的pH_____ (填“>”、“<”或“=”)7.
(3)单质A_____ (填“能”或“不能”)与B的最高价氧化物对应的水化物的浓溶液发生反应。
(4)E的简单氢化物通入胆矾溶液中,产物含红色单质和两种最高价含氧酸,该反应的离子方程式为_____ 。
(5)3molF单质通入热KOH溶液中完全反应,共转移5mol电子。在该反应中,氧化剂与还原剂的质量之比为_____ 。
(6)一定条件下,AC、BC和熔盐(能传导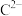 )能形成原电池(产物为无污染气体),其中负极通入的是
)能形成原电池(产物为无污染气体),其中负极通入的是_____ (填化学式),正极的电极反应为_____ 。
| A | B | C | D |
| E | F | ||
| G | H |
(2)在C、D、G的最简单氢化物中,最不稳定的是
(3)单质A
(4)E的简单氢化物通入胆矾溶液中,产物含红色单质和两种最高价含氧酸,该反应的离子方程式为
(5)3molF单质通入热KOH溶液中完全反应,共转移5mol电子。在该反应中,氧化剂与还原剂的质量之比为
(6)一定条件下,AC、BC和熔盐(能传导
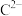 )能形成原电池(产物为无污染气体),其中负极通入的是
)能形成原电池(产物为无污染气体),其中负极通入的是
更新时间:2023-09-27 22:02:58
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末,常用作有机反应的催化剂。实验室制备CuBr的实验步骤和装置如图。

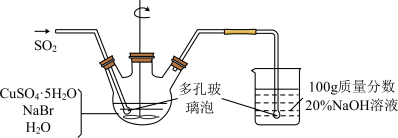
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去蒸馏水中的_______ (写化学式); 三颈烧瓶中反应生成CuBr的离子方程式为_______ ;控制反应在60℃进行,实验中可采取的措施是 _______ ;说明反应已完成的现象是 _______ 。
(2)步骤②抽滤需要避光的原因是_______ ,步骤③依次用溶有少量SO2的水、溶有少量SO2的乙醇、极易挥发的乙醚洗涤,洗涤剂需“溶有SO2”的原因是_______ ;最后用乙醚的目的可能是_______ 。
(3)将产品在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,得到产品21.6g。本实验产品的产率是_______ (保留小数点后1位)。
(4)欲利用上述装置烧杯中的吸收液(经检测主要含有Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。完善下列步骤:①在烧杯中继续通入SO2至恰好反应完全;②向烧杯中加入_______ g 20% NaOH;③加入少量维生素C溶液作抗氧化剂;④通过蒸发浓缩、_______ 、过滤、用乙醇洗涤2~3次;⑤置于真空干燥箱中干燥。


(1)实验所用蒸馏水需经煮沸,煮沸目的是除去蒸馏水中的
(2)步骤②抽滤需要避光的原因是
(3)将产品在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,得到产品21.6g。本实验产品的产率是
(4)欲利用上述装置烧杯中的吸收液(经检测主要含有Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。完善下列步骤:①在烧杯中继续通入SO2至恰好反应完全;②向烧杯中加入
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铁是生产和生活中的重要元素。
(1)钢是用量最大、用途最高的合金,它的熔点比纯铁___ (填“高”或“低”)。
(2)若一定量的普通铁粉和水蒸气在高温下反应生成44.8LH2(已换算到标况下),则转移电子的物质的量为____ mol。
(3)现有一瓶溶液,请设计实验检验其中是否含有Fe3+。___
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,该反应的离子方程式为___ 。
(5)聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,含少量碳及二氧化硅)为原料制备的流程如下:
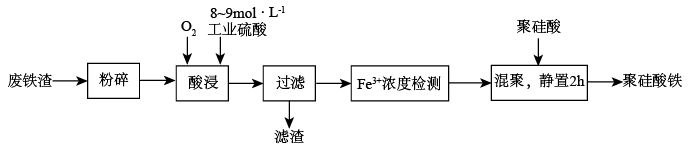
①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为___ 。
②酸浸时,通入O2的目的是___ 。
③“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+;再用酸性K2Cr2O7标准溶液测定Fe2+的量(Cr2O72-被还原为Cr3+),则SnCl2、Fe2+和 Cr3+三者中还原性最强的是___ 。
(1)钢是用量最大、用途最高的合金,它的熔点比纯铁
(2)若一定量的普通铁粉和水蒸气在高温下反应生成44.8LH2(已换算到标况下),则转移电子的物质的量为
(3)现有一瓶溶液,请设计实验检验其中是否含有Fe3+。
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,该反应的离子方程式为
(5)聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,含少量碳及二氧化硅)为原料制备的流程如下:

①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为
②酸浸时,通入O2的目的是
③“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+;再用酸性K2Cr2O7标准溶液测定Fe2+的量(Cr2O72-被还原为Cr3+),则SnCl2、Fe2+和 Cr3+三者中还原性最强的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)CH4既是一种重要的能源,也是一种重要的化工原料。已知8. 0g CH4完全燃烧生成液态水放出445.15kJ热量,则其热化学方程式为_______ 。
(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
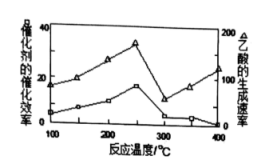
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在_______ 左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuA1O2,难溶物)。将CuA1O2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为_______
③CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下4.48LCH4可处理11.2LNOx,则x值为_______
(1)CH4既是一种重要的能源,也是一种重要的化工原料。已知8. 0g CH4完全燃烧生成液态水放出445.15kJ热量,则其热化学方程式为
(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在

②该反应催化剂的有效成分为偏铝酸亚铜(CuA1O2,难溶物)。将CuA1O2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为
③CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下4.48LCH4可处理11.2LNOx,则x值为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】砷(As)广泛分布于自然界,其原子结构示意图是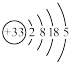
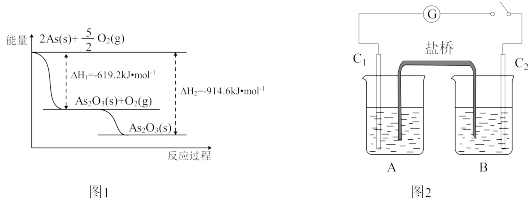
(1)砷位于元素周期表中________ 族,其气态氢化物的稳定性比NH3________ (填“强”或“弱”).
(2)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差.根据图1写出As2O5分解为As2O3的热化学方程式:________
(3)砷酸盐可发生如下反应:AsO +2I﹣+2H+⇌AsO
+2I﹣+2H+⇌AsO +I2+H2O.图2装置中,C1、C2是石墨电极.A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是
+I2+H2O.图2装置中,C1、C2是石墨电极.A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是 ________
(4)利用(3)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样mg溶于NaOH溶液,得到含AsO 和AsO
和AsO 的混合溶液.As2O5与NaOH溶液反应的离子方程式是
的混合溶液.As2O5与NaOH溶液反应的离子方程式是________ .
②上述混合液用0.02500mol•L﹣1的I2溶液滴定,用________ 做指示剂,滴定至________ ,停止滴定,记录数据.重复滴定2次,平均消耗I2溶液20.00mL.则试样中As2O3的质量分数是________
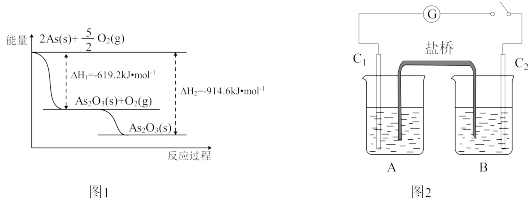
(1)砷位于元素周期表中
(2)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差.根据图1写出As2O5分解为As2O3的热化学方程式:
(3)砷酸盐可发生如下反应:AsO
 +2I﹣+2H+⇌AsO
+2I﹣+2H+⇌AsO +I2+H2O.图2装置中,C1、C2是石墨电极.A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是
+I2+H2O.图2装置中,C1、C2是石墨电极.A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转.此时C2上发生的电极反应是 (4)利用(3)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样mg溶于NaOH溶液,得到含AsO
 和AsO
和AsO 的混合溶液.As2O5与NaOH溶液反应的离子方程式是
的混合溶液.As2O5与NaOH溶液反应的离子方程式是②上述混合液用0.02500mol•L﹣1的I2溶液滴定,用
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氢能是一种极具发展潜力的清洁能源,以下反应是目前大规模制取氢气的重要方法之一

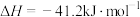
回答下列问题:
(1)欲提高CO的平衡转化率,理论上可以采取的措施为_______ 。
a.通入过量CO b.升高温度 c.加入催化剂 d.通入过量水蒸气
(2)800℃时,该反应的平衡常数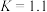 ,在容积为1L的密闭容器中进行反应,测得某一时刻混合物中CO、
,在容积为1L的密闭容器中进行反应,测得某一时刻混合物中CO、 、
、 、
、 的物质的量分别为1mol、3mol、1mol、1mol。
的物质的量分别为1mol、3mol、1mol、1mol。
①写出该反应的平衡常数表达式
_______ 。
②该时刻反应的进行方向为_______ (填“正向进行”、“逆向进行”或“已达平衡”)。
(3)830℃时,该反应的平衡常数 ,在容积为1L的密闭容器中,将2molCO与2mol
,在容积为1L的密闭容器中,将2molCO与2mol 混合加热到830℃。反应达平衡时CO的转化率为
混合加热到830℃。反应达平衡时CO的转化率为_______ 。
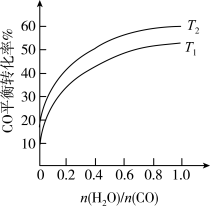
(4)下图表示不同温度条件下,CO平衡转化率随着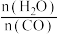 的变化趋势。判断
的变化趋势。判断 、
、 的大小关系:
的大小关系:_______ ,判断理由为_______ 。
(5)以乙醇为燃料的乙醇燃料电池,碱性电解质溶液时,负极反应式为_______ 。

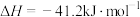
回答下列问题:
(1)欲提高CO的平衡转化率,理论上可以采取的措施为
a.通入过量CO b.升高温度 c.加入催化剂 d.通入过量水蒸气
(2)800℃时,该反应的平衡常数
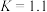 ,在容积为1L的密闭容器中进行反应,测得某一时刻混合物中CO、
,在容积为1L的密闭容器中进行反应,测得某一时刻混合物中CO、 、
、 、
、 的物质的量分别为1mol、3mol、1mol、1mol。
的物质的量分别为1mol、3mol、1mol、1mol。①写出该反应的平衡常数表达式

②该时刻反应的进行方向为
(3)830℃时,该反应的平衡常数
 ,在容积为1L的密闭容器中,将2molCO与2mol
,在容积为1L的密闭容器中,将2molCO与2mol 混合加热到830℃。反应达平衡时CO的转化率为
混合加热到830℃。反应达平衡时CO的转化率为(4)下图表示不同温度条件下,CO平衡转化率随着
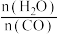 的变化趋势。判断
的变化趋势。判断 、
、 的大小关系:
的大小关系:
(5)以乙醇为燃料的乙醇燃料电池,碱性电解质溶液时,负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2 和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品。
(1)写出氯碱工业中电解饱和食盐水的离子方程式:________ 。
(2)①室温下,0.1 mol·L–1 NaClO溶液的pH___ 0.1 mol·L–1 Na2SO3溶液的pH。(填“大于”、“小于”或“等于”)已知:H2SO3的Ka1=1.54×10–2,Ka2=1.02×10–7;HClO的Ka=2.95×10–8
②写出一种可以证明NaHSO3溶液中HSO3–的电离程度大于HSO3–水解程度的方法:____
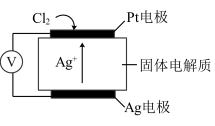
(3)氯气含量检测仪中,原电池工作原理示意图如图所示,则Cl2在Pt电极放电的电极反应为_____
(4)工业上用NaClO3氧化酸性FeCl2废液,通过控制条件,使Fe3+水解产物聚合,形成可溶的多聚体,最终析出红棕色胶状沉淀Fe2O3·nH2O。其中水解形成羟桥配离子的离子方程式为:2Fe3++10H2O [Fe(H2O)4 (OH)2 Fe(H2O)4]4++2H+ 。欲使上述水解平衡正向移动,可采用的方法有
[Fe(H2O)4 (OH)2 Fe(H2O)4]4++2H+ 。欲使上述水解平衡正向移动,可采用的方法有________ (填字母)。
A.加水稀释 B.加热 C.加入盐酸 D.加入NaHCO3
(5)ClO2和Cl2均能将电镀废水中的CN–氧化为无毒的物质,自身被还原为Cl–。处理含CN–相同量的电镀废水,所需Cl2的质量是ClO2的______ 倍。(保留三位有效数字)
(1)写出氯碱工业中电解饱和食盐水的离子方程式:
(2)①室温下,0.1 mol·L–1 NaClO溶液的pH
②写出一种可以证明NaHSO3溶液中HSO3–的电离程度大于HSO3–水解程度的方法:
(3)氯气含量检测仪中,原电池工作原理示意图如图所示,则Cl2在Pt电极放电的电极反应为

(4)工业上用NaClO3氧化酸性FeCl2废液,通过控制条件,使Fe3+水解产物聚合,形成可溶的多聚体,最终析出红棕色胶状沉淀Fe2O3·nH2O。其中水解形成羟桥配离子的离子方程式为:2Fe3++10H2O
 [Fe(H2O)4 (OH)2 Fe(H2O)4]4++2H+ 。欲使上述水解平衡正向移动,可采用的方法有
[Fe(H2O)4 (OH)2 Fe(H2O)4]4++2H+ 。欲使上述水解平衡正向移动,可采用的方法有A.加水稀释 B.加热 C.加入盐酸 D.加入NaHCO3
(5)ClO2和Cl2均能将电镀废水中的CN–氧化为无毒的物质,自身被还原为Cl–。处理含CN–相同量的电镀废水,所需Cl2的质量是ClO2的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.物质X、Y、Z均含同种短周期元素,其转化关系如下图所示(反应条件未标出)。
X Y
Y Z
Z
(1)若X是无色极易溶于水的刺激性气味气体,Z是红棕色气体,由Y与W反应生成Z的化学方程式是_______ 。
(2)若X含三种短周期元素,其中两种元素的原子的质子数之和等于另一种元素原子的质子数,单质W是常见金属,则X的稀溶液转化为Y的离子方程式是_______ 。
(3)若X是空气的主要成分之一,W原子的最外层电子数是内层电子数的二倍;则Y与W反应生成0.1 mol Z时,反应中转移的电子数为_______ 。
Ⅱ.已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系。

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式_______ 。
(2)若A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,反应的离子方程式是_______
(3)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,试写出此反应的化学方程式_______ 。
X
 Y
Y Z
Z(1)若X是无色极易溶于水的刺激性气味气体,Z是红棕色气体,由Y与W反应生成Z的化学方程式是
(2)若X含三种短周期元素,其中两种元素的原子的质子数之和等于另一种元素原子的质子数,单质W是常见金属,则X的稀溶液转化为Y的离子方程式是
(3)若X是空气的主要成分之一,W原子的最外层电子数是内层电子数的二倍;则Y与W反应生成0.1 mol Z时,反应中转移的电子数为
Ⅱ.已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系。

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式
(2)若A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,反应的离子方程式是
(3)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,试写出此反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表列出了5种元素在周期表中的位置。
回答下列问题:
(1)①的元素符号是_______ ,⑤的元素符号是_______
(2)以上元素中,金属性最强的是_______ (填元素符号)。
(3)④元素的最高价氧化物对应的水化物呈_______ 性(填“酸”或“碱”或“两”)。
(4)③④⑤对应元素中原子半径最小的是_______ (填元素符号)。
(5)元素③与元素②形成的化合物,可用于呼吸面具或潜水艇中作为氧气的来源,它的化学式是_______ 。
(6)少量元素③的单质通常保存在_______ 中(填“煤油”或“水”)。
(7)元素①的氢化物与元素②的氢化物更稳定的是_______ (填化学式)。
族 周期 | I A | 0 | ||||||
| 1 | H | Ⅱ A | Ⅲ A | Ⅳ A | V A | Ⅵ A | Ⅶ A | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ |
(1)①的元素符号是
(2)以上元素中,金属性最强的是
(3)④元素的最高价氧化物对应的水化物呈
(4)③④⑤对应元素中原子半径最小的是
(5)元素③与元素②形成的化合物,可用于呼吸面具或潜水艇中作为氧气的来源,它的化学式是
(6)少量元素③的单质通常保存在
(7)元素①的氢化物与元素②的氢化物更稳定的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大。A与C形成的化合物能使湿润的红色石蕊试纸变蓝;D是地壳中含量最多的元素;D、F原子的最外层电子数相等;E的焰色反应呈黄色;B元素的一种同位素在考古时可用于测定一些文物的年代。请回答下列问题:(注意回答问题时均用元素符号表示)
(1)元素B在周期表中的位置:___________ 。
(2)元素A与C组成的10电子的阳离子的电子式:___________ 。元素A与D组成的18电子分子的结构式:___________ 。
(3) 和
和 形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:
形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:___________ 。
(4)D和F的简单气态氢化物沸点比较高的是:___________ (写分子式),原因:______ 。
(5)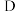 、
、 、
、 、G的简单离子半径由小到大的顺序为
、G的简单离子半径由小到大的顺序为___________ (用离子符号表示)。
(6)用电子式表示化合物E2D的形成过程:___________ 。
(1)元素B在周期表中的位置:
(2)元素A与C组成的10电子的阳离子的电子式:
(3)
 和
和 形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:
形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:(4)D和F的简单气态氢化物沸点比较高的是:
(5)
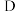 、
、 、
、 、G的简单离子半径由小到大的顺序为
、G的简单离子半径由小到大的顺序为(6)用电子式表示化合物E2D的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表列出了①~⑩十种元素在元素周期表中的位置。

根据表中元素①~⑩,回答下列问题:
(1)①元素有三种质子数相同,中子数不同的核素,互称为_______ 。
(2)③、⑤的最高价氧化物对应的水化物的碱性:③_______ ⑤(选填“>”或“<”)。
(3)⑧的固态氢化物 与
与 反应生成
反应生成 和一种可燃性气体单质
和一种可燃性气体单质_______ (填化学式)。
(4)某小组同学设计实验比较VIIA族元素的非金属性:
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有 溶液的棉球变为橙黄色,湿润的淀粉
溶液的棉球变为橙黄色,湿润的淀粉 试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。

乙同学设计实验如下:向A中通入少量 充分反应后,静置A中液体为橙黄色,将A中液体滴入试管内,取下试管,充分振荡,试管中的
充分反应后,静置A中液体为橙黄色,将A中液体滴入试管内,取下试管,充分振荡,试管中的 ;层变为紫红色。
;层变为紫红色。

①以上两位同学的实验,_______ (填“甲”或“乙)同学的实验能证明非金属性: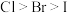 。
。
②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有_______ 。(填字母)
A. 、
、 、
、 的熔点逐渐升高 B.
的熔点逐渐升高 B. 、
、 、
、 的稳定性逐渐减弱
的稳定性逐渐减弱
C. 、
、 、
、 水溶液的酸性逐渐增强 D.
水溶液的酸性逐渐增强 D. 、
、 、
、 的还原性逐渐增强
的还原性逐渐增强

根据表中元素①~⑩,回答下列问题:
(1)①元素有三种质子数相同,中子数不同的核素,互称为
(2)③、⑤的最高价氧化物对应的水化物的碱性:③
(3)⑧的固态氢化物
 与
与 反应生成
反应生成 和一种可燃性气体单质
和一种可燃性气体单质(4)某小组同学设计实验比较VIIA族元素的非金属性:
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有
 溶液的棉球变为橙黄色,湿润的淀粉
溶液的棉球变为橙黄色,湿润的淀粉 试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
乙同学设计实验如下:向A中通入少量
 充分反应后,静置A中液体为橙黄色,将A中液体滴入试管内,取下试管,充分振荡,试管中的
充分反应后,静置A中液体为橙黄色,将A中液体滴入试管内,取下试管,充分振荡,试管中的 ;层变为紫红色。
;层变为紫红色。
①以上两位同学的实验,
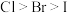 。
。②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有
A.
 、
、 、
、 的熔点逐渐升高 B.
的熔点逐渐升高 B. 、
、 、
、 的稳定性逐渐减弱
的稳定性逐渐减弱C.
 、
、 、
、 水溶液的酸性逐渐增强 D.
水溶液的酸性逐渐增强 D. 、
、 、
、 的还原性逐渐增强
的还原性逐渐增强
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】卤族元素能形成多种物质,结构和性质之间充满联系。
(1)部分卤族元素的某种性质a随核电荷数的变化趋势如图所示,则a表示正确的是_____ 。(填字母)
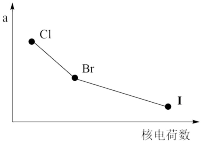
a.原子半径 b.氢化物的稳定性
c.单质的氧化性 d.元素的非金属性
(2)溴化碘(IBr)的化学性质类似于卤素单质,溴化碘和水反应所得产物中有一种为三原子分子,该分子的电子式为_____ ;溴原子核外电子能量最高的电子层符号是_____ 。
(3)ClF3的熔、沸点比BrF3的_____ (填“高”或“低”),理由是_____ 。
ClO2气体可处理污水中的CN-,以下是ClO2的两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
(4)ClO2与CN- (C是+2价)反应产生2种无毒气体,反应中氧化剂和还原剂物质的量之比为_____ 。
(5)请评价上述哪一种方法制备的ClO2更适合用于饮用水的消毒______ 。
(1)部分卤族元素的某种性质a随核电荷数的变化趋势如图所示,则a表示正确的是

a.原子半径 b.氢化物的稳定性
c.单质的氧化性 d.元素的非金属性
(2)溴化碘(IBr)的化学性质类似于卤素单质,溴化碘和水反应所得产物中有一种为三原子分子,该分子的电子式为
(3)ClF3的熔、沸点比BrF3的
ClO2气体可处理污水中的CN-,以下是ClO2的两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
(4)ClO2与CN- (C是+2价)反应产生2种无毒气体,反应中氧化剂和还原剂物质的量之比为
(5)请评价上述哪一种方法制备的ClO2更适合用于饮用水的消毒
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A、B、C、D、E、F、G为七种短周期主族元素,原子序数依次增大。已知:A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、G在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17,质子数之和为31。D与F同周期,且在该周期中D元素的原子半径最大。回答下列问题:
(1)B、C、G的简单氢化物中稳定性最弱的是____ (填化学式)。
(2)G的某种氧化物能使酸性KMnO4溶液褪色,反应的离子方程式为____ 。
(3)B、C、D、E、F形成的简单离子半径由小到大的顺序为____ (用离子符号表示)。
(4)A与B能形成离子化合物A5B,A5B中既含离子键又含共价键,其电子式为____ ,该物质能与水剧烈反应生成两种气体,这两种气体的化学式是____ 。
(5)F的最高价氧化物对应的水化物和D的最高价氧化物对应的水化物的水溶液发生反应的离子方程式为____ 。
(1)B、C、G的简单氢化物中稳定性最弱的是
(2)G的某种氧化物能使酸性KMnO4溶液褪色,反应的离子方程式为
(3)B、C、D、E、F形成的简单离子半径由小到大的顺序为
(4)A与B能形成离子化合物A5B,A5B中既含离子键又含共价键,其电子式为
(5)F的最高价氧化物对应的水化物和D的最高价氧化物对应的水化物的水溶液发生反应的离子方程式为
您最近一年使用:0次



