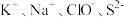下列实验结论正确且能作为相应定律或原理证据的是
| 选项 | A | B | C | D |
| 定律或原理 | 勒夏特列原理 | 元素周期律 | 盖斯定律 | 盐类水解原理 |
| 实验方案 | 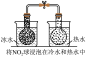 2NO2  N2O4 ΔH<0 N2O4 ΔH<0 | 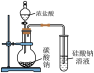 | 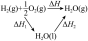 | 取pH试纸于玻璃片上,用玻璃棒蘸取少量次氯酸钠溶液,点在试纸上观察颜色测pH |
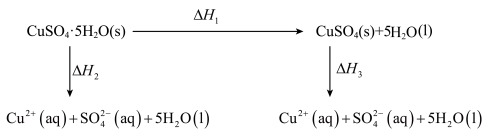
| 实验结论 | 气体颜色左球加深、右球变浅 | 验证元素非金属性:C > Si | 测得:ΔH=ΔH1+ΔH2 | 验证:次氯酸为弱酸 |
| A.A | B.B | C.C | D.D |
更新时间:2023-10-08 08:26:39
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图是氯及其部分化合物的“价类二维图”,下列说法错误的是
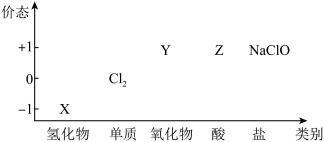

| A.Cl2的水溶液在空气中久置后,最终变成X的水溶液 |
| B.Y既有氧化性,又有还原性 |
| C.可存在X→Cl2→NaClO的转化关系 |
| D.X和Z在水溶液能够大量共存 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下图为某短周期元素的价类二维图,W为酸式盐。能正确描述反应的离子方程式的是
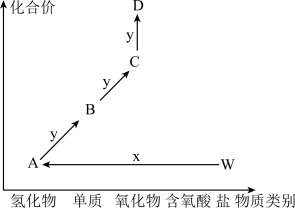

A.若x为强酸,W转化为A的反应为: +H+=SO2↑+H2O +H+=SO2↑+H2O |
| B.若x为强酸,少量C与Ca(ClO)2溶液的反应为:SO2+Ca2++H2O+2ClO-=CaSO3↓+2HClO |
C.若x为强碱,C与D按1:1混合后与NaOH溶液的反应为:NO+NO2+2OH-=2 +H2O +H2O |
D.若x为强碱,A与稀醋酸的反应为NH3+H+= |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知:
N2(g) + 2O2(g) =2 NO2(g) ΔH = +67.7kJ/mol
2N2H4(g) + 2NO2(g) =3N2(g) + 4H2O (g) ΔH = -1135.7kJ/mol
下列说法正确的是
N2(g) + 2O2(g) =2 NO2(g) ΔH = +67.7kJ/mol
2N2H4(g) + 2NO2(g) =3N2(g) + 4H2O (g) ΔH = -1135.7kJ/mol
下列说法正确的是
| A.N2H4(g) + O2(g) = N2(g) + 2H2O(g) ΔH = -1068 kJ/mol |
B.肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4 + H2O N2H5+ + OH- N2H5+ + OH- |
| C.铂做电极,以KOH溶液为电解质的肼——空气燃料电池,放电时的负极反应式:N2H4 -4e- + 4OH- = N2 + 4H2O |
D.2NO2 N2O4,加压时颜色加深,可以用勒夏特列原理解释 N2O4,加压时颜色加深,可以用勒夏特列原理解释 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】由金红石(TiO2)制取单质Ti的反应步骤为: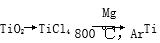
已知:①C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)===TiCl4(s)+O2(g) ΔH=+141 kJ·mol-1
则④TiO2(s)+2Cl2(g)+2C(s)===TiCl4(s)+2CO(g)的ΔH为
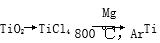
已知:①C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)===TiCl4(s)+O2(g) ΔH=+141 kJ·mol-1
则④TiO2(s)+2Cl2(g)+2C(s)===TiCl4(s)+2CO(g)的ΔH为
| A.—160 kJ·mol-1 | B.+160 kJ·mol-1 |
| C.-80 kJ·mol-1 | D.+80 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
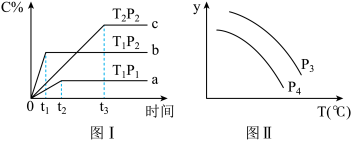
【推荐1】电厂烟气脱氮的主反应为:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) △H1,副反应为:2NH3(g)+8NO(g)
5N2(g)+6H2O(g) △H1,副反应为:2NH3(g)+8NO(g) 5N2O(g)+3H2O(g) △H2。平衡混合气中N2与N2O含量与温度的关系如图所示。下列说法错误的是( )
5N2O(g)+3H2O(g) △H2。平衡混合气中N2与N2O含量与温度的关系如图所示。下列说法错误的是( )
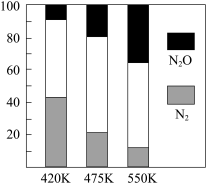
 5N2(g)+6H2O(g) △H1,副反应为:2NH3(g)+8NO(g)
5N2(g)+6H2O(g) △H1,副反应为:2NH3(g)+8NO(g) 5N2O(g)+3H2O(g) △H2。平衡混合气中N2与N2O含量与温度的关系如图所示。下列说法错误的是( )
5N2O(g)+3H2O(g) △H2。平衡混合气中N2与N2O含量与温度的关系如图所示。下列说法错误的是( )
| A.△H1<0 △H2>0 |
| B.选择合适的催化剂,升高温度等措施可以加快脱氮反应速率 |
| C.理论上较高的温度和较低压强有利于生成无公害气体 |
| D.反应过程中,采取不断分离出N2(g)有利于主反应的进行,提高反应物的转化率 |
您最近一年使用:0次
【推荐2】30℃时,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g) 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是
 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.当v逆(X)=2v正(Z),可以说明反应达平衡 |
| B.反应前2 min的平均速率v(Z)=2.0×10-3 mol/(L·min) |
| C.其他条件不变,再充入0.2 molZ,平衡时X的体积分数增大 |
| D.该反应在350℃时的平衡常数小于1.44 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某试剂的结构式如图所示, 四种元素分处三个短周期,原子序数依次增大,
四种元素分处三个短周期,原子序数依次增大, 原子的最外层电子数是
原子的最外层电子数是 原子最外层电子数的一半。下列说法正确的是
原子最外层电子数的一半。下列说法正确的是
 四种元素分处三个短周期,原子序数依次增大,
四种元素分处三个短周期,原子序数依次增大, 原子的最外层电子数是
原子的最外层电子数是 原子最外层电子数的一半。下列说法正确的是
原子最外层电子数的一半。下列说法正确的是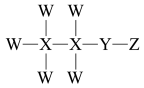
| A.该物质所含元素的原子核都是由质子和中子构成的 |
B.原子半径由大到小的顺序为 |
C. 和 和 两元素形成的最高价氧化物的水化物酸性: 两元素形成的最高价氧化物的水化物酸性: |
D.工业上一般可通过电解 的氧化物来制备单质 的氧化物来制备单质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素X、Y、Z、M原子序数依次增大,Z的单质为空气中的主要成分,M的最高价氧化物对应的水化物为强酸,它们组成的一种分子结构如图所示。下列说法中正确的是


| A.X、Y、Z、M的氧化物均为酸性氧化物 | B.X、Z、M组成的化合物均为共价化合物 |
| C.Y元素的某种核素可在考古时测定文物年代 | D.沸点: ,所以非金属性:M>Y ,所以非金属性:M>Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】根据下列操作和现象所得到的结论正确的是
| 操作和现象 | 结论 | |
| A | 向碳酸钙中加入盐酸,产生的气体经饱和碳酸氢钠溶液洗气后,再通入硅酸钠溶液,出现白色沉淀 | 利用该实验可以证明非金属性:Cl>C>Si |
| B | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的1,2-二溴乙烷无色,能溶于四氯化碳 |
| C | 向淀粉溶液中加入稀硫酸加热,再向其中加入过量的氢氧化钠溶液最后加碘水,溶液未变蓝 | 淀粉已经完全水解 |
| D | 将浸透石蜡油的石棉放在硬质试管的底部,试管中加入碎瓷片,用酒精灯给碎瓷片加强热,将产生的气体通入酸性高锰酸钾溶液中,溶液颜色逐渐褪去 | 蜡油分解产物一定为乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

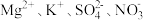

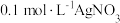 溶液:
溶液: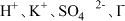
 溶液:
溶液: