氢能是一种极具发展潜能的清洁能源。对于可逆反应:
 ,在其他条件不变时,改变下列条件能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
,在其他条件不变时,改变下列条件能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是

 ,在其他条件不变时,改变下列条件能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
,在其他条件不变时,改变下列条件能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是| A.增大压强 | B.升高温度 | C.使用催化剂 | D.多充入CO |
更新时间:2023-10-09 22:10:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某探究性学习小组认为 与KI溶液反应时,能发生以下反应:①
与KI溶液反应时,能发生以下反应:①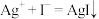
 ,②
,②
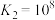 。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。
。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。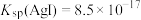 ,氧化性
,氧化性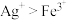 ,下列有关叙述正确的是
,下列有关叙述正确的是
 与KI溶液反应时,能发生以下反应:①
与KI溶液反应时,能发生以下反应:①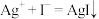
 ,②
,②
 。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。
。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。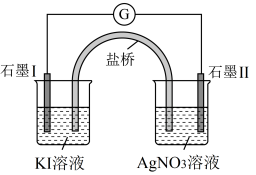
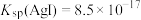 ,氧化性
,氧化性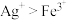 ,下列有关叙述正确的是
,下列有关叙述正确的是| A.石墨Ⅰ为正极,盐桥内溶质为KCl |
B.石墨Ⅱ的电极反应式为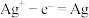 |
| C.往KI溶液中加入淀粉可检验生成的产物 |
D.平衡常数 : : ;反应活化能:①>② ;反应活化能:①>② |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列对于概念的理解正确的是
| A.溶液中存在溶质分子,该溶质就是弱电解质 |
| B.需要加热的化学反应就是吸热反应 |
| C.升高温度,反应速率加快,是因为体系内活化分子百分数增大 |
| D.活化分子之间的碰撞均能发生化学反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下图为一带可移动隔板的密闭容器,某温度下,左、右两侧反应均达到平衡,此时隔板处于容器中央。若保持温度不变,向左侧容器中充入一定量的H2,下列说法正确的是
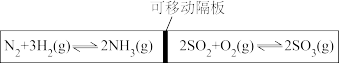
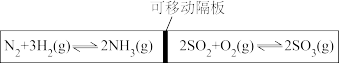
| A.两侧平衡均向正反应方向移动 |
| B.左侧平衡向逆反应方向移动 |
| C.右侧平衡向逆反应方向移动 |
| D.两侧平衡均向逆反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列现象不能用化学平衡移动原理解释的是
A.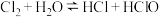 ,向新制氯水中加入碳酸钙,漂白性增强 ,向新制氯水中加入碳酸钙,漂白性增强 |
B.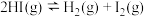 ,达平衡后缩小容器容积可使体系颜色变深 ,达平衡后缩小容器容积可使体系颜色变深 |
C.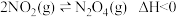 ,将装有NO2的玻璃球浸入热水中,红棕色变深 ,将装有NO2的玻璃球浸入热水中,红棕色变深 |
D.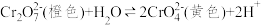 ,向K2Cr2O7溶液中滴加几滴浓硫酸,橙色加深 ,向K2Cr2O7溶液中滴加几滴浓硫酸,橙色加深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知反应2H2(g)+CO(g)⇌CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,
测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列大小比较正确的是

测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列大小比较正确的是
平衡常数 | 温度/℃ | ||
500 | 700 | 800 | |
K | 2.50 | 0.34 | 0.15 |

| A.平衡常数:K(a)>K(c),K(b)=K(d) |
| B.正反应速率:v(a)>v(c),v(b)=v(d) |
| C.达到平衡所需时间:t(a)=t(c),t(b)>t(d) |
| D.平均相对分子质量:M(a)=M(c),M(b)>M(d) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】O3是一种理想的脱硝剂,其脱硝反应之一为2NO (g)+3O3(g) N2O5(g)+3O2(g)
N2O5(g)+3O2(g)  。在某恒容密闭容器中充入一定量的O3和NO,在不同温度下测得c(N2O5)与时间的关系如图所示,下列说法正确的是
。在某恒容密闭容器中充入一定量的O3和NO,在不同温度下测得c(N2O5)与时间的关系如图所示,下列说法正确的是
 N2O5(g)+3O2(g)
N2O5(g)+3O2(g)  。在某恒容密闭容器中充入一定量的O3和NO,在不同温度下测得c(N2O5)与时间的关系如图所示,下列说法正确的是
。在某恒容密闭容器中充入一定量的O3和NO,在不同温度下测得c(N2O5)与时间的关系如图所示,下列说法正确的是
| A.温度:T1>T2 | B.平衡常数:K(T1)>K(T2) |
| C.反应速率:vb(正)>va(正) | D.高温条件下,有利于该反应自发进行 |
您最近一年使用:0次


 4N2+6H2O
4N2+6H2O 溶液中滴加草酸溶液,观察紫色是否消失
溶液中滴加草酸溶液,观察紫色是否消失  沉淀转入烧杯中,加足量稀硫酸溶解,加热浓缩,冷却结晶
沉淀转入烧杯中,加足量稀硫酸溶解,加热浓缩,冷却结晶  和
和 ,发生反应
,发生反应 。达到平衡后,下列说法正确的是
。达到平衡后,下列说法正确的是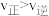 ,平衡常数增大
,平衡常数增大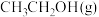 的浓度增大
的浓度增大 ,
, 变大,
变大, 变小
变小

