葡萄糖酸锌是一种抗缺锌药物,可由 为原料制得。工业上以废锌铁合金(主要成分为Zn,含有少量的Fe、Fe2O3、ZnO、CuO和油污等杂质)为原料制备
为原料制得。工业上以废锌铁合金(主要成分为Zn,含有少量的Fe、Fe2O3、ZnO、CuO和油污等杂质)为原料制备 的流程如图。
的流程如图。

(1)碱洗的目的是___________ 。
(2)氧化时发生反应的离子方程式为___________ 。
(3)取“氧化”过程中的上层清液,滴加酸性 稀溶液,紫红色褪去,可能的原因是
稀溶液,紫红色褪去,可能的原因是_____ 。
(4)由过滤所得的滤液为原料制备 ,请补充完整相应的实验方案:向滤液中
,请补充完整相应的实验方案:向滤液中___________ ,过滤、晾干,得到 。
。
实验中须用到的试剂:锌粉、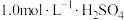 。
。
(5)以 为原料可制得葡萄糖酸锌
为原料可制得葡萄糖酸锌 。为测定葡萄糖酸锌样品的纯度,进行下列实验。
。为测定葡萄糖酸锌样品的纯度,进行下列实验。
步骤1:称取5.200g样品溶于水配成100mL溶液,取25.00mL置于锥形瓶中,滴入少量的铬黑T作指示剂。
步骤2:向锥形瓶中加入过量的 ,振荡。
,振荡。
步骤3:用 锌标准溶液滴定过量的EDTA至终点,消耗锌标准溶液16.00mL(已知:
锌标准溶液滴定过量的EDTA至终点,消耗锌标准溶液16.00mL(已知: 与EDTA反应的化学计量比为1∶1)。
与EDTA反应的化学计量比为1∶1)。
①计算此产品中锌元素的质量分数:___________ 。(写出计算过程)
②葡萄糖酸锌中锌元素的含量为14.28%,对照①计算结果,产生误差的可能原因是(样品纯或不纯)___________ 。
 为原料制得。工业上以废锌铁合金(主要成分为Zn,含有少量的Fe、Fe2O3、ZnO、CuO和油污等杂质)为原料制备
为原料制得。工业上以废锌铁合金(主要成分为Zn,含有少量的Fe、Fe2O3、ZnO、CuO和油污等杂质)为原料制备 的流程如图。
的流程如图。
(1)碱洗的目的是
(2)氧化时发生反应的离子方程式为
(3)取“氧化”过程中的上层清液,滴加酸性
 稀溶液,紫红色褪去,可能的原因是
稀溶液,紫红色褪去,可能的原因是(4)由过滤所得的滤液为原料制备
 ,请补充完整相应的实验方案:向滤液中
,请补充完整相应的实验方案:向滤液中 。
。实验中须用到的试剂:锌粉、
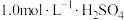 。
。(5)以
 为原料可制得葡萄糖酸锌
为原料可制得葡萄糖酸锌 。为测定葡萄糖酸锌样品的纯度,进行下列实验。
。为测定葡萄糖酸锌样品的纯度,进行下列实验。步骤1:称取5.200g样品溶于水配成100mL溶液,取25.00mL置于锥形瓶中,滴入少量的铬黑T作指示剂。
步骤2:向锥形瓶中加入过量的
 ,振荡。
,振荡。步骤3:用
 锌标准溶液滴定过量的EDTA至终点,消耗锌标准溶液16.00mL(已知:
锌标准溶液滴定过量的EDTA至终点,消耗锌标准溶液16.00mL(已知: 与EDTA反应的化学计量比为1∶1)。
与EDTA反应的化学计量比为1∶1)。①计算此产品中锌元素的质量分数:
②葡萄糖酸锌中锌元素的含量为14.28%,对照①计算结果,产生误差的可能原因是(样品纯或不纯)
更新时间:2023-09-15 13:30:41
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】磷酸二氢钾( )广泛用于工农业生产中,以磷灰石为原料生产磷酸二氢钾的工业流程为:
)广泛用于工农业生产中,以磷灰石为原料生产磷酸二氢钾的工业流程为:
I.制备磷酸
方法1——热法(如图)
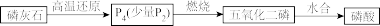
方法2——湿法(如图)

已知:①磷灰石的主要成分是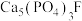 ,还含有铝、铁、镁、硅等元素。
,还含有铝、铁、镁、硅等元素。
②白磷( )常温下为固体,易升华。
)常温下为固体,易升华。
③除了钾、钠、铵外的磷酸盐、磷酸一氢盐往往难溶于水;磷酸二氢盐绝大多数都易溶于水。
(1)热法和湿法都需要先将磷灰石粉碎,目的是___________ 。
(2)“高温还原”是在石英砂(主要成分 )存在下,用焦炭将
)存在下,用焦炭将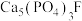 还原,反应过程中同时有CO和两种钙盐生成,主要反应的化学方程式为
还原,反应过程中同时有CO和两种钙盐生成,主要反应的化学方程式为___________ 。
(3)“酸浸”时,用两酸(硫酸和磷酸)分步浸取比只用硫酸浸取率更高,先加入的酸为___________ 。酸浸时会产生一种能腐蚀玻璃的物质,这种物质的分子式为___________ 。
(4)“脱硫”时,用 除去粗磷酸中少量的
除去粗磷酸中少量的 ,其离子方程式为
,其离子方程式为___________ 。
(5)与湿法相比,热法制备磷酸的缺点是___________ 。(列一条)
II.制备磷酸二氢钾
向原料液(含等物质的量KCl与 的水溶液)加入正三丁胺(难溶于水的无色液体、弱碱),保持30℃一个小时,抽滤,滤饼经洗涤、干燥得磷酸二氢钾,滤液中加入氨水再生有机相,并生成副产物。
的水溶液)加入正三丁胺(难溶于水的无色液体、弱碱),保持30℃一个小时,抽滤,滤饼经洗涤、干燥得磷酸二氢钾,滤液中加入氨水再生有机相,并生成副产物。
(6)正三丁胺在制备过程中的作用为___________ 。
(7)副产物的化学式为___________ 。
(8)若制备磷酸过程中磷元素损失a%,制备磷酸二氢钾时原料的转化率为b%,则1吨含“ ”(类似于盐可写成氧化物的形式)28.4%的磷灰石可生产磷酸二氢钾
”(类似于盐可写成氧化物的形式)28.4%的磷灰石可生产磷酸二氢钾___________ g。
 )广泛用于工农业生产中,以磷灰石为原料生产磷酸二氢钾的工业流程为:
)广泛用于工农业生产中,以磷灰石为原料生产磷酸二氢钾的工业流程为:I.制备磷酸
方法1——热法(如图)
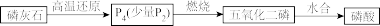
方法2——湿法(如图)

已知:①磷灰石的主要成分是
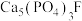 ,还含有铝、铁、镁、硅等元素。
,还含有铝、铁、镁、硅等元素。②白磷(
 )常温下为固体,易升华。
)常温下为固体,易升华。③除了钾、钠、铵外的磷酸盐、磷酸一氢盐往往难溶于水;磷酸二氢盐绝大多数都易溶于水。
(1)热法和湿法都需要先将磷灰石粉碎,目的是
(2)“高温还原”是在石英砂(主要成分
 )存在下,用焦炭将
)存在下,用焦炭将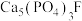 还原,反应过程中同时有CO和两种钙盐生成,主要反应的化学方程式为
还原,反应过程中同时有CO和两种钙盐生成,主要反应的化学方程式为(3)“酸浸”时,用两酸(硫酸和磷酸)分步浸取比只用硫酸浸取率更高,先加入的酸为
(4)“脱硫”时,用
 除去粗磷酸中少量的
除去粗磷酸中少量的 ,其离子方程式为
,其离子方程式为(5)与湿法相比,热法制备磷酸的缺点是
II.制备磷酸二氢钾
向原料液(含等物质的量KCl与
 的水溶液)加入正三丁胺(难溶于水的无色液体、弱碱),保持30℃一个小时,抽滤,滤饼经洗涤、干燥得磷酸二氢钾,滤液中加入氨水再生有机相,并生成副产物。
的水溶液)加入正三丁胺(难溶于水的无色液体、弱碱),保持30℃一个小时,抽滤,滤饼经洗涤、干燥得磷酸二氢钾,滤液中加入氨水再生有机相,并生成副产物。(6)正三丁胺在制备过程中的作用为
(7)副产物的化学式为
(8)若制备磷酸过程中磷元素损失a%,制备磷酸二氢钾时原料的转化率为b%,则1吨含“
 ”(类似于盐可写成氧化物的形式)28.4%的磷灰石可生产磷酸二氢钾
”(类似于盐可写成氧化物的形式)28.4%的磷灰石可生产磷酸二氢钾
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】锰是重要的合金材料和催化剂,在工农业生产和科技领域有广泛的用途。将废旧锌锰电池回收处理后,将含MnO2、MnOOH、Zn(OH)2及少量Fe的废料进行回收处理,能实现资源的再生利用。用该废料制备Zn和MnO2的一种工艺流程如图:

已知:Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
回答下列问题:
(1)还原焙烧过程中,MnOOH与炭黑反应,锰元素被还原为MnO,该反应的化学方程式为_____ 。
(2)滤渣1主要成分的化学式是________ 。
(3)净化阶段
①为了除掉滤渣2中的元素,选择最佳的加入试剂为______ (填序号)。
A.氯水 B.O2 C.氨水 D.MnCO3
②已知:室温下,Ksp[Mn(OH)2]=10-13,Ksp[Fe(OH)3]=1×10-38,Ksp[Zn(OH)2]=10-17。净化时溶液中Mn2+、Zn2+的浓度约为0. 1mol·L-1,调节pH的合理范围是______ 。
(4)将MnO2和Li2CO3按4:1的物质的量比配料,混合搅拌,然后升温至600C~750°C, 制取产品LiMn2O4。写出该反应的化学方程式:________ 。
(5)LiMn2O4材料常制作成可充电电池(如图),该电池的总反应为

①充电时,锰酸锂为电池的_______ (填“正极”“负极”“阴极”或“阳极”);该电极上发生的电极反应式为______________ 。
②该电池作为电源放电时,若电路中转移0.2mol e-,则石墨电极将减重____________ 。

已知:Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
回答下列问题:
(1)还原焙烧过程中,MnOOH与炭黑反应,锰元素被还原为MnO,该反应的化学方程式为
(2)滤渣1主要成分的化学式是
(3)净化阶段
①为了除掉滤渣2中的元素,选择最佳的加入试剂为
A.氯水 B.O2 C.氨水 D.MnCO3
②已知:室温下,Ksp[Mn(OH)2]=10-13,Ksp[Fe(OH)3]=1×10-38,Ksp[Zn(OH)2]=10-17。净化时溶液中Mn2+、Zn2+的浓度约为0. 1mol·L-1,调节pH的合理范围是
(4)将MnO2和Li2CO3按4:1的物质的量比配料,混合搅拌,然后升温至600C~750°C, 制取产品LiMn2O4。写出该反应的化学方程式:
(5)LiMn2O4材料常制作成可充电电池(如图),该电池的总反应为


①充电时,锰酸锂为电池的
②该电池作为电源放电时,若电路中转移0.2mol e-,则石墨电极将减重
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】碘化亚铁( )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)___________ ,若无此装置,写出铁粉参与的副反应的化学方程式:___________ 。
(2)硬质玻璃管直接接入收集器而不用导管的原因是___________ ,收集器浸泡在冷水中的原因是___________ 。
(3)试剂a的作用是___________ 。
(4)已知氧化性: 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:___________ 。
 )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)
(2)硬质玻璃管直接接入收集器而不用导管的原因是
(3)试剂a的作用是
(4)已知氧化性:
 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】现有常温条件下甲、乙、丙三种溶液,甲为0.1mol·L-1的NaOH溶液,乙为0.1mol·L-1的HCl溶液,丙为0.1mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=_______ ;
(2)丙溶液中存在的电离平衡为________________ (用电离平衡方程式表示);
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的由小到大顺序为________ ;

(4)某同学用甲溶液分别滴定20.00mL乙溶液和20.00mL丙溶液,得到如图所示两条滴定曲线,请完成有关问题:
①甲溶液滴定丙溶液的曲线是________ (填“图1”或“图2”);
②a=_________ mL
③pH试纸测定溶液pH的操作方法为_______________________________ 。
(1)甲溶液的pH=
(2)丙溶液中存在的电离平衡为
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的由小到大顺序为

(4)某同学用甲溶液分别滴定20.00mL乙溶液和20.00mL丙溶液,得到如图所示两条滴定曲线,请完成有关问题:
①甲溶液滴定丙溶液的曲线是
②a=
③pH试纸测定溶液pH的操作方法为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】辉铜矿与铜蓝矿都是天然含硫铜矿,在地壳中二者常伴生存在。现取一份该伴生矿样品,经检测后确定仅含Cu2S、CuS和惰性杂质。为进一步确定其中Cu2S、CuS的含量,某同学进行了如下实验:
①取2.6g样品,加入200.0mL0.2000mol·L-1酸性KMnO4溶液,加热(硫元素全部转化为SO42-),滤去不溶杂质;
②收集滤液至250mL容量瓶中,定容;
③取25.00mL溶液,用0.1000mol·L-1FeSO4溶液滴定,消耗20.00mL;
④加入适量NH4HF2溶液(掩蔽Fe3+和Mn2+,使其不再参与其他反应),再加入过量KI固体,轻摇使之溶解并发生反应:2Cu2++4I-=2CuI+I2;
⑤加入2滴淀粉溶液,用0.1000mol·L-1Na2S2O3溶液滴定,消耗30.00mL(已知:2S2O32-+I2=S4O62-+2I-)。
回答下列问题:
(1)写出Cu2S溶于酸性KMnO4溶液的离子方程式:___________ ;
(2)配制0.1000mol· L-1FeSO4溶液时要用煮沸过的稀硫酸,原因是___________ ,配制过程中所需玻璃仪器除了烧杯、玻璃棒、容量瓶外还有___________ ;
(3)③中取25.00mL待测溶液所用的仪器是___________ ;
(4)⑤中滴定至终点时的现象为___________ ;
(5)混合样品中Cu2S和CuS的含量分别为_________ %、_________ %(结果均保留1位小数)。
①取2.6g样品,加入200.0mL0.2000mol·L-1酸性KMnO4溶液,加热(硫元素全部转化为SO42-),滤去不溶杂质;
②收集滤液至250mL容量瓶中,定容;
③取25.00mL溶液,用0.1000mol·L-1FeSO4溶液滴定,消耗20.00mL;
④加入适量NH4HF2溶液(掩蔽Fe3+和Mn2+,使其不再参与其他反应),再加入过量KI固体,轻摇使之溶解并发生反应:2Cu2++4I-=2CuI+I2;
⑤加入2滴淀粉溶液,用0.1000mol·L-1Na2S2O3溶液滴定,消耗30.00mL(已知:2S2O32-+I2=S4O62-+2I-)。
回答下列问题:
(1)写出Cu2S溶于酸性KMnO4溶液的离子方程式:
(2)配制0.1000mol· L-1FeSO4溶液时要用煮沸过的稀硫酸,原因是
(3)③中取25.00mL待测溶液所用的仪器是
(4)⑤中滴定至终点时的现象为
(5)混合样品中Cu2S和CuS的含量分别为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】实验室中以活性炭为催化剂制备 并测定钴元素的含量。
并测定钴元素的含量。
已知: 是橙黄色晶体,可溶于水和稀酸、不溶于乙醇;在强碱溶液中煮沸产生
是橙黄色晶体,可溶于水和稀酸、不溶于乙醇;在强碱溶液中煮沸产生 、
、 ;
; 不易被氧化,
不易被氧化, 有较强还原性。
有较强还原性。
Ⅰ.制备晶体(装置如图1,55℃水浴加热)
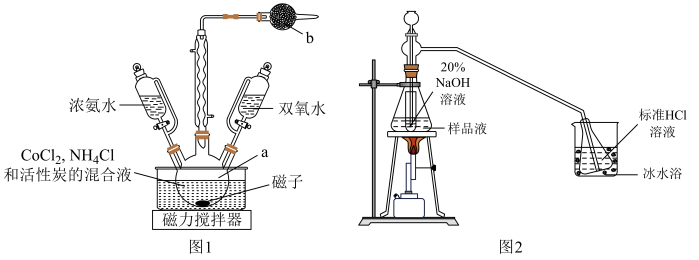
Ⅱ.测定产品 中钴元素的含量(装置如图2)
中钴元素的含量(装置如图2)
称取 样品于锥形瓶中,加水溶解。在另一锥形瓶中加入
样品于锥形瓶中,加水溶解。在另一锥形瓶中加入 标准
标准 溶液并置于冰水浴中,向漏斗中加入足量
溶液并置于冰水浴中,向漏斗中加入足量 的
的 溶液,加热,保持微沸状态一段时间后,取出插入标准
溶液,加热,保持微沸状态一段时间后,取出插入标准 溶液中的导气管,用蒸馏水冲洗导管内外,洗涤液并入装有标准
溶液中的导气管,用蒸馏水冲洗导管内外,洗涤液并入装有标准 溶液的锥形瓶中。取出锥形瓶,加入指示剂,用
溶液的锥形瓶中。取出锥形瓶,加入指示剂,用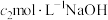 标准溶液滴定剩余的
标准溶液滴定剩余的 ,滴定终点时消耗
,滴定终点时消耗 标准溶液
标准溶液 。
。
回答下列问题:
(1) 制备
制备 的化学方程式为
的化学方程式为___________ 。
(2)仪器a的名称是___________ ;b中的试剂是___________ 。
(3)向 、
、 和活性炭混合液中先加浓氨水目的是
和活性炭混合液中先加浓氨水目的是___________ 。
(4)样品中钴元素的质量分数为___________ (用含 、
、 、
、 、
、 、
、 的代数式表示)。若缺少“蒸馏水冲洗导管内外”,会使测定结果
的代数式表示)。若缺少“蒸馏水冲洗导管内外”,会使测定结果___________ (填“偏高”“偏低”或“无影响”)。
(5)① 的空间结构为正八面体,若
的空间结构为正八面体,若 中2个
中2个 被2个
被2个 取代,能得到
取代,能得到___________ 种产物。
②钴(Ⅱ)与氯化钴和氨水以及 反应中若不加活性炭催化剂,可能有
反应中若不加活性炭催化剂,可能有 、
、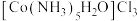 生成。现有
生成。现有 浓度为
浓度为 的
的 或
或 溶液,用
溶液,用 的
的 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液
溶液 ,则该溶液中的溶质为
,则该溶液中的溶质为___________ (填化学式)。
 并测定钴元素的含量。
并测定钴元素的含量。已知:
 是橙黄色晶体,可溶于水和稀酸、不溶于乙醇;在强碱溶液中煮沸产生
是橙黄色晶体,可溶于水和稀酸、不溶于乙醇;在强碱溶液中煮沸产生 、
、 ;
; 不易被氧化,
不易被氧化, 有较强还原性。
有较强还原性。Ⅰ.制备晶体(装置如图1,55℃水浴加热)

Ⅱ.测定产品
 中钴元素的含量(装置如图2)
中钴元素的含量(装置如图2)称取
 样品于锥形瓶中,加水溶解。在另一锥形瓶中加入
样品于锥形瓶中,加水溶解。在另一锥形瓶中加入 标准
标准 溶液并置于冰水浴中,向漏斗中加入足量
溶液并置于冰水浴中,向漏斗中加入足量 的
的 溶液,加热,保持微沸状态一段时间后,取出插入标准
溶液,加热,保持微沸状态一段时间后,取出插入标准 溶液中的导气管,用蒸馏水冲洗导管内外,洗涤液并入装有标准
溶液中的导气管,用蒸馏水冲洗导管内外,洗涤液并入装有标准 溶液的锥形瓶中。取出锥形瓶,加入指示剂,用
溶液的锥形瓶中。取出锥形瓶,加入指示剂,用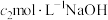 标准溶液滴定剩余的
标准溶液滴定剩余的 ,滴定终点时消耗
,滴定终点时消耗 标准溶液
标准溶液 。
。回答下列问题:
(1)
 制备
制备 的化学方程式为
的化学方程式为(2)仪器a的名称是
(3)向
 、
、 和活性炭混合液中先加浓氨水目的是
和活性炭混合液中先加浓氨水目的是(4)样品中钴元素的质量分数为
 、
、 、
、 、
、 、
、 的代数式表示)。若缺少“蒸馏水冲洗导管内外”,会使测定结果
的代数式表示)。若缺少“蒸馏水冲洗导管内外”,会使测定结果(5)①
 的空间结构为正八面体,若
的空间结构为正八面体,若 中2个
中2个 被2个
被2个 取代,能得到
取代,能得到②钴(Ⅱ)与氯化钴和氨水以及
 反应中若不加活性炭催化剂,可能有
反应中若不加活性炭催化剂,可能有 、
、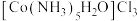 生成。现有
生成。现有 浓度为
浓度为 的
的 或
或 溶液,用
溶液,用 的
的 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液
溶液 ,则该溶液中的溶质为
,则该溶液中的溶质为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】Ⅰ.铁是日常生活中常见的元素之一,应用非常广泛。试回答下列问题:
(1)Fe2+的基态电子排布式为_______ ,铁在周期表中的位置_______ 。
(2)FeCl3水溶液pH_______ 7,原因是_______ (用化学方程式作答),把氯化铁溶液蒸干灼烧得到_______ (化学式)。
Ⅱ.葡萄糖酸亚铁[(C6H11O7)2Fe]是吸收效果好的营养强化剂,常温下易溶于水。一种制备葡萄糖酸亚铁的实验流程如下:

(3)工业上硫酸亚铁可用硫铁矿(主要成分FeS2)与硫酸铁溶液反应制得,同时得到硫酸,写出该反应的化学方程式:_______ 。
(4)为制得FeCO3,反应Ⅰ中混合两种试剂的操作为_______ 。
(5)反应Ⅱ中需加入稍过量的葡萄糖酸,目的是_______ 。
(1)Fe2+的基态电子排布式为
(2)FeCl3水溶液pH
Ⅱ.葡萄糖酸亚铁[(C6H11O7)2Fe]是吸收效果好的营养强化剂,常温下易溶于水。一种制备葡萄糖酸亚铁的实验流程如下:

(3)工业上硫酸亚铁可用硫铁矿(主要成分FeS2)与硫酸铁溶液反应制得,同时得到硫酸,写出该反应的化学方程式:
(4)为制得FeCO3,反应Ⅰ中混合两种试剂的操作为
(5)反应Ⅱ中需加入稍过量的葡萄糖酸,目的是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】用Zn(主要含有Fe、Al、Pb杂质)和硫酸来制取H2,利用制氢废液制备硫酸锌晶体(ZnSO4·7H2O)、Al2O3和Fe2O3,流程如下:
已知Al3+、Fe3+、Zn2+的氢氧化物完全沉淀的pH分别为5.2、4.1和8.5,ZnSO4·7H2O晶体易溶于水,易风化。回答下列问题:
(1)调节pH=2的目的是______________ ,调节pH=2,可加入_________ (填化学式)。
(2)写出生成沉淀3的化学方程式:______________________ 。
(3)加热浓缩ZnSO4溶液出现极薄品膜时,要停止加热的主要原因是_____________ 。
(4)某同学用如图所示的装置抽滤。
①有关抽滤的说法正确的是__________ 。
A.抽滤的目的主要是得到较干燥的沉淀
B.滤纸的直径应略小于漏斗内径,又能盖住全部小孔
C.图中有一处出错
D.抽滤结束,从吸滤瓶的支管口倒出滤液
②抽滤,洗涤沉淀的具体操作是___________________________ 。
(5)为得到干燥的ZnSO4·7H2O产品,选择干燥方法是________ 。
A.加热烘干 B.用浓H2SO4干燥
C.用酒精洗干 D.在空气中自然干燥
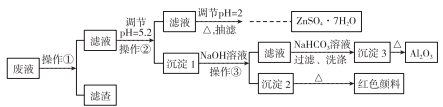
已知Al3+、Fe3+、Zn2+的氢氧化物完全沉淀的pH分别为5.2、4.1和8.5,ZnSO4·7H2O晶体易溶于水,易风化。回答下列问题:
(1)调节pH=2的目的是
(2)写出生成沉淀3的化学方程式:
(3)加热浓缩ZnSO4溶液出现极薄品膜时,要停止加热的主要原因是
(4)某同学用如图所示的装置抽滤。
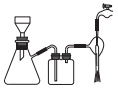
①有关抽滤的说法正确的是
A.抽滤的目的主要是得到较干燥的沉淀
B.滤纸的直径应略小于漏斗内径,又能盖住全部小孔
C.图中有一处出错
D.抽滤结束,从吸滤瓶的支管口倒出滤液
②抽滤,洗涤沉淀的具体操作是
(5)为得到干燥的ZnSO4·7H2O产品,选择干燥方法是
A.加热烘干 B.用浓H2SO4干燥
C.用酒精洗干 D.在空气中自然干燥
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】溶液A中存在Ba2+、Fe2+、Al3+、Fe3+、Cu2+、HCO 、CO
、CO 、Cl-、NO
、Cl-、NO 、SO
、SO 中的五种离子,浓度均为0.01 mol·L-1,溶液体积为1 L。对溶液A进行以下实验,整个过程如图所示(部分产物省略),溶液B与溶液A中所含阴离子种类相同。
中的五种离子,浓度均为0.01 mol·L-1,溶液体积为1 L。对溶液A进行以下实验,整个过程如图所示(部分产物省略),溶液B与溶液A中所含阴离子种类相同。
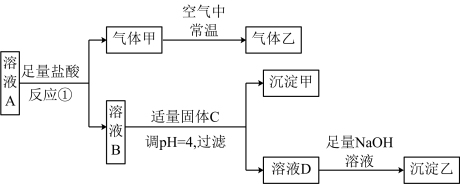
请回答下列问题:
(1)溶液A中的离子为___________ ;溶液A显___________ (填“酸”“碱”或“中”)性,用离子方程式表示原因___________ (写出一个即可)。
(2)反应①的离子方程式为___________ 。
(3)沉淀甲是___________ ,沉淀乙是___________ (填化学式)。
(4)固体C可能是___________(填字母)。
(5)气体甲、气体乙都能造成环境问题,将等体积的气体甲和乙通入足量NaOH溶液中,被完全吸收,写出反应的离子方程式为___________ 。
(6)若向原溶液A中加入足量的NaOH溶液,充分反应后将沉淀过滤、洗涤、干燥并灼烧至恒重,得到固体的质量为___________ g。
 、CO
、CO 、Cl-、NO
、Cl-、NO 、SO
、SO 中的五种离子,浓度均为0.01 mol·L-1,溶液体积为1 L。对溶液A进行以下实验,整个过程如图所示(部分产物省略),溶液B与溶液A中所含阴离子种类相同。
中的五种离子,浓度均为0.01 mol·L-1,溶液体积为1 L。对溶液A进行以下实验,整个过程如图所示(部分产物省略),溶液B与溶液A中所含阴离子种类相同。
请回答下列问题:
(1)溶液A中的离子为
(2)反应①的离子方程式为
(3)沉淀甲是
(4)固体C可能是___________(填字母)。
| A.CuO | B.Cu(OH)2 | C.CuSO4 | D.CuCl2 |
(6)若向原溶液A中加入足量的NaOH溶液,充分反应后将沉淀过滤、洗涤、干燥并灼烧至恒重,得到固体的质量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】Mn3O4可用于电子工业生产软磁铁氧体,用作电子计算机中存储信息的磁芯、磁盘等。软锰矿主要成分是MnO2,还含有少量的Fe2O3、SiO2、Al2O3,采用以下工艺流程可由软锰矿制得Mn3O4。
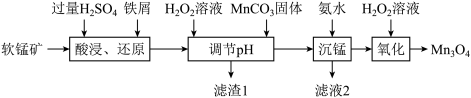
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)“酸浸、还原”时,为了加快化学反应速率,可以采取的措施有________ (只需填一种),“酸浸、还原”后溶液中含有的金属阳离子主要有________ ,铁屑与MnO2发生反应的离子方程式为________ 。
(2)“调节pH”时加入H2O2溶液的目的是________ ,“调节pH”的范围为________ 。
(3)“沉锰”时,其他条件一定,沉锰过程中锰离子的沉淀率与溶液温度的关系如图所示。50℃后,溶液温度越高,锰离子的沉淀率越低的原因是________ 。

(4)“氧化”时一般控制温度在80℃~85℃,可以采取的加热方法是________ ,反应化学方程式为________ 。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
(1)“酸浸、还原”时,为了加快化学反应速率,可以采取的措施有
(2)“调节pH”时加入H2O2溶液的目的是
(3)“沉锰”时,其他条件一定,沉锰过程中锰离子的沉淀率与溶液温度的关系如图所示。50℃后,溶液温度越高,锰离子的沉淀率越低的原因是

(4)“氧化”时一般控制温度在80℃~85℃,可以采取的加热方法是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】五水合硫代硫酸钠(Na2S2O3﹒5H2O,式量为248)俗称海波、大苏打,可用于纺织、造纸等领域。某学习小组制备Na2S2O3﹒5H2O,并测定产品纯度,实验方案如下。
I.制备Na2S2O3﹒5H2O
已知:S+Na2SO3 Na2S2O3
Na2S2O3
按如图所示装置(加热及夹持装置省略)进行实验,再经多步操作制得Na2S2O3﹒5H2O的粗产品

(1)仪器F的名称为_____ ,装置B的作用之一是观察SO2的生成速率,其中的试剂最好选用_____ 。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(2)用离子方程式表示Na2CO3溶液的作用:_____ 。
(3)C中溶液经过滤、_____ 、_____ 、过滤洗涤、干燥可制得粗产品。
Ⅱ.测定产品纯度
称取粗产品12.400g配制成100mL溶液,取25.00mL该溶液于锥形瓶中,用0.2500mol·L-1的I2标准液滴定,反应原理为:I2+2S2O →2I-+S4O
→2I-+S4O ,实验数据如表:
,实验数据如表:
(4)用_____ 作为指示剂,滴定至终点时溶液的颜色由_____ 色变为_____ 色,且30s内溶液颜色不变。粗产品中Na2S2O3﹒5H2O的质量分数为_____ 。下列情况可能导致测量结果偏低的操作是_____ 。
a.粗产品中Na2S2O3﹒5H2O失去部分结晶水
b.滴定前装I2标准液的滴定管未用标准液润洗
c.锥形瓶用蒸馏水洗净后未用待测液润洗
d.滴定时锥形瓶中有少量液滴溅出
I.制备Na2S2O3﹒5H2O
已知:S+Na2SO3
 Na2S2O3
Na2S2O3按如图所示装置(加热及夹持装置省略)进行实验,再经多步操作制得Na2S2O3﹒5H2O的粗产品


(1)仪器F的名称为
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(2)用离子方程式表示Na2CO3溶液的作用:
(3)C中溶液经过滤、
Ⅱ.测定产品纯度
称取粗产品12.400g配制成100mL溶液,取25.00mL该溶液于锥形瓶中,用0.2500mol·L-1的I2标准液滴定,反应原理为:I2+2S2O
 →2I-+S4O
→2I-+S4O ,实验数据如表:
,实验数据如表:| 编号 | 初读数(mL) | 末读数(mL) |
| ① | 0.00 | 19.99 |
| ② | 1.00 | 21.01 |
| ③ | 1.00 | 23.00 |
a.粗产品中Na2S2O3﹒5H2O失去部分结晶水
b.滴定前装I2标准液的滴定管未用标准液润洗
c.锥形瓶用蒸馏水洗净后未用待测液润洗
d.滴定时锥形瓶中有少量液滴溅出
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】氮化镓(GaN)在5G基站及工业互联网系统建设等方面用途广泛。从砷化镓废料(主要成分为GaAs,含Fe2O3、 SiO2和CaCO3等杂质)中回收砷,制备GaN的工艺流程如图:
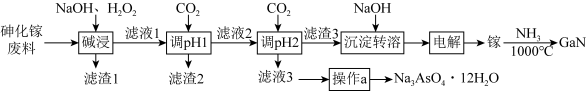
已知:①Ga与Al同主族,化学性质相似;
②离子完全沉淀的pH值: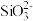 为8,
为8, 为5.5。
为5.5。
回答下列问题:
(1)为了提高“碱浸”效率应采用的措施是_______ (写 出一种措施)。
(2)“滤液1”中含有NaGaO2等溶质, “碱浸”时反应的离子方程式为_______ 。“滤渣1”的成分为_______ (填化学式)。
(3)通CO2两次调pH的原因是_______ 。
(4)“操作a”为_______ 、过滤、洗涤、干燥。
(5)“电解”时阴极的电极反应为_______ 。
(6)制备GaN时,参与反应的氧化剂与还原剂的物质的量之比为_______ 。
(7)取m克GaN样品溶于足量的热NaOH溶液(GaN+OH- +H2O = +NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
+NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是_______ 。(已知: NH3+H3BO3 =NH3·H3BO3;NH3·H3BO3 +HCl=NH4Cl+H3BO3 )

已知:①Ga与Al同主族,化学性质相似;
②离子完全沉淀的pH值:
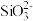 为8,
为8, 为5.5。
为5.5。回答下列问题:
(1)为了提高“碱浸”效率应采用的措施是
(2)“滤液1”中含有NaGaO2等溶质, “碱浸”时反应的离子方程式为
(3)通CO2两次调pH的原因是
(4)“操作a”为
(5)“电解”时阴极的电极反应为
(6)制备GaN时,参与反应的氧化剂与还原剂的物质的量之比为
(7)取m克GaN样品溶于足量的热NaOH溶液(GaN+OH- +H2O =
 +NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
+NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
您最近一年使用:0次



