回答下列问题:
(1)元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有___________ 种。
(2)下列微粒中的键角由大到小的顺序为___________ (填序号)。
① ②
② ③
③ ④
④
(3)基态Ni原子核外电子排布式为___________ 。F、K和Ni三种元素组成的一种化合物的晶胞如下图所示,该物质的化学式为___________ 。

(4)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电;
①CuF的熔点比CuCl的高,其原因是___________ 。
②比较Cu、Zn的第二电离能的大小: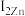
___________ 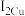 (填“>”或“<”)。
(填“>”或“<”)。
(5)在硫酸铜溶液中加入氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色的溶液,此蓝色沉淀溶解的离子方程式为:___________ 。
(6) 的晶胞如图所示,密度为
的晶胞如图所示,密度为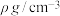 ,相邻的两个
,相邻的两个 的最近核间距为acm,则
的最近核间距为acm,则 的摩尔质量为
的摩尔质量为___________ g/mol(列出代数式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

(1)元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有
(2)下列微粒中的键角由大到小的顺序为
①
 ②
② ③
③ ④
④
(3)基态Ni原子核外电子排布式为

(4)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电;
①CuF的熔点比CuCl的高,其原因是
②比较Cu、Zn的第二电离能的大小:
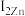
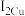 (填“>”或“<”)。
(填“>”或“<”)。(5)在硫酸铜溶液中加入氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色的溶液,此蓝色沉淀溶解的离子方程式为:
(6)
 的晶胞如图所示,密度为
的晶胞如图所示,密度为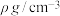 ,相邻的两个
,相邻的两个 的最近核间距为acm,则
的最近核间距为acm,则 的摩尔质量为
的摩尔质量为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
更新时间:2023-10-13 14:05:43
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有 A、B、C、D、E、F、G、H 八种元素,均为前四周期元素,它们的原子序数依次增大。 请根据下列相关信息,回答有关问题。
A 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素
B 元素是形成化合物种类最多的元素
C 元素基态原子的核外 p 电子数比 s 电子数少 1
D 元素基态原子的核外 p 轨道中有两个未成对电子
E 元素的气态基态原子的第一至第四电离能分别是 I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol
F 元素的主族序数与周期数的差为 4
G 元素是前四周期中电负性最小的元素
H 元素位于元素周期表中的第八纵行
(1)C2A4的电子式为__________ (A、C 为字母代号,请将字母代号用元素符号表示,下同)。
(2)B 元素的原子核外共有__________ 种不同运动状态的电子。
(3)某同学推断 E 元素基态原子的核外电子排布图为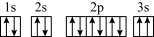 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了_________ ,该元素原子的 I3远远大于 I2,其原因是____________________ 。
(4)D、E、F 三种元素的简单离子半径由大到小的顺序是__________ (用离子符号表示)。
(5)用惰性电极电解 EF2的水溶液的离子方程式为__________ 。
(6)H 位于元素周期表中__________ 区(按电子排布分区),其基态原子的价电子排布式为_________ ,实验室用一种黄色溶液检验 H2+时产生蓝色沉淀,该反应的离子方程式为____________________ 。
A 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素
B 元素是形成化合物种类最多的元素
C 元素基态原子的核外 p 电子数比 s 电子数少 1
D 元素基态原子的核外 p 轨道中有两个未成对电子
E 元素的气态基态原子的第一至第四电离能分别是 I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol
F 元素的主族序数与周期数的差为 4
G 元素是前四周期中电负性最小的元素
H 元素位于元素周期表中的第八纵行
(1)C2A4的电子式为
(2)B 元素的原子核外共有
(3)某同学推断 E 元素基态原子的核外电子排布图为
 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了(4)D、E、F 三种元素的简单离子半径由大到小的顺序是
(5)用惰性电极电解 EF2的水溶液的离子方程式为
(6)H 位于元素周期表中
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:

回答下列问题:
(1)基态钛原子的价电子排布图为______________ ,其原子核外共有________ 种运动状态不相同的电子。金属钛晶胞如下图1所示,为_______________ 堆积(填堆积方式)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l >> l-b > b-b(l为孤对电子对,b为键合电子对),则关于H2O中的H-O-H键角可得出的结论是________ 。
(3)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃,可知TiCl4为________ 晶体。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是____________ 。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为___________ 。
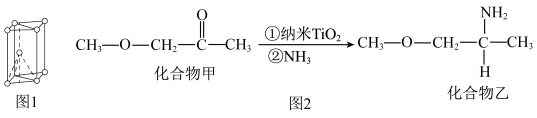
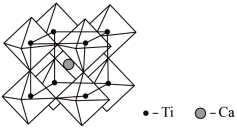
(5)钙钛矿晶体的结构如右图所示。钛离子位于立方晶胞的角顶,被________ 个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被________ 个氧离子包围。钙钛矿晶体的化学式为________________ 。若该晶胞的边长为a pm,则钙钛矿晶体的密度为______ g.cm-3(只要求列算式,不必计算出数值)。

回答下列问题:
(1)基态钛原子的价电子排布图为
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l >> l-b > b-b(l为孤对电子对,b为键合电子对),则关于H2O中的H-O-H键角可得出的结论是
| A.180° | B.接近120°,但小于120° |
| C.接近120°,但大于120° | D.接近109°28’,但小于109°28’ |
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是

(5)钙钛矿晶体的结构如右图所示。钛离子位于立方晶胞的角顶,被

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】M、N、X、Y、Z、W、R是原子序数依次增大的前四周期元素,基态N原子的最外层电子数是电子层数的2倍,W是电负性最小的短周期主族元素,基态R原子含有4个未成对电子,其中5种元素形成的一种阳离子结构如图所示。
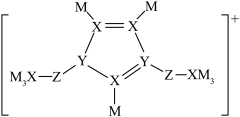
回答下列问题:
(1)基态X原子的价电子排布图为_______ ;与Y同周期且第一电离能大于Y的元素有_______ 种。
(2)M、X形成两种离子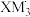 、
、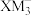 ,键角:
,键角: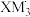
_______ 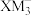 (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是_______ 。
(3)R的一种配合物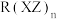 的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应:
的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应: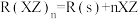 。
。
①
_______ 。
②该配合物中 键与
键与 键的数目之比为
键的数目之比为_______ 。
③反应过程中断裂的化学键只有配位键,形成的化学键是_______ 。
(4)在超高压下,W与N可形成化合物 ,
, (小圆球)按简单立方排布,形成
(小圆球)按简单立方排布,形成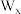 立方体空隙(如下图所示),电子对
立方体空隙(如下图所示),电子对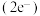 和N原子交替分布填充在立方体的中心。
和N原子交替分布填充在立方体的中心。
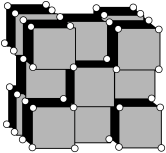

_______ ,晶体中 配位的N原子数为
配位的N原子数为_______ ;晶胞中W和N的最短距离为dnm, 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为_______  。
。

回答下列问题:
(1)基态X原子的价电子排布图为
(2)M、X形成两种离子
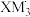 、
、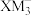 ,键角:
,键角: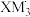
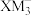 (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是(3)R的一种配合物
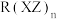 的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应:
的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应: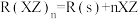 。
。①

②该配合物中
 键与
键与 键的数目之比为
键的数目之比为③反应过程中断裂的化学键只有配位键,形成的化学键是
(4)在超高压下,W与N可形成化合物
 ,
, (小圆球)按简单立方排布,形成
(小圆球)按简单立方排布,形成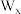 立方体空隙(如下图所示),电子对
立方体空隙(如下图所示),电子对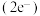 和N原子交替分布填充在立方体的中心。
和N原子交替分布填充在立方体的中心。

 配位的N原子数为
配位的N原子数为 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】 、
、 、
、 均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态 原子的价电子排布式为
原子的价电子排布式为___________ ,基态 、
、 、
、 原子的轨道中未成对电子数目最多的是
原子的轨道中未成对电子数目最多的是___________ (填元素符号)。
(2)一种 的配离子
的配离子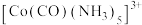 中,
中, 的配位数是
的配位数是___________ ,设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 该配离子中所含
该配离子中所含 键的数目为
键的数目为___________ 。
(3)在 催化下,烯烃、炔烃、醛可与
催化下,烯烃、炔烃、醛可与 发生加成反应。如①
发生加成反应。如① ;②
;② ;③
;③ ;④
;④ 。其中碳原子采取
。其中碳原子采取 杂化的分子有
杂化的分子有___________ (填物质序号), 分子的空间构型为
分子的空间构型为___________ 。
(4)铁氰化钾 是检验
是检验 的重要试剂。
的重要试剂。
①铁氰化钾中,其组成元素的第一电离能由大到小的顺序为_____ (用元素符号表示)。
②铁氰化钾中,存在的化学键为_____ (填标号)。
A.离子键 B. 键 C.
键 C. 键 D.分子间作用力 E.金属键
键 D.分子间作用力 E.金属键
(5)一种 合金的立方晶胞如图所示,其沿x轴、y轴、z轴的投影完全相同。
合金的立方晶胞如图所示,其沿x轴、y轴、z轴的投影完全相同。
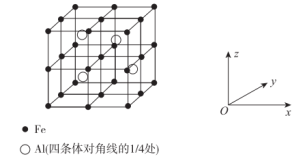
该合金的化学式可表示为_____ 。若此合金中最近的两个 原子核中心之间的距离为
原子核中心之间的距离为 ,则此合金的密度
,则此合金的密度
___________  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 )
)
 、
、 、
、 均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。(1)基态
 原子的价电子排布式为
原子的价电子排布式为 、
、 、
、 原子的轨道中未成对电子数目最多的是
原子的轨道中未成对电子数目最多的是(2)一种
 的配离子
的配离子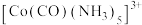 中,
中, 的配位数是
的配位数是 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 该配离子中所含
该配离子中所含 键的数目为
键的数目为(3)在
 催化下,烯烃、炔烃、醛可与
催化下,烯烃、炔烃、醛可与 发生加成反应。如①
发生加成反应。如① ;②
;② ;③
;③ ;④
;④ 。其中碳原子采取
。其中碳原子采取 杂化的分子有
杂化的分子有 分子的空间构型为
分子的空间构型为(4)铁氰化钾
 是检验
是检验 的重要试剂。
的重要试剂。①铁氰化钾中,其组成元素的第一电离能由大到小的顺序为
②铁氰化钾中,存在的化学键为
A.离子键 B.
 键 C.
键 C. 键 D.分子间作用力 E.金属键
键 D.分子间作用力 E.金属键(5)一种
 合金的立方晶胞如图所示,其沿x轴、y轴、z轴的投影完全相同。
合金的立方晶胞如图所示,其沿x轴、y轴、z轴的投影完全相同。
该合金的化学式可表示为
 原子核中心之间的距离为
原子核中心之间的距离为 ,则此合金的密度
,则此合金的密度
 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 )
)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过____________ 方法区分晶体、准晶体和非晶体。
(2)基态铜原子价层电子排布图为______ 。
(3)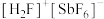 (氟锑酸)是一种超强酸,存在
(氟锑酸)是一种超强酸,存在 ,该离子的空间构型为
,该离子的空间构型为______ ,与 具有相同空间构型和成键方式的分子和阴离子分别是
具有相同空间构型和成键方式的分子和阴离子分别是______ (各举一例)。
(4) (氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。
(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。 中中心原子的杂化类型是
中中心原子的杂化类型是______ ;氟化铵中存在______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
(5) 被广泛用作高压电气设备的绝缘介质。
被广泛用作高压电气设备的绝缘介质。 是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则
是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则 键的键能为
键的键能为______ kJ·mol ,
, 键的键能为
键的键能为______ kJ·mol 。
。 。
。
①CuF的熔点比CuCl的高,原因是____________ 。
②已知 为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数
为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数
______ nm(列出计算式)。
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态铜原子价层电子排布图为
(3)
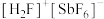 (氟锑酸)是一种超强酸,存在
(氟锑酸)是一种超强酸,存在 ,该离子的空间构型为
,该离子的空间构型为 具有相同空间构型和成键方式的分子和阴离子分别是
具有相同空间构型和成键方式的分子和阴离子分别是(4)
 (氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。
(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。 中中心原子的杂化类型是
中中心原子的杂化类型是A.离子键 B.σ键 C.π键 D.氢键
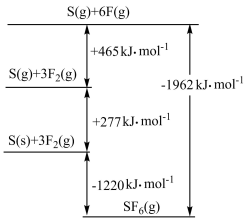
(5)
 被广泛用作高压电气设备的绝缘介质。
被广泛用作高压电气设备的绝缘介质。 是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则
是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 。
。
 。
。①CuF的熔点比CuCl的高,原因是
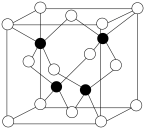
②已知
 为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数
为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硼化合物在工农业和医药方面用途广泛。请回答:
(1) B(OH)3分子的空间结构(以B为中心)名称是_______ ,硼原子的杂化轨道类型是_______ 。B(OH)3的水溶液呈酸性的原因是_______
(2)Li、Be、B在元素周期表上处于相邻位置,正确的是_______。
(3)B与La形成的某化合物晶体结构如下图。立方体的每一个顶点上都有一个由硼原子框架形成的八面体,八面体又以顶点互相连接。该化合物的化学式为_______ ,该晶体中La的配位数是_______ 。

(1) B(OH)3分子的空间结构(以B为中心)名称是
(2)Li、Be、B在元素周期表上处于相邻位置,正确的是_______。
A.基态原子半径: | B.电负性: |
C.第一电离能: | D.第二电离能: |

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。汽车尾气中含有害的一氧化碳和一氧化氮,利用钯(Pd)等金属作催化剂可以迅速将二者转化为无害的二氧化碳和氮气。
(1)钯与镍位于同列,且在镍的下一周期,钯在元素周期表的位置是__ ,基态镍原子的价电子的电子排布图为__ 。
(2)C、N、O的第一电离能由大到小的顺序为__ 。
(3)SO2分子的VSEPR构型为__ ;SO3分子中心原子的杂化形式为__ ;N2O与CO2互为等电子体,且N2O分子中O只与一个N相连,N2O的空间构型为_ ,分子中的σ键和π键数目之比是__ 。
(4)大π键是3个或3个以上原子彼此平行的p轨道从侧面相互重叠形成的π键。一氧化氮分子中,氮与氧之间形成一个σ键、一个2电子π键与一个3电子π键,则3电子π键__ (填“是”或“不是”)大π键;一氧化氮可与Fe2+生成棕色[Fe(H2O)5NO]2+离子,为检验亚铁离子的反应之一,[Fe(H2O)5NO]2+离子中配位体是__ 。
(5)CO可形成熔点为-20℃,沸点为103℃的配合物Fe(CO)5,Fe(CO)5分子中铁元素的化合价为___ ,属于__ 晶体。

(6)钯晶体的晶胞如图,晶胞的边长为apm,NA表示阿伏加 德罗常数的值,则钯单质的密度为___ g/cm3(列出计算式)。
(1)钯与镍位于同列,且在镍的下一周期,钯在元素周期表的位置是
(2)C、N、O的第一电离能由大到小的顺序为
(3)SO2分子的VSEPR构型为
(4)大π键是3个或3个以上原子彼此平行的p轨道从侧面相互重叠形成的π键。一氧化氮分子中,氮与氧之间形成一个σ键、一个2电子π键与一个3电子π键,则3电子π键
(5)CO可形成熔点为-20℃,沸点为103℃的配合物Fe(CO)5,Fe(CO)5分子中铁元素的化合价为

(6)钯晶体的晶胞如图,晶胞的边长为apm,NA表示阿伏加 德罗常数的值,则钯单质的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素。A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子。
(1)基态的F3+核外电子排布式是____________________________________________ 。
(2)B的气态氢化物在水中的溶解度远大于A、C的气态氢化物,原因是______________ 。
(3)化合物FD3是棕色固体、易潮解、100 ℃左右时升华,它的晶体类型是______________ ;化合物ECAB中的阴离子与AC2互为等电子体,该阴离子的电子式是____________________ 。
(4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是______________________________________________________________ 。
(5)化合物EF[F(AB)6]是一种蓝色晶体,下图表示其晶胞的 (E+未画出)。该蓝色晶体的一个晶胞中E+的个数为
(E+未画出)。该蓝色晶体的一个晶胞中E+的个数为________ 。

(1)基态的F3+核外电子排布式是
(2)B的气态氢化物在水中的溶解度远大于A、C的气态氢化物,原因是
(3)化合物FD3是棕色固体、易潮解、100 ℃左右时升华,它的晶体类型是
(4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是
(5)化合物EF[F(AB)6]是一种蓝色晶体,下图表示其晶胞的
 (E+未画出)。该蓝色晶体的一个晶胞中E+的个数为
(E+未画出)。该蓝色晶体的一个晶胞中E+的个数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答下列问题:
(1)基态Cu+核外电子排布式为_______ ;基态O原子未成对电子有_______ 个。
(2) 离子的VSEPR模型为
离子的VSEPR模型为_______ ,写出 离子的一种等电子体
离子的一种等电子体_______ 。从分于结构角度分析,HNO3酸性强于HNO2的原因是_______ 。
(3) 是一种叠氮一炔基Husigen环加成反应产物,该分子中N原子的杂化方式为
是一种叠氮一炔基Husigen环加成反应产物,该分子中N原子的杂化方式为_______ 。
(4)NH3分子中H-N-H键角为107°。如图是[Zn(NH3)6]2+的部分结构以及H-N-H键角的测量值。解释NH3形成[Zn(NH3)6]2+后H-N-H键角变大的原因:_______ 。

(5)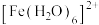 与
与 反应生成的
反应生成的 中,
中, 以
以 原子与
原子与 形成配位键。请在
形成配位键。请在 结构示意图的相应位置补填缺少的配体
结构示意图的相应位置补填缺少的配体_______ 。

(1)基态Cu+核外电子排布式为
(2)
 离子的VSEPR模型为
离子的VSEPR模型为 离子的一种等电子体
离子的一种等电子体(3)
 是一种叠氮一炔基Husigen环加成反应产物,该分子中N原子的杂化方式为
是一种叠氮一炔基Husigen环加成反应产物,该分子中N原子的杂化方式为(4)NH3分子中H-N-H键角为107°。如图是[Zn(NH3)6]2+的部分结构以及H-N-H键角的测量值。解释NH3形成[Zn(NH3)6]2+后H-N-H键角变大的原因:

(5)
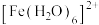 与
与 反应生成的
反应生成的 中,
中, 以
以 原子与
原子与 形成配位键。请在
形成配位键。请在 结构示意图的相应位置补填缺少的配体
结构示意图的相应位置补填缺少的配体
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】三草酸合铁酸钾: 是制备铁触媒的主要原料,在光照下能分解:
是制备铁触媒的主要原料,在光照下能分解: 。回答下列问题:
。回答下列问题:
(1)基态Fe原子的价电子排布式为_______ 。
(2)三草酸合铁酸钾所含有的元素中,电负性最大的是_______ (填元素符号,下同),该元素所在的周期中,第一电离能比它大的所有元素为_______ 。
(3) 分子中σ键和π键的个数比为
分子中σ键和π键的个数比为_______ ,C原子的杂化方式为_______ 。 分子的立体构型为
分子的立体构型为_______ 。
(4)金刚石的晶胞结构如图所示,碳原子分别位于顶点、面心和体内。

①若图中原子A的坐标为(0,0,0),原子B的坐标为(1,0,0),则原子C的坐标为_______ 。
②若金刚石的晶胞边长为apm,则其中碳碳键的键长d=_______ (用含a的代数式表示)pm。
(5)铁有δ、γ、α三种同素异形体(如图),三种晶体在不同温度下能发生转化。

①δ-Fe晶胞与γ-Fe晶体晶胞中铁原子的配位数之比为_______ 。
②若δ-Fe晶胞边长为ncm,α-Pe晶胞边长为mcm,则两种晶胞空间利用率之比为_______ 。(用含n、m的代数式表示)
 是制备铁触媒的主要原料,在光照下能分解:
是制备铁触媒的主要原料,在光照下能分解: 。回答下列问题:
。回答下列问题:(1)基态Fe原子的价电子排布式为
(2)三草酸合铁酸钾所含有的元素中,电负性最大的是
(3)
 分子中σ键和π键的个数比为
分子中σ键和π键的个数比为 分子的立体构型为
分子的立体构型为(4)金刚石的晶胞结构如图所示,碳原子分别位于顶点、面心和体内。

①若图中原子A的坐标为(0,0,0),原子B的坐标为(1,0,0),则原子C的坐标为
②若金刚石的晶胞边长为apm,则其中碳碳键的键长d=
(5)铁有δ、γ、α三种同素异形体(如图),三种晶体在不同温度下能发生转化。

①δ-Fe晶胞与γ-Fe晶体晶胞中铁原子的配位数之比为
②若δ-Fe晶胞边长为ncm,α-Pe晶胞边长为mcm,则两种晶胞空间利用率之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Fe、Co、Ni是第四周期重要的金属元素,回答下列问题:
(1)基态 的价电子排布图为
的价电子排布图为_______ 。镍易形成 配合物,其熔点为-19.3℃,沸点为43℃,则其晶体类型是
配合物,其熔点为-19.3℃,沸点为43℃,则其晶体类型是_______ ,该配合物中三种元素电负性由大到小的顺序为_______ 。
(2)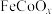 是一种新型光电催化剂,第四电离能大小关系是
是一种新型光电催化剂,第四电离能大小关系是
_______ 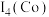 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是_______ 。
(3)二茂铁是一种具有芳香族性质的有机过渡金属化合物,其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。环戊二烯( )可用于制备二茂铁。
)可用于制备二茂铁。
①环戊二烯中碳原子的杂化方式为_______ 。
②1 mol环戊二烯中有_______ mol  键。
键。
(4) 晶体的晶胞如图甲所示。已知晶胞边长为a nm,阿伏加德罗常数的值为
晶体的晶胞如图甲所示。已知晶胞边长为a nm,阿伏加德罗常数的值为 ,该晶胞中
,该晶胞中 位于
位于 所形成的正八面体的体心,则晶胞密度为
所形成的正八面体的体心,则晶胞密度为_______  。
。
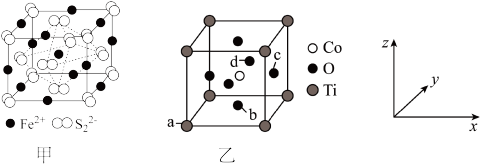
(5)钴的一种化合物晶胞结构如乙图所示。
已知a点的原子坐标参数为 ,b点为
,b点为 ,c点为
,c点为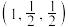 ,则d点的原子坐标参数为
,则d点的原子坐标参数为_______ 。
(1)基态
 的价电子排布图为
的价电子排布图为 配合物,其熔点为-19.3℃,沸点为43℃,则其晶体类型是
配合物,其熔点为-19.3℃,沸点为43℃,则其晶体类型是(2)
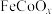 是一种新型光电催化剂,第四电离能大小关系是
是一种新型光电催化剂,第四电离能大小关系是
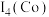 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(3)二茂铁是一种具有芳香族性质的有机过渡金属化合物,其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。环戊二烯(
 )可用于制备二茂铁。
)可用于制备二茂铁。①环戊二烯中碳原子的杂化方式为
②1 mol环戊二烯中有
 键。
键。(4)
 晶体的晶胞如图甲所示。已知晶胞边长为a nm,阿伏加德罗常数的值为
晶体的晶胞如图甲所示。已知晶胞边长为a nm,阿伏加德罗常数的值为 ,该晶胞中
,该晶胞中 位于
位于 所形成的正八面体的体心,则晶胞密度为
所形成的正八面体的体心,则晶胞密度为 。
。
(5)钴的一种化合物晶胞结构如乙图所示。
已知a点的原子坐标参数为
 ,b点为
,b点为 ,c点为
,c点为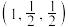 ,则d点的原子坐标参数为
,则d点的原子坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氢气热值大,无污染,被誉为“世界最清洁的能源”,氢气的储存是氢能利用的热点问题。
(1)氨硼烷(NH3BH3)含氢量高、热稳定性好,是具有潜力的固体储氢材料。
①氨硼烷分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),H、B、N三种元素的电负性由大到小的顺序是_______ 。
②NH3BH3的熔点比CH3CH3_______ (填“高”或“低”),原因是在NH3BH3分子之间,存在_______ ,也称“双氢键”。
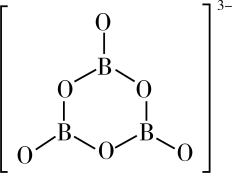
③氨硼烷在催化剂作用下水解释放氢气3NH3BH3+6H2O=3 +
+ +9H2,
+9H2, 的结构如图所示,
的结构如图所示, 离子中B原子的杂化轨道类型为
离子中B原子的杂化轨道类型为_______ 。
(2)氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢,其晶胞结构如图所示,为长方体。
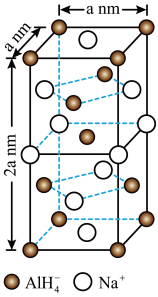
①NaAlH4晶体中, 的配位数为
的配位数为_______ 。
②设NA为阿伏加德罗常数的值,NaAlH4晶体的密度为_______ g/cm3(列出表达式)。
③NaAlH4的释氢机理为:每3个 中,有2个分别放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构。这种结构变化由表面层扩展到整个晶体,从而释放出氢气。该释氢过程可用化学方程式表示为
中,有2个分别放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构。这种结构变化由表面层扩展到整个晶体,从而释放出氢气。该释氢过程可用化学方程式表示为_______ 。
④金属氢化物是应用广泛的还原剂。KH的还原性比NaH的强。原因是_______ 。
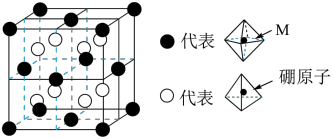
(3)某种新型储氢材料的晶胞如图所示,八面体中心为M金属离子,顶点均为NH3配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为188 g·mol-1,则在该化合物中,M离子的最外层电子排布式为_______ 。
(1)氨硼烷(NH3BH3)含氢量高、热稳定性好,是具有潜力的固体储氢材料。
①氨硼烷分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),H、B、N三种元素的电负性由大到小的顺序是
②NH3BH3的熔点比CH3CH3
③氨硼烷在催化剂作用下水解释放氢气3NH3BH3+6H2O=3
 +
+ +9H2,
+9H2, 的结构如图所示,
的结构如图所示, 离子中B原子的杂化轨道类型为
离子中B原子的杂化轨道类型为
(2)氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢,其晶胞结构如图所示,为长方体。

①NaAlH4晶体中,
 的配位数为
的配位数为②设NA为阿伏加德罗常数的值,NaAlH4晶体的密度为
③NaAlH4的释氢机理为:每3个
 中,有2个分别放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构。这种结构变化由表面层扩展到整个晶体,从而释放出氢气。该释氢过程可用化学方程式表示为
中,有2个分别放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构。这种结构变化由表面层扩展到整个晶体,从而释放出氢气。该释氢过程可用化学方程式表示为④金属氢化物是应用广泛的还原剂。KH的还原性比NaH的强。原因是
(3)某种新型储氢材料的晶胞如图所示,八面体中心为M金属离子,顶点均为NH3配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为188 g·mol-1,则在该化合物中,M离子的最外层电子排布式为

您最近一年使用:0次



