高铁酸钾(K2FeO4)是一种新型、高效、无毒的水处理剂。工业上,利用廉价的铁黄(FeOOH)等为原料制备高铁酸钾。工艺流程如图:
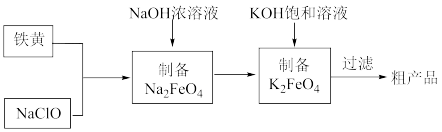
下列说法错误的是

下列说法错误的是
| A.高铁酸钾在水处理过程中涉及氧化还原反应和盐类水解反应 |
| B.制备Na2FeO4反应中氧化剂和还原剂的物质的量之比为2∶3 |
| C.根据流程可以判断相同温度下K2FeO4的溶解度小于Na2FeO4 |
| D.若通过电解法以铁为原料制备高铁酸钾,铁棒应该做阳极 |
2024·广西·一模 查看更多[5]
广西部分高中2024届高三第一次摸底测试化学试题广西南宁市2024届高三上学期毕业班摸底测试化学试题福建省厦门外国语学校2023-2024学年高二上学期期末模拟考试化学试题(已下线)选择题6-10(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
更新时间:2023-10-27 22:40:39
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】世界卫生组织(WHO)和中国卫健委公认二氧化氯(ClO2)为新时代绿色消毒剂。常温下,ClO2气体与Cl2具有相似的颜色与气味,易溶于水,在水中的溶解度是Cl2的5~8倍。ClO2对热、震动、撞击和摩擦相当敏感,极易分解发生爆炸。ClO2几乎不与冷水反应,遇热水则会分解。经研究表明,ClO2反应释放出的原子氧可以氧化色素,所以ClO2也是优良的漂白剂。工业上可采用SO2与氯酸钠在酸性条件下反应制取ClO2,并生成NaHSO4,相信在不久的将来,ClO2将广泛应用到杀菌消毒领域。实验室可通过下列反应制取ClO2:2KClO3+H2C2O4+H2SO4═2ClO2↑+2CO2↑+K2SO4+2H2O。下列说法不正确的是
| A.ClO2是优良的漂白剂是因为具有强氧化性 |
| B.生成1molClO2有2mol电子发生转移 |
| C.一般可用冰水吸收ClO2气体,形成ClO2溶液 |
| D.工业上制取ClO2过程中,参加反应的氧化剂和还原剂物质的量之比为2:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】亚氯酸钠(NaClO2) 是一种高效漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氧酸钠的流程如下:

下列说法错误的是

下列说法错误的是
| A.反应①中NaClO3是氧化剂,SO2是还原剂 |
| B.若反应①通过原电池来实现,则SO2应该在负极发生反应 |
| C.反应②条件下,ClO2的氧化性大于H2O2 |
| D.反应②中的H2O2可用NaClO4代替 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关实验操作、现象、解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 用铂丝蘸取某待测液在酒精灯外焰上灼烧 | 火焰呈黄色 | 待测液不含钾元素 |
| B | AgBr沉淀中滴入KCl溶液 | 有白色沉淀出现 | AgCl比AgBr更难溶 |
| C | 铁丝插入稀硝酸中 | 有无色气体产生 | 生成氢气 |
| D | 向NaCN溶液中滴加无色酚酞试液 | 溶液变红 | HCN是弱电解质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是| A.3g 3He含有的电子数为NA |
B. mol CO2的体积是2.24L mol CO2的体积是2.24L |
C.1 L 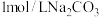 溶液中含阴阳离子总数小于 溶液中含阴阳离子总数小于 |
D. g金属钠与过量的氧气反应,无论加热与否转移电子数均为 g金属钠与过量的氧气反应,无论加热与否转移电子数均为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】由于锂电池的需求急剧增长,全球陷入锂资源“争夺战”。而海水是一个巨大的资源宝库,科研人员利用电解原理富集海水中的锂离子,其原理如图所示(a、b均为惰性电极),下列有关说法正确的是


| A.a电极为阴极,发生氧化反应 |
| B.b电极反应式为2H++2e-=H2↑ |
| C.一段时间后,b电极附近溶液的pH降低 |
| D.当有1molLi+通过交换膜,b电极产生35.5克气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用惰性电极电解下列溶液,一段时间后,再加入一定量的另一种物质(括号内物质),电解质溶液基本不变的是
| A.CuCl2(CuSO4) | B.NaOH(H2O) | C.NaCl(NaCl) | D.CuSO4[Cu(OH)2] |
您最近一年使用:0次

 等气体,使应用受限。
等气体,使应用受限。 菌在酸性
菌在酸性 溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为
溶液中可实现天然气的催化脱硫,其原理如图所示,总反应方程式为 。下列说法正确的是
。下列说法正确的是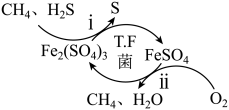
 ”生成的
”生成的 和
和 物质的量之比为
物质的量之比为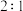
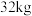 硫,则消耗
硫,则消耗
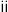 ”发生的反应为
”发生的反应为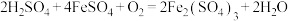
 用于净水
用于净水 制取无水
制取无水 固体时,需在
固体时,需在 气流中蒸发
气流中蒸发 ,出现白色浑浊:
,出现白色浑浊: