NH3发生催化氧化反应生成NO,实验室也可以使用铜和稀硝酸制备少量NO。NH3在强碱条件下能被NaClO氧化生成N2H4;N2H4可被NaClO继续氧化生成N2,也可被HNO2氧化生成HN3,N2H4能与AgNO3溶液反应产生银镜;HN3是一种弱酸,酸性与醋酸相当。CO可将机动车尾气中的NO转化为N2,反应为: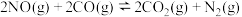 ,ΔH=-746.5kJ·mol-1下列说法正确的是
,ΔH=-746.5kJ·mol-1下列说法正确的是
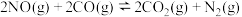 ,ΔH=-746.5kJ·mol-1下列说法正确的是
,ΔH=-746.5kJ·mol-1下列说法正确的是| A.该反应在任何条件下都能自发进行 |
B.反应的平衡常数可表示为 |
| C.使用高效的催化剂可以降低反应的焓变 |
D.其它条件不变,增大 的值,NO的转化率下降 的值,NO的转化率下降 |
更新时间:2023-09-24 11:44:10
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是
| A.在25℃、101 kPa,1 mol CH4(g)和2 mol CH4(g)的燃烧热相等 |
| B.1 mol浓硫酸与1 mol NaOH溶液完全中和所放出的热量为中和热 |
| C.工业合成氨的反应中加入催化剂可增大反应速率,同时提高反应物的平衡转化率 |
| D.△H越大,说明反应热量变化越大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列与化学反应能量变化相关的叙述正确的是
| A.焓变是指1mol物质参加反应时的能量变化 |
| B.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
C.在一个化学反应中,当反应物总焓小于生成物的总焓时, 为负值 为负值 |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列关于工业合成氨的叙述错误的是
| A.在动力、设备,材料允许的情况下,反应尽可能在高压下进行 |
| B.温度越高越有利于工业合成氨 |
| C.在工业合成氨中,N2、H2的循环利用可降低成本 |
| D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】向恒温恒容密闭容器中通入 和
和 ,一定条件下反应
,一定条件下反应 达到平衡后,再通入一定量的
达到平衡后,再通入一定量的 ,再次达到新平衡。下列有关判断正确的是
,再次达到新平衡。下列有关判断正确的是
 和
和 ,一定条件下反应
,一定条件下反应 达到平衡后,再通入一定量的
达到平衡后,再通入一定量的 ,再次达到新平衡。下列有关判断正确的是
,再次达到新平衡。下列有关判断正确的是A.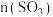 始终不变 始终不变 | B.反应平衡常数增大 |
| C.逆反应速率减小 | D. 的转化率增大 的转化率增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】对于反应2NO(g)+2CO(g)⇌2CO2(g)+N2(g) ΔH=-746.5kJ⋅mol﹣1,下列说法正确的是
| A.该反应在任何条件下都能自发进行 |
B.反应的平衡常数可表示为K=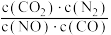 |
| C.使用高效的催化剂可以降低反应的焓变 |
D.其它条件不变,增大 的值,NO的转化率下降 的值,NO的转化率下降 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:
已知: ,
, ,其中
,其中 、
、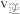 为正、逆反应速率,
为正、逆反应速率, 、
、 为正、逆反应速率常数,x为各组分的物质的量分数。已知平衡常数K,为各生成物的物质的量分数幂之积与各反应物的物质的量分数幂之积的比,则平衡常数
为正、逆反应速率常数,x为各组分的物质的量分数。已知平衡常数K,为各生成物的物质的量分数幂之积与各反应物的物质的量分数幂之积的比,则平衡常数 为( )
为( )

已知:
 ,
, ,其中
,其中 、
、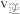 为正、逆反应速率,
为正、逆反应速率, 、
、 为正、逆反应速率常数,x为各组分的物质的量分数。已知平衡常数K,为各生成物的物质的量分数幂之积与各反应物的物质的量分数幂之积的比,则平衡常数
为正、逆反应速率常数,x为各组分的物质的量分数。已知平衡常数K,为各生成物的物质的量分数幂之积与各反应物的物质的量分数幂之积的比,则平衡常数 为( )
为( )A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在25 ℃,1.01×105Pa条件下,反应2N2O5(g)=4NO2(g)+O2(g) △H= +56.7kJ/mol能自发进行的合理解释是
| A.该反应是熵减反应 | B.该反应是分解反应 |
| C.该反应的焓变效应大于熵变效应 | D.该反应的熵变效应大于焓变效应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列说法不正确的是
| A.冰在室温下自动熔化成水,这是熵增过程 |
B.用 合成聚碳酸酯可降解塑料,实现“碳”的循环利用 合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
C.在 中 中 提供空轨道, 提供空轨道, 中N原子提供孤对电子 中N原子提供孤对电子 |
D.在25℃和101kPa时, 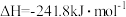 , , 的燃烧热为 的燃烧热为 |
您最近一年使用:0次



 ,则平衡时 NO的转化率升高
,则平衡时 NO的转化率升高

