二氧化氯消毒剂是国际上公认的高效消毒灭菌剂,回答下列问题:
I.制备ClO2
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
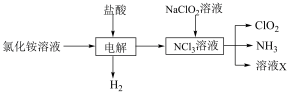
(1)NH4Cl的电子式为___________ 。
(2)若NaClO2与NCl3完全反应,则“溶液X”中的溶质为________ (填化学式)。
Ⅱ.NaClO2的应用
(3)NaClO2具有强氧化性,可将烟气中的NO氧化为NO ,在该反应过程中无有毒气体生成。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图所示。
,在该反应过程中无有毒气体生成。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图所示。
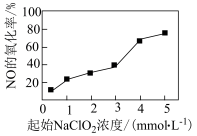
①NaClO2溶液在酸性条件下除去NO的离子方程式为___________ 。
②NO的氧化率随起始NaClO2浓度的增大而增大,原因是___________ 。
(4)ClO2具有较好的杀菌消毒作用。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。若ClO2的还原产物为Cl-,则ClO2的有效氯含量为___________ (保留2位小数)。
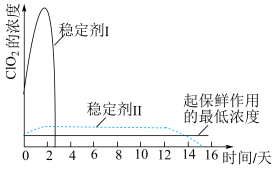
(5)ClO2能被多种稳定剂吸收,若将其用于果蔬保鲜,你认为下图中效果较好的稳定剂是___________ (填“稳定剂I”或“稳定剂Ⅱ”),原因是___________ 。
I.制备ClO2
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

(1)NH4Cl的电子式为
(2)若NaClO2与NCl3完全反应,则“溶液X”中的溶质为
Ⅱ.NaClO2的应用
(3)NaClO2具有强氧化性,可将烟气中的NO氧化为NO
 ,在该反应过程中无有毒气体生成。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图所示。
,在该反应过程中无有毒气体生成。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图所示。
①NaClO2溶液在酸性条件下除去NO的离子方程式为
②NO的氧化率随起始NaClO2浓度的增大而增大,原因是
(4)ClO2具有较好的杀菌消毒作用。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。若ClO2的还原产物为Cl-,则ClO2的有效氯含量为
(5)ClO2能被多种稳定剂吸收,若将其用于果蔬保鲜,你认为下图中效果较好的稳定剂是

更新时间:2023-11-04 08:59:38
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
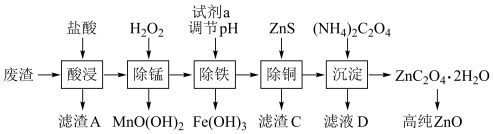
【推荐1】 可作为紫外线吸收剂应用于化妆品中.某工厂采用如图所示工艺处理工厂废渣(主要成分为
可作为紫外线吸收剂应用于化妆品中.某工厂采用如图所示工艺处理工厂废渣(主要成分为 ,另含少量
,另含少量 等)制取高纯
等)制取高纯 .回答下列问题:
.回答下列问题:
已知:①草酸 受热易分解生成
受热易分解生成 ;
;
②常温下: .
.
(1)提高酸浸速率的措施有____________________________________________________ (写一条即可).
(2)“滤渣A”的主要成分为___________ .
(3) 的电子式为
的电子式为___________ .
(4)试剂a为___________ ,“滤液D”中主要含有的离子有_______________________ .
(5)写出“除锰”中,生成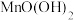 的离子方程式:
的离子方程式:______________________ .
(6)写出由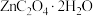 制得氧化锌的化学方程式:
制得氧化锌的化学方程式:______________________ .
(7)“除锰”后滤液中 ,“除铁”操作中可以调节
,“除铁”操作中可以调节 的范围是
的范围是___________ .
 可作为紫外线吸收剂应用于化妆品中.某工厂采用如图所示工艺处理工厂废渣(主要成分为
可作为紫外线吸收剂应用于化妆品中.某工厂采用如图所示工艺处理工厂废渣(主要成分为 ,另含少量
,另含少量 等)制取高纯
等)制取高纯 .回答下列问题:
.回答下列问题:
已知:①草酸
 受热易分解生成
受热易分解生成 ;
;②常温下:
 .
.(1)提高酸浸速率的措施有
(2)“滤渣A”的主要成分为
(3)
 的电子式为
的电子式为(4)试剂a为
(5)写出“除锰”中,生成
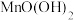 的离子方程式:
的离子方程式:(6)写出由
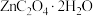 制得氧化锌的化学方程式:
制得氧化锌的化学方程式:(7)“除锰”后滤液中
 ,“除铁”操作中可以调节
,“除铁”操作中可以调节 的范围是
的范围是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D、E、F为原子序数依次增大的六种短周期主族元素。已知:A是宇宙中含量最高的元素;B、C形成的化合物是形成酸雨的主要物质;D、E、F为同周期元素,它们的最高价氧化物的水化物均可两两反应。用元素符号回答下列问题:
(1)元素C原子核内质子数比中子数少2个,满足该条件的原子符号为_______ ;元素E在周期中的位置:_______ 。
(2)若元素F的单质是一种黄绿色气体,常温时由F形成的最高价氧化物甲是一种液态物质,将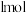 甲完全溶于水形成溶液时放出
甲完全溶于水形成溶液时放出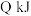 的热量,写出该过程的热化学反应方程式
的热量,写出该过程的热化学反应方程式_______ ;若元素F的单质是一种黄色固体,下列表述中能证明元素C的非金属性强于F的是_______ (填写序号)。
①元素C和F形成的化合物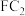 中,F化合价为
中,F化合价为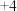 ,C化合价为
,C化合价为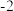
②元素C、F各自形成的最简单氢化物的沸点:前者>后者
③常温时,元素C的单质为气态,F的单质为固态
④元素C的单质可将F从其氢化物溶液中置换出来
(3)元素A、B可形成一种离子化合物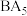 ,该化合物的电子式为
,该化合物的电子式为_______ 。
(4)用高能射线照射A、C形成的10电子分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的化学式_______ ,该阳离子存在的化学键类型有_______ 。
(5)写出元素D、E的最高价氧化物的水化物相互反应的离子方程式_______ 。
(1)元素C原子核内质子数比中子数少2个,满足该条件的原子符号为
(2)若元素F的单质是一种黄绿色气体,常温时由F形成的最高价氧化物甲是一种液态物质,将
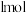 甲完全溶于水形成溶液时放出
甲完全溶于水形成溶液时放出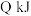 的热量,写出该过程的热化学反应方程式
的热量,写出该过程的热化学反应方程式①元素C和F形成的化合物
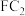 中,F化合价为
中,F化合价为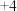 ,C化合价为
,C化合价为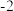
②元素C、F各自形成的最简单氢化物的沸点:前者>后者
③常温时,元素C的单质为气态,F的单质为固态
④元素C的单质可将F从其氢化物溶液中置换出来
(3)元素A、B可形成一种离子化合物
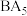 ,该化合物的电子式为
,该化合物的电子式为(4)用高能射线照射A、C形成的10电子分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的化学式
(5)写出元素D、E的最高价氧化物的水化物相互反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】汽车安全气囊是行车安全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气囊工作的化学原理,取安全装置中的固体粉末进行实验。经组成分析,确定该粉末仅含Na、Fe、N、O四种元素。水溶性实验表明,固体粉末部分溶解。经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸。取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72L。单质乙在高温、隔绝空气的条件下与红棕色不溶物粉末反应,生成氧化物丙和另一种单质。化合物丙与空气接触可转化为可溶性盐。请回答下列问题:
(1)甲的化学式为_______ ;丙的电子式为_______ 。
(2)单质乙与红棕色粉末发生反应的化学方程式为_______ ;安全气囊中红棕色粉末的作用是_______ 。
(3)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是_______ (填字母代号)。
(4)可溶性盐的成分可能是_______ ;请设计一个可行的简单实验方案,探究化合物丙与空气接触后生成可溶性盐的成分(不考虑结晶水合物),请简单叙述你的实验方案、原理:_______ 。
(1)甲的化学式为
(2)单质乙与红棕色粉末发生反应的化学方程式为
(3)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是_______ (填字母代号)。
| A.KCl | B.KNO3 | C.Na2S | D.CuO |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】利用某工厂废水(主要成分含有 、
、 、
、 ,及少量
,及少量 、
、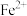 、
、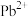 )制备
)制备 溶液的实验流程如下:
溶液的实验流程如下:

已知:①溶液中金属离子的浓度小于 时,可视为沉淀完全。
时,可视为沉淀完全。
②室温下 。
。
(1)①“氧化”步骤的离子方程式为___________ 。
②调节 的目的是
的目的是___________ 。
(2)流程中分两步除杂而不采用直接加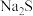 溶液除杂,除了减少
溶液除杂,除了减少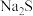 的使用量之外,还可能的原因是:
的使用量之外,还可能的原因是:___________ 。
(3)以 溶液为原料制备的
溶液为原料制备的 脱硫剂,可用于脱除煤气中的
脱硫剂,可用于脱除煤气中的 。
。
①400℃时,将一定比例 、
、 、
、 和
和 的混合气体以一定流速通过装有
的混合气体以一定流速通过装有 脱硫剂的硫化反应器。硫化过程中
脱硫剂的硫化反应器。硫化过程中 与
与 、
、 反应生成
反应生成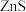 和
和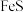 ,其化学方程式为
,其化学方程式为___________ 。
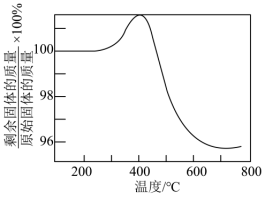
②将硫化后的固体在 (体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图所示。在280~400℃范围内,固体质量增加的主要原因是
(体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图所示。在280~400℃范围内,固体质量增加的主要原因是___________ 。
 、
、 、
、 ,及少量
,及少量 、
、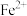 、
、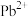 )制备
)制备 溶液的实验流程如下:
溶液的实验流程如下:
已知:①溶液中金属离子的浓度小于
 时,可视为沉淀完全。
时,可视为沉淀完全。②室温下
 。
。(1)①“氧化”步骤的离子方程式为
②调节
 的目的是
的目的是(2)流程中分两步除杂而不采用直接加
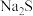 溶液除杂,除了减少
溶液除杂,除了减少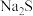 的使用量之外,还可能的原因是:
的使用量之外,还可能的原因是:(3)以
 溶液为原料制备的
溶液为原料制备的 脱硫剂,可用于脱除煤气中的
脱硫剂,可用于脱除煤气中的 。
。①400℃时,将一定比例
 、
、 、
、 和
和 的混合气体以一定流速通过装有
的混合气体以一定流速通过装有 脱硫剂的硫化反应器。硫化过程中
脱硫剂的硫化反应器。硫化过程中 与
与 、
、 反应生成
反应生成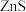 和
和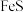 ,其化学方程式为
,其化学方程式为②将硫化后的固体在
 (体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图所示。在280~400℃范围内,固体质量增加的主要原因是
(体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图所示。在280~400℃范围内,固体质量增加的主要原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】半导体芯片行业是金属靶材的主要应用领域之一。利用镍铂靶材废料(主要成分为Ni、Pt以及微量Fe、Al的单质)采用选择性溶解法回收铂并制备硫酸镍晶体的一种工艺流程如下:

已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
②王水是按浓盐酸和浓硝酸的体积比为3∶1配制而成;
③氧化性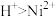
④室温: ;
;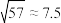
(1)“酸浸”时镍发生反应的化学方程式为_______ 。
(2)铂在王水中生成二元强酸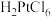 ,其中Pt元素的化合价为
,其中Pt元素的化合价为_______ ,该反应的离子方程式为_______ 。
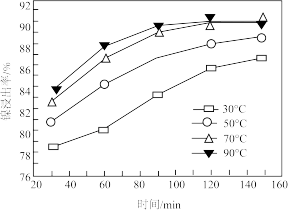
(3)设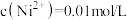 “调pH”应控制的pH范围是
“调pH”应控制的pH范围是_______ 。
(4)当液固比为4∶1时,"酸浸"过程中镍的浸出率与温度和时间的关系如图所示,“酸浸”的最佳温度和时间是_______ 。
(5)沉铂过程中, 的沉淀率随温度的升高而增大,结合平衡移动原理解释
的沉淀率随温度的升高而增大,结合平衡移动原理解释 沉淀率随温度变化的主要原因
沉淀率随温度变化的主要原因_______ 。
(6)在“沉铂”过程中,若向 的溶液里加入等体积的
的溶液里加入等体积的 溶液,使
溶液,使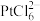 沉淀完全,则加入
沉淀完全,则加入 溶液的浓度最小值为
溶液的浓度最小值为_______ mol/L(结果保留两位小数,忽略溶液混合后体积的变化)。
(7)“操作1”中包括沉淀的洗涤,应选用下列哪种试剂最佳_______。

已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ |  |  |  |
| 开始沉淀时(c=0.01mol/L)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时 (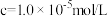 )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
③氧化性
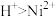
④室温:
 ;
;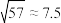
(1)“酸浸”时镍发生反应的化学方程式为
(2)铂在王水中生成二元强酸
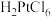 ,其中Pt元素的化合价为
,其中Pt元素的化合价为(3)设
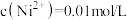 “调pH”应控制的pH范围是
“调pH”应控制的pH范围是(4)当液固比为4∶1时,"酸浸"过程中镍的浸出率与温度和时间的关系如图所示,“酸浸”的最佳温度和时间是

(5)沉铂过程中,
 的沉淀率随温度的升高而增大,结合平衡移动原理解释
的沉淀率随温度的升高而增大,结合平衡移动原理解释 沉淀率随温度变化的主要原因
沉淀率随温度变化的主要原因(6)在“沉铂”过程中,若向
 的溶液里加入等体积的
的溶液里加入等体积的 溶液,使
溶液,使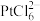 沉淀完全,则加入
沉淀完全,则加入 溶液的浓度最小值为
溶液的浓度最小值为(7)“操作1”中包括沉淀的洗涤,应选用下列哪种试剂最佳_______。
| A.蒸馏水 | B.浓盐酸 | C.氯化铵溶液 | D.王水 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】四氢铝钠( )是强还原剂和供氢剂,高铁酸钠(
)是强还原剂和供氢剂,高铁酸钠( )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为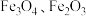 和
和 含少量
含少量 )为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:
)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题: 中氢的化合价为
中氢的化合价为______ 。
(2)浸渣的主要成分是______ (填化学式),其可作为制备玻璃的原料,写出盛放 溶液的试剂瓶不能用玻璃塞的原因
溶液的试剂瓶不能用玻璃塞的原因______ (用离子方程式表达);
(3)“转化”中 的具体作用是
的具体作用是_____ ,由 制备
制备 的离子方程式为
的离子方程式为_______ ;“分离”中铝元素转化成_______ (填离子符号)。
(4)“沉铝”时通入过量 发生反应的离子方程式为
发生反应的离子方程式为_______ ;所得滤液经蒸干、灼烧得到固体有______ (填化学式)。
(5)“合成”中乙醚作溶剂,发生反应的化学方程式为_______ 。
(6)“有效氢”指单位质量(1g)含氢还原剂的还原能力相当于多少克氢气的还原能力。 的“有效氢”
的“有效氢”_______ (保留三位有效数字)。(保留三位有效数字)。
 )是强还原剂和供氢剂,高铁酸钠(
)是强还原剂和供氢剂,高铁酸钠( )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为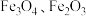 和
和 含少量
含少量 )为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:
)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题: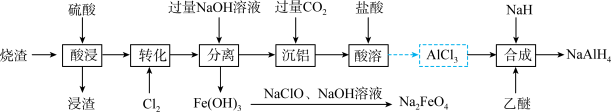
 中氢的化合价为
中氢的化合价为(2)浸渣的主要成分是
 溶液的试剂瓶不能用玻璃塞的原因
溶液的试剂瓶不能用玻璃塞的原因(3)“转化”中
 的具体作用是
的具体作用是 制备
制备 的离子方程式为
的离子方程式为(4)“沉铝”时通入过量
 发生反应的离子方程式为
发生反应的离子方程式为(5)“合成”中乙醚作溶剂,发生反应的化学方程式为
(6)“有效氢”指单位质量(1g)含氢还原剂的还原能力相当于多少克氢气的还原能力。
 的“有效氢”
的“有效氢”
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】根据当地资源等情况,硫酸工业常用黄铁矿(主要成分为FeS2)作为原料。完成下列填空:
(1)将0.050mol SO2(g) 和0.030mol O2(g) 充入一个2L的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)⇌2SO3(g)+Q。经2分钟反应达到平衡,测得n(SO3)=0.040mol,则O2的平均反应速率为______
(2)在容积不变时,下列措施中有利于提高SO2平衡转化率的有______ (选填编号)
a.移出氧气 b.降低温度
c.减小压强 d.再充入0.050molSO2(g)和0.030molO2(g)
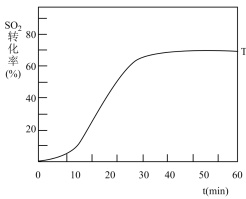
(3)在起始温度T1(673K)时SO2的转化率随反应时间(t)的变化如图,请在图中画出其他条件不变情况下,起始温度为T2(723K)时SO2的转化率随反应时间变化的示意图___
(4)黄铁矿在一定条件下煅烧的产物为SO2和Fe3O4
①将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需维持溶液有足够的酸性,其原因是______
②FeS2能将溶液中的Fe3+还原为Fe2+,本身被氧化为SO42﹣。写出有关的离子方程式______ 。有2mol氧化产物生成时转移的电子数为______
(1)将0.050mol SO2(g) 和0.030mol O2(g) 充入一个2L的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)⇌2SO3(g)+Q。经2分钟反应达到平衡,测得n(SO3)=0.040mol,则O2的平均反应速率为
(2)在容积不变时,下列措施中有利于提高SO2平衡转化率的有
a.移出氧气 b.降低温度
c.减小压强 d.再充入0.050molSO2(g)和0.030molO2(g)
(3)在起始温度T1(673K)时SO2的转化率随反应时间(t)的变化如图,请在图中画出其他条件不变情况下,起始温度为T2(723K)时SO2的转化率随反应时间变化的示意图

(4)黄铁矿在一定条件下煅烧的产物为SO2和Fe3O4
①将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需维持溶液有足够的酸性,其原因是
②FeS2能将溶液中的Fe3+还原为Fe2+,本身被氧化为SO42﹣。写出有关的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】亚铁氰化钾的化学式为K4Fe(CN)6,一种用含NaCN废水合成该化合物的主要工艺流程如下:
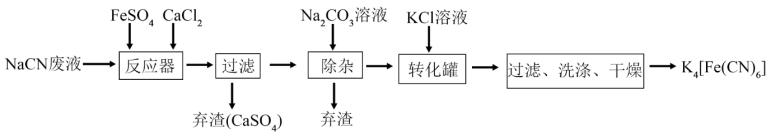
(1)请依据工艺流程图中的信息,回答下列问题:
①在“除杂”步骤中弃渣的主要成分为__________________ (填化学式)。
②在“反应器“中发生的主要反应的化学方程式为:________________________________ ;
③相同温度下溶解度:Na4[Fe(CN)6]________ K4[Fe(CN)6] (选填“>”、“<”或“=”)
(2)氰化钠(NaCN)是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。NaCN的电子式为__________________________ ;实验室用NaCN固体配制NaCN溶液时,应先将其溶于氢氧化钠溶液中,再用蒸馏水稀释。NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是______________________________________ 。
(3)已知:氢氰酸是一种有苦杏仁气味的无色剧毒液体,易挥发,25℃时,Ka(HCN)=6.25×10-10。
①处理含CN-废水的方法是:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5-8.5,用NaClO完全氧化OCN-生成N2和两种盐。
请写出第二步反应的离子方程式:_________________________________________ 。
②反应CN-+H2O HCN+OH-在25℃时的平衡常数K=
HCN+OH-在25℃时的平衡常数K=_____________ (填数值)。
(4)K4Fe(CN)6与高锰酸钾溶液反应,其方程式为:
K4Fe(CN)6+KMnO4 +H2SO4=KHSO4+Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平), 若有1mol K4Fe(CN)6被高锰酸钾氧化时,则消耗KMnO4的物质的量为________ mol。

(1)请依据工艺流程图中的信息,回答下列问题:
①在“除杂”步骤中弃渣的主要成分为
②在“反应器“中发生的主要反应的化学方程式为:
③相同温度下溶解度:Na4[Fe(CN)6]
(2)氰化钠(NaCN)是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。NaCN的电子式为
(3)已知:氢氰酸是一种有苦杏仁气味的无色剧毒液体,易挥发,25℃时,Ka(HCN)=6.25×10-10。
①处理含CN-废水的方法是:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5-8.5,用NaClO完全氧化OCN-生成N2和两种盐。
请写出第二步反应的离子方程式:
②反应CN-+H2O
 HCN+OH-在25℃时的平衡常数K=
HCN+OH-在25℃时的平衡常数K=(4)K4Fe(CN)6与高锰酸钾溶液反应,其方程式为:
K4Fe(CN)6+KMnO4 +H2SO4=KHSO4+Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平), 若有1mol K4Fe(CN)6被高锰酸钾氧化时,则消耗KMnO4的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】含氯消毒剂是一类毒性低、价格低、杀菌效率高、被广泛使用的高效杀毒剂,在控制病原微生物污染和传播等方面右着重要作用。亚氯酸钠(NaClO2)是一种优质的漂白剂和消毒剂。一种以氯酸钠(NaClO3)为原料制备NaClO2粗品的工艺流程如图所示:
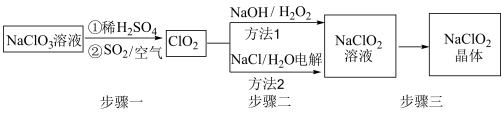
已知:①纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
②硫单质与碱在一定条件下可以反应:3S+6KOH=2K2S+K2SO3+3H2O。
(1)步骤一中通入空气的作用是___________ 。
(2)写出方法1中发生反应的化学方程式:___________ ,此方法中不宜用S代替H2O2,理由是___________ 。
(3)方法2所用食盐水由粗盐水精制而成,精制时,为除去粗盐水中的Ca2+和 ,按顺序加入的除杂试剂为
,按顺序加入的除杂试剂为_______ 。可用NaOH溶液吸收电解产生的氯气,该反应的离子方程式是________ 。
(4)NaClO2和Cl2消毒时,还原产物均为Cl-。消毒剂的消毒效率可用单位质量消毒剂被还原时得电子数表示,计算NaClO2的消毒效率是Cl2的___________ 倍。(计算结果保留一位小数)

已知:①纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
②硫单质与碱在一定条件下可以反应:3S+6KOH=2K2S+K2SO3+3H2O。
(1)步骤一中通入空气的作用是
(2)写出方法1中发生反应的化学方程式:
(3)方法2所用食盐水由粗盐水精制而成,精制时,为除去粗盐水中的Ca2+和
 ,按顺序加入的除杂试剂为
,按顺序加入的除杂试剂为(4)NaClO2和Cl2消毒时,还原产物均为Cl-。消毒剂的消毒效率可用单位质量消毒剂被还原时得电子数表示,计算NaClO2的消毒效率是Cl2的
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】草酸是一种重要的试剂。下面是利用草酸探究浓度对反应速率影响的实验。
(1)为证明浓度对反应速率的影响,教科书《化学反应原理》中设计了如下实验:取两支试管,各加入4mL0.01mol·L-1的KMnO4酸性溶液,分别向其中加入0.1mol·L-1、0.2mol·L-1H2C2O4溶液2mL,记录溶液褪色所需时间。
实验中发生反应的离子方程式为___ 。
预期现象是:
①溶液的颜色由___ 色变为___ 色。
②其中加入___ mol·L-1H2C2O4的那支试管中的溶液先变色。然而实验结果并不尽如人意。实验过程颜色复杂,且褪色先缓慢后逐渐加快;最大的问题是草酸浓度大,反应速率却更慢。
本实验能否作为课堂实验研究浓度对化学反应速率的影响?适宜的条件是怎样的?某校一研究小组对此进行了探究。下面是他们的实验报告的一部分:
表1试验安排及结果
应用SPSS16.0对正交试验结果进行方差分析,结果如表:
表2各因素水平的数据处理结果
(2)由表2可知,三因素中,____ 的浓度(选填“A”、“B”或“C”,下同)对反应速率影响显著,而___ 的浓度对反应速率的影响不显著。
(3)由表2可知,当高锰酸钾浓度为___ mol·L-1、草酸浓度为____ mol·L-1时,反应最快。即因素A、B的较适宜实验条件得以确定。
根据以上实验结果,该小组同学继续探究硫酸的浓度是怎样影响本反应速率的,测得实验结果如下:
表3不同硫酸浓度下的褪色时间
(4)根据课堂实验的合适时间,可选溶液的褪色时间约为1分钟和2分钟的两份溶液,即此时硫酸的浓度____ mol·L-1和___ mol·L-1,这也有利于观察这两个反应速率的差异。
结论:草酸与酸性高锰酸钾溶液的反应,可作为课堂实验探究浓度对反应速率的影响。
(1)为证明浓度对反应速率的影响,教科书《化学反应原理》中设计了如下实验:取两支试管,各加入4mL0.01mol·L-1的KMnO4酸性溶液,分别向其中加入0.1mol·L-1、0.2mol·L-1H2C2O4溶液2mL,记录溶液褪色所需时间。
实验中发生反应的离子方程式为
预期现象是:
①溶液的颜色由
②其中加入
本实验能否作为课堂实验研究浓度对化学反应速率的影响?适宜的条件是怎样的?某校一研究小组对此进行了探究。下面是他们的实验报告的一部分:
表1试验安排及结果
| 实验 编号 | A(KMnO4溶液 浓度/mol·L-1) | B(草酸溶液 浓度/mol·L-1) | C(硫酸溶液 浓度/mol·L-1) | 褪色时间/s |
| 1 | 3 | 3 | 1 | 336 |
| 2 | 1 | 2 | 3 | 82 |
| 3 | 3 | 1 | 3 | 76 |
| 4 | 1 | 3 | 2 | 133 |
| 5 | 2 | 3 | 3 | 102 |
| 6 | 3 | 2 | 2 | 156 |
| 7 | 2 | 2 | 1 | 300 |
| 8 | 2 | 1 | 2 | 115 |
| 9 | 1 | 1 | 1 | 200 |
表2各因素水平的数据处理结果
| A(KMnO4溶液) | B(草酸溶液) | C(硫酸溶液) | |||||||
| 浓度/mol·L-1 | 0.005 | 0.010 | 0.015 | 0.1 | 0.5 | 0.9 | 6 | 12 | 18 |
| 平均褪色时间/s | 138.3 | 172.3 | 189.3 | 130.3 | 179.3 | 190.3 | 278.7 | 134.7 | 86.7 |
(3)由表2可知,当高锰酸钾浓度为
根据以上实验结果,该小组同学继续探究硫酸的浓度是怎样影响本反应速率的,测得实验结果如下:
表3不同硫酸浓度下的褪色时间
| c(H2SO4)/mol·L-1 | 18 | 16 | 14 | 12 | 10 | 8 | 6 |
| 褪色时间/s | 67 | 83 | 90 | 103 | 129 | 146 | 200 |
结论:草酸与酸性高锰酸钾溶液的反应,可作为课堂实验探究浓度对反应速率的影响。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】含硫化合物,不仅用于研究化学反应的原理,也在生产生活有普遍应用。
(1)以反应 为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
请回答:①上表中,a为_______ ,b为_______ 。
②上述三个实验中的反应速率最快的应该是实验_______ (用I、II、III作答)
(2)亚硫酸钠是一种常见的食品添加剂。为检验某食品中亚硫酸钠含量(通常以 样品中含
样品中含 的质量计),某研究小组同学设计了如下实验方案。
的质量计),某研究小组同学设计了如下实验方案。
I.称取样品 ;
;
II.向样品中加入足量稀硫酸;
III.将I中产生的 用足量
用足量 溶液吸收;
溶液吸收;
IV.将II所得硫酸溶液用氢氧化钠标准液滴定;
V.数据处理。
① 是一种食品添加剂。写出
是一种食品添加剂。写出 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式_______ 。
②步骤III中 的作用是
的作用是_______ 。
③步骤IV中可选用的指示剂为_______ 。下图显示滴定终点时,滴定管(量程为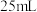 )读数为
)读数为_______  。
。

④步骤IV中消耗 溶液
溶液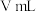 ,则
,则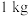 样品中含
样品中含 的质量是
的质量是_______ g(用含W、V的代数式表示)。
⑤步骤IV中的下列操作会造成该实验亚硫酸盐含量测定结果偏低的有_______ 。
a.滴定开始读数时仰视读数
b.装入氢氧化钠标准液前,碱式滴定管未用氢氧化钠标准液润洗
c.锥形瓶内用水冲洗后未干燥
d.在滴定过程中发现局部溶液发生色变就立即停止滴定
(1)以反应
 为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。| 实验序号 |  溶液 溶液 |  溶液 溶液 | 蒸馏水 | 温度/℃ | ||
浓度/( ) ) | 体积/mL | 浓度/( ) ) | 体积/mL | 体积/mL | ||
| I | 0.1 | 1.5 | 0.1 | 1.5 | 10 | 20 |
| II | 0.1 | 2.5 | 0.1 | 1.5 | 9 | a |
| III | 0.1 | b | 0.1 | 1.5 | 9 | 30 |
②上述三个实验中的反应速率最快的应该是实验
(2)亚硫酸钠是一种常见的食品添加剂。为检验某食品中亚硫酸钠含量(通常以
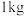 样品中含
样品中含 的质量计),某研究小组同学设计了如下实验方案。
的质量计),某研究小组同学设计了如下实验方案。I.称取样品
 ;
;II.向样品中加入足量稀硫酸;
III.将I中产生的
 用足量
用足量 溶液吸收;
溶液吸收;IV.将II所得硫酸溶液用氢氧化钠标准液滴定;
V.数据处理。
①
 是一种食品添加剂。写出
是一种食品添加剂。写出 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式②步骤III中
 的作用是
的作用是③步骤IV中可选用的指示剂为
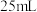 )读数为
)读数为 。
。
④步骤IV中消耗
 溶液
溶液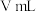 ,则
,则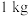 样品中含
样品中含 的质量是
的质量是⑤步骤IV中的下列操作会造成该实验亚硫酸盐含量测定结果偏低的有
a.滴定开始读数时仰视读数
b.装入氢氧化钠标准液前,碱式滴定管未用氢氧化钠标准液润洗
c.锥形瓶内用水冲洗后未干燥
d.在滴定过程中发现局部溶液发生色变就立即停止滴定
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】某兴趣小组探究外界因素对化学反应的影响,设计了下面两组实验。
I.探究反应物浓度对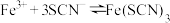 的影响
的影响
(1).在小烧杯中加入10mL蒸馏水,再滴入5滴0.05 FeCl3溶液、5滴0.15
FeCl3溶液、5滴0.15 KSCN溶液,用玻璃棒搅拌,使其充分混合,此时测得溶液吸光度为
KSCN溶液,用玻璃棒搅拌,使其充分混合,此时测得溶液吸光度为 。然后将溶液平均注入a、b、c三支试管中。按下列方案进行实验并记录溶液的吸光度(溶液颜色越深,吸光度越大):
。然后将溶液平均注入a、b、c三支试管中。按下列方案进行实验并记录溶液的吸光度(溶液颜色越深,吸光度越大):
①配制100mL0.15 KSCN溶液所需要用到的玻璃仪器有100mL容量瓶、烧杯和
KSCN溶液所需要用到的玻璃仪器有100mL容量瓶、烧杯和____________ 。
②试管a和c是为了验证____________________________________ ,预测两支试管吸光度的大小关系:
η1__________ η3(填“>”“<”或“=”)。
③已知η2<η0,试用平衡移动原理解释此现象___________________________________________________ 。
II.用0.50 KI溶液、0.2%淀粉溶液、0.20
KI溶液、0.2%淀粉溶液、0.20 K2S2O8溶液、0.10
K2S2O8溶液、0.10 Na2S2O3溶液等试剂,探究反应条件对化学反应速率的影响。
Na2S2O3溶液等试剂,探究反应条件对化学反应速率的影响。
已知: (慢)
(慢) 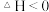

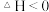
(2).向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色, 与
与 初始的物质的量需满足的关系为:
初始的物质的量需满足的关系为:
_______________ 。
(3).为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中Vx=__________ mL,理由是_______________________________________________________ 。
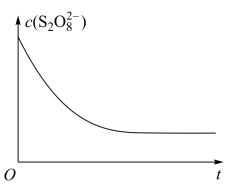
(4).已知某条件下,浓度 ~反应时间t的变化曲线如图,若保持其他条件不变,请在坐标图中,画出降低反应温度时
~反应时间t的变化曲线如图,若保持其他条件不变,请在坐标图中,画出降低反应温度时 ~t的变化曲线示意图(注意要进行必要的标注)
~t的变化曲线示意图(注意要进行必要的标注)___________ 。
I.探究反应物浓度对
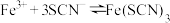 的影响
的影响(1).在小烧杯中加入10mL蒸馏水,再滴入5滴0.05
 FeCl3溶液、5滴0.15
FeCl3溶液、5滴0.15 KSCN溶液,用玻璃棒搅拌,使其充分混合,此时测得溶液吸光度为
KSCN溶液,用玻璃棒搅拌,使其充分混合,此时测得溶液吸光度为 。然后将溶液平均注入a、b、c三支试管中。按下列方案进行实验并记录溶液的吸光度(溶液颜色越深,吸光度越大):
。然后将溶液平均注入a、b、c三支试管中。按下列方案进行实验并记录溶液的吸光度(溶液颜色越深,吸光度越大):试管编号 | 加入试剂 | 吸光度 |
a | 5滴m1 | η1 |
b | 少量还原铁粉 | η2 |
c | 5滴蒸馏水 | η3 |
 KSCN溶液所需要用到的玻璃仪器有100mL容量瓶、烧杯和
KSCN溶液所需要用到的玻璃仪器有100mL容量瓶、烧杯和②试管a和c是为了验证
η1
③已知η2<η0,试用平衡移动原理解释此现象
II.用0.50
 KI溶液、0.2%淀粉溶液、0.20
KI溶液、0.2%淀粉溶液、0.20 K2S2O8溶液、0.10
K2S2O8溶液、0.10 Na2S2O3溶液等试剂,探究反应条件对化学反应速率的影响。
Na2S2O3溶液等试剂,探究反应条件对化学反应速率的影响。已知:
 (慢)
(慢) 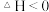

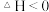
(2).向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,
 与
与 初始的物质的量需满足的关系为:
初始的物质的量需满足的关系为:
(3).为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积V/mL | ||||
K2S2O3溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
(4).已知某条件下,浓度
 ~反应时间t的变化曲线如图,若保持其他条件不变,请在坐标图中,画出降低反应温度时
~反应时间t的变化曲线如图,若保持其他条件不变,请在坐标图中,画出降低反应温度时 ~t的变化曲线示意图(注意要进行必要的标注)
~t的变化曲线示意图(注意要进行必要的标注)
您最近一年使用:0次



