过量的碳排放会引起温室效应,针对固碳方法开展了大量研究工作。
(1)海水可以吸收一定量的二氧化碳。
①溶于海水的CO2主要以4种无机碳形式存在,其中 占95%,写出CO2溶于水产生
占95%,写出CO2溶于水产生 的方程式:
的方程式:_____ 。
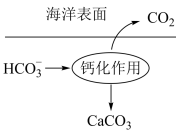
②在海洋中,珊瑚虫可以将海水中的 和
和 通过钙化用(如图)转化为CaCO3,钙化作用的离子方程式为
通过钙化用(如图)转化为CaCO3,钙化作用的离子方程式为_____ 。
(2)“尾气CO2固化及磷石膏联产工艺”涉及CO2减排和工业固废磷石膏处理两大工业环保技术领域,其部分工艺流程如下图:
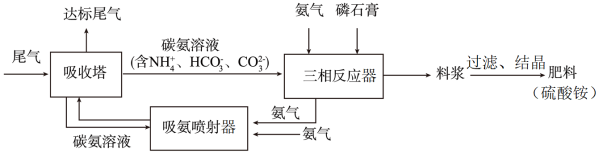
已知:磷石膏主要成分CaSO4·2H2O。
①吸收塔中发生的反应可能有_____ (写出2个离子方程式)。
②写出三相反应器中沉淀转化反应的离子方程式_____ 。
③三相反应器中氨气的作用是_____ 。
(3)如图是利用氢氧燃料电池进行CO2浓缩富集的装置。
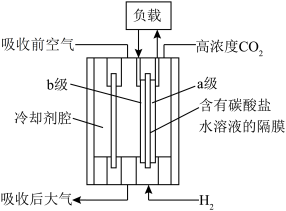
①对比吸收前和吸收后空气成分,含量一定下降的是CO2和_____ 。
②结合a、b两极的电极反应和微粒迁移,解释该装置能进行CO2浓缩富集的原理_____ 。
(1)海水可以吸收一定量的二氧化碳。
①溶于海水的CO2主要以4种无机碳形式存在,其中
 占95%,写出CO2溶于水产生
占95%,写出CO2溶于水产生 的方程式:
的方程式:②在海洋中,珊瑚虫可以将海水中的
 和
和 通过钙化用(如图)转化为CaCO3,钙化作用的离子方程式为
通过钙化用(如图)转化为CaCO3,钙化作用的离子方程式为
(2)“尾气CO2固化及磷石膏联产工艺”涉及CO2减排和工业固废磷石膏处理两大工业环保技术领域,其部分工艺流程如下图:

已知:磷石膏主要成分CaSO4·2H2O。
①吸收塔中发生的反应可能有
②写出三相反应器中沉淀转化反应的离子方程式
③三相反应器中氨气的作用是
(3)如图是利用氢氧燃料电池进行CO2浓缩富集的装置。

①对比吸收前和吸收后空气成分,含量一定下降的是CO2和
②结合a、b两极的电极反应和微粒迁移,解释该装置能进行CO2浓缩富集的原理
更新时间:2023-11-05 15:45:45
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】铊(Tl)在工业中的用途非常广泛,其中铊锡合金可作超导材料:铊镉合金是原子能工业中的重要材料。铊主要从铅精矿焙烧产生的富铊灰(主要成分PbO、ZnO、Fe2O3、 FeO、Tl2O等)中提炼,具体工艺流程如图。
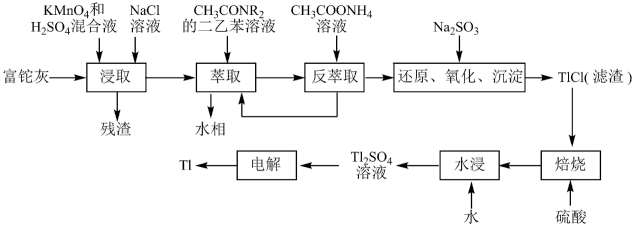
已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H+ +CH3CONR2+TlCl
 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。
回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供H+,另一作用为_______ 。
(2)在实验室中,“萃取”过程使用的玻璃仪器有烧杯,还有_______ ,用平衡移动解释“反萃取”过程的原理和目的_______ 。
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为_______ ,为提高经济效益充分利用原料,该反应的滤液可加入_______ 步骤循环使用最合适。
(4)Tl+对人体毒性很大,难溶盐KFe[Fe(CN)6]可通过离子交换治疗Tl2SO4中毒,将其转化为沉淀同时生成K2SO4溶液,写出治疗Tl2SO4中毒的离子方程式:_______ 。
(5)电解Tl2SO4溶液制备金属Tl的装置如图所示。石墨(C)上电极反应式为_______ 。


已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H+ +CH3CONR2+TlCl

 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供H+,另一作用为
(2)在实验室中,“萃取”过程使用的玻璃仪器有烧杯,还有
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为
(4)Tl+对人体毒性很大,难溶盐KFe[Fe(CN)6]可通过离子交换治疗Tl2SO4中毒,将其转化为沉淀同时生成K2SO4溶液,写出治疗Tl2SO4中毒的离子方程式:
(5)电解Tl2SO4溶液制备金属Tl的装置如图所示。石墨(C)上电极反应式为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】锌是一种重要的金属,在电镀电池等工业上具有广泛的应用。以废锌催化剂(主要成分为ZnO及少量Fe2O3、CuO、MnO2)为原料制备锌的工艺流程如下。

已知:①“浸取”后溶液中的阳离子主要是[ Zn( NH3)4]2+、[Cu(NH3)4]2+。
②25 °C时Ksp(ZnS)= 1.6×10-24 ;深度除杂标准:溶液中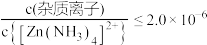 回答下列问题:
回答下列问题:
(1)滤渣①的主要成分是_______ (填化学式);“浸取”时,ZnO发生反应的离子方程式为_______ 。
(2)加入过量氨水的作用之一是使 ZnO、CuO溶解,另一个作用是_______ ;“萃取”时需要进行多次萃取且合并萃取液,其目的是_______ 。
(3)“深度除铜”时涉及的部分反应为:
[Cu(NH3)4]2+ +4H2O Cu2+ +
Cu2+ +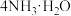 K1=a
K1=a
[Cu(NH3)4]2++S2- +4H2O CuS↓+
CuS↓+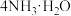 K2=b
K2=b
(NH4)2S的加入量 对锌的回收率及铜锌比
对锌的回收率及铜锌比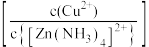 的影响如图所示。
的影响如图所示。
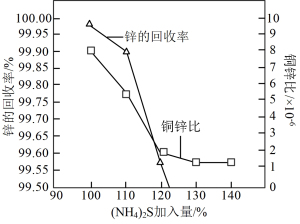
①当(NH4)2S加入量超过100%时,锌的回收率下降的可能原因是_______ (用离子方程式表示)。
②(NH4)2S较为合理的加入量约为120%,理由是_______ 。
③室温下,向“浸取”液中加入一定量(NH4)2S固体,“深度除铜”后,测得溶液中 c(Cu2+)为1.0×10-8 mol·L-1,此时溶液中c(S2- )为_______ mol·L-1(用含a、b的代数式表示,忽略S2-水解)。
(4)用惰性电极“电解”时,阴极存在竞争反应,该竞争反应的电极反应式为_______ 。

已知:①“浸取”后溶液中的阳离子主要是[ Zn( NH3)4]2+、[Cu(NH3)4]2+。
②25 °C时Ksp(ZnS)= 1.6×10-24 ;深度除杂标准:溶液中
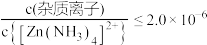 回答下列问题:
回答下列问题:(1)滤渣①的主要成分是
(2)加入过量氨水的作用之一是使 ZnO、CuO溶解,另一个作用是
(3)“深度除铜”时涉及的部分反应为:
[Cu(NH3)4]2+ +4H2O
 Cu2+ +
Cu2+ +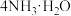 K1=a
K1=a[Cu(NH3)4]2++S2- +4H2O
 CuS↓+
CuS↓+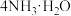 K2=b
K2=b (NH4)2S的加入量
 对锌的回收率及铜锌比
对锌的回收率及铜锌比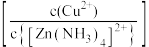 的影响如图所示。
的影响如图所示。
①当(NH4)2S加入量超过100%时,锌的回收率下降的可能原因是
②(NH4)2S较为合理的加入量约为120%,理由是
③室温下,向“浸取”液中加入一定量(NH4)2S固体,“深度除铜”后,测得溶液中 c(Cu2+)为1.0×10-8 mol·L-1,此时溶液中c(S2- )为
(4)用惰性电极“电解”时,阴极存在竞争反应,该竞争反应的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】三氧化二钴主要用作颜料、釉料及磁性材料,利用铜钴矿石制备Co2O3的工艺流程如图所示。

已知:铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,其中还含有一定量的Fe2O3、MgO和CaO等。请回答下列问题:
(1)“浸泡”过程中可以加快反应速率和提高原料利用率的方法是___ 。(写出2种即可)
(2)“浸泡”过程中,加入Na2SO3溶液的主要作用是___ 。
(3)向“沉铜”后的滤液中加入NaClO3溶液,写出滤液中的金属离子与NaClO3反应的离子方程式___ 。
(4)CoC2O4•2H2O在空气中高温煅烧得到Co2O3的化学方程式是___ 。
(5)一定温度下,向滤液A中加入足量的NaF溶液可将Ca2+、Mg2+沉淀而除去,若所得滤液B中c(Mg2+)═1.0×10-5 mol•L-1,则滤液B中c(Ca2+)为___ 。[已知该温度下Ksp(CaF2)=3.4×10-11,Ksp(MgF2)═7.1×10-11]。

已知:铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,其中还含有一定量的Fe2O3、MgO和CaO等。请回答下列问题:
(1)“浸泡”过程中可以加快反应速率和提高原料利用率的方法是
(2)“浸泡”过程中,加入Na2SO3溶液的主要作用是
(3)向“沉铜”后的滤液中加入NaClO3溶液,写出滤液中的金属离子与NaClO3反应的离子方程式
(4)CoC2O4•2H2O在空气中高温煅烧得到Co2O3的化学方程式是
(5)一定温度下,向滤液A中加入足量的NaF溶液可将Ca2+、Mg2+沉淀而除去,若所得滤液B中c(Mg2+)═1.0×10-5 mol•L-1,则滤液B中c(Ca2+)为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】用系统命法写出下列物质名称或结构简式
(1)C4H10的一氯代物有_____________ 种。
(2)某有机物含C、H、O三种元素,分子模型如图所示(图中球与球之间的连线代表化学键.如单键、双键等)。该有机物的结构简式为_____________________ ,所含官能团的名称为 __________

(3)常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-)/c(H+)=1×10-8。常温下,0. 1 mol·L-1 HA溶液的pH=________ ;
(4)常温下,将0.1mol/L HCl溶液与0.1 mol/L MOH溶液等体积混合,测得混合后溶液的pH=5,则MOH在水中的电离方程式为_________________ 。
(5)已知常温时CH3COOH⇌CH3COO – + H+,Ka=2×10–5,则反应CH3COO – + H2O⇌CH3COOH + OH–的平衡常数Kh=________________ 。
(6)常温下,若在0.10 mol·L–1 CuSO4溶液中加入NaOH稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________ mol·L–1 {Ksp[Cu(OH)2]=2.2×10–20}。
(7)1mol/L Na2C2O4溶液中离子浓度由大到小顺序_________________________ ,列出质子守恒关系式_____________________
(1)C4H10的一氯代物有
(2)某有机物含C、H、O三种元素,分子模型如图所示(图中球与球之间的连线代表化学键.如单键、双键等)。该有机物的结构简式为

(3)常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-)/c(H+)=1×10-8。常温下,0. 1 mol·L-1 HA溶液的pH=
(4)常温下,将0.1mol/L HCl溶液与0.1 mol/L MOH溶液等体积混合,测得混合后溶液的pH=5,则MOH在水中的电离方程式为
(5)已知常温时CH3COOH⇌CH3COO – + H+,Ka=2×10–5,则反应CH3COO – + H2O⇌CH3COOH + OH–的平衡常数Kh=
(6)常温下,若在0.10 mol·L–1 CuSO4溶液中加入NaOH稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
(7)1mol/L Na2C2O4溶液中离子浓度由大到小顺序
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】氢氰酸(HCN)有剧毒,易挥发。金矿提金时,用NaCN溶液浸取金生成[Au(CN)2]-,再用锌置换出金,产生的含氰废水需处理后排放。
(1)①[Au(CN)2]-存在着两步电离平衡,其第一步电离方程式为___________ 。
②NaCN可用于制备CuCN,CuCN浊液中加入Na2S溶液可发生反应:2CuCN(s)+S2-(aq) Cu2S(s)+2CN-(aq),该反应的平衡常数K=
Cu2S(s)+2CN-(aq),该反应的平衡常数K=___________ 。[已知Ksp(CuCN)=3.5×10-20,Ksp(Cu2S)=1.0×10-48]。
(2)Cu2+可催化H2O2氧化废水中的CN-。其他条件相同时,总氰化物(CN-、HCN等)去除率随溶液初始pH变化如图所示。
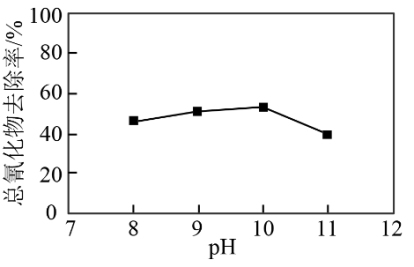
①酸性条件下,H2O2也能氧化CN-,但实际处理废水时却不在酸性条件下进行的原因是___________ 。
②当溶液初始pH>10时,总氰化物去除率下降的原因可能是___________ 。
(3)通过电激发产生HO·和OH-处理废水中的CN-,可能的反应机理如图所示。虚线方框内的过程可描述为___________ 。

(1)①[Au(CN)2]-存在着两步电离平衡,其第一步电离方程式为
②NaCN可用于制备CuCN,CuCN浊液中加入Na2S溶液可发生反应:2CuCN(s)+S2-(aq)
 Cu2S(s)+2CN-(aq),该反应的平衡常数K=
Cu2S(s)+2CN-(aq),该反应的平衡常数K=(2)Cu2+可催化H2O2氧化废水中的CN-。其他条件相同时,总氰化物(CN-、HCN等)去除率随溶液初始pH变化如图所示。

①酸性条件下,H2O2也能氧化CN-,但实际处理废水时却不在酸性条件下进行的原因是
②当溶液初始pH>10时,总氰化物去除率下降的原因可能是
(3)通过电激发产生HO·和OH-处理废水中的CN-,可能的反应机理如图所示。虚线方框内的过程可描述为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4 -+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。某实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计方案如下(KMnO4溶液已酸化):
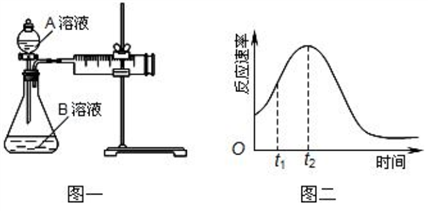
(1)该实验探究的是______ 对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是_____ (填实验序号)。
(2)若实验①在2min末注射器的活塞向右移动到了b mL的位置,则这段时间的反应速率可表示为v(CO2)=______ mL/min。若实验②在t min收集了4.48×10-3L CO2(标准状况下),则t min末c(MnO4-)=______ 。
(3)该小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是:①___________ 、②___________ 。
(4)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2、K2=5.4×10-5,写出草酸的电离方程式_______ 、________ 。试从电离平衡移动的角度解释K1>>K2的原因_______________ 。
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.lmol·L-l H2C2O4溶液 | 30mL 0.01mol.L-l KMnO4溶液 |
| ② | 20mL 0.2mol·L-l H2C2O4溶液 | 30mL 0.01mol.L-l KMnO4溶液 |

(1)该实验探究的是
(2)若实验①在2min末注射器的活塞向右移动到了b mL的位置,则这段时间的反应速率可表示为v(CO2)=
(3)该小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是:①
(4)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2、K2=5.4×10-5,写出草酸的电离方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】硒是典型的半导体材料,在光照下导电性可提高近千倍。如图是从某工厂的硒化银半导体废料(含Ag2Se、Cu单质)中提取硒、银的工艺流程图:
(1)已知反应③生成一种可参与大气循环的气体单质,写出该反应的离子程式_______ 。
(2)已知:常温下Ag2SO4、AgCl的饱和溶液中阳离子和阴离子浓度关系如图所示,反应②为_______ (写离子方程式);该反应的化学平衡常数的数量级为_______ 。 、SeO
、SeO 摩尔分数随pH的变化如图所示,则室温下SeO
摩尔分数随pH的变化如图所示,则室温下SeO 的Kh=
的Kh=________ 。_______ (写电极反应式)。

(1)已知反应③生成一种可参与大气循环的气体单质,写出该反应的离子程式
(2)已知:常温下Ag2SO4、AgCl的饱和溶液中阳离子和阴离子浓度关系如图所示,反应②为

 、SeO
、SeO 摩尔分数随pH的变化如图所示,则室温下SeO
摩尔分数随pH的变化如图所示,则室温下SeO 的Kh=
的Kh=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】按要求回答下列问题
可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为H3PO4,沸点高,难挥发)有一定关系。
(1)室温下,测得0.1 mol/L H3PO4溶液的pH= 1.5,用电离方程式解释原因:_______ 。
(2)羟基磷酸钙[Ca5(PO4)3OH]是牙齿表面起保护作用的一层坚硬物质, 在唾液中存在如下平衡:Ca5(PO4)3OH(s)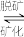 5Ca2+(aq) +3
5Ca2+(aq) +3 (aq) + OH-(aq),长期过量饮用可乐会破坏这层坚硬物质,造成龋齿。结合平衡移动原理解释原因:
(aq) + OH-(aq),长期过量饮用可乐会破坏这层坚硬物质,造成龋齿。结合平衡移动原理解释原因:_______ 。
(3)用含氟牙膏刷牙,氟离子会与牙釉质[主要成分为Ca5(PO4)3OH]发生反应: Ca5(PO4)3OH(s)+F-(aq) Ca5(PO4)3F(s)+OH-(aq),该反应的平衡常数K=
Ca5(PO4)3F(s)+OH-(aq),该反应的平衡常数K=_______ (已知Ksp[Ca5(PO4)3OH]=7×l0-37,Ksp[Ca5(PO4)3F]=2.8×l0-61)。
(4)向磷酸溶液中滴加NaOH溶液,含磷各微粒在溶液中的物质的量分数与pH的关系如图。
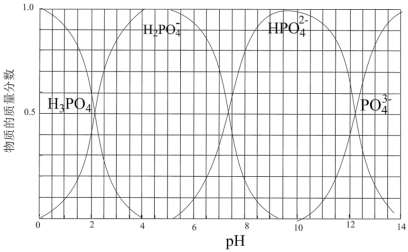
①向磷酸溶液中滴加NaOH溶液至pH = 10时发生的主要反应的离子方程式是_______ 。
②下列关于0.1 mol/L Na2HPO4溶液的说法正确的是_______ (填序号)。
a.Na2HPO4溶液显碱性,原因是 的水解程度大于其电离程度
的水解程度大于其电离程度
b.c(Na+) + c(H+) = c( )+ 2c(
)+ 2c( ) + 3c(
) + 3c( )+ c(OH- )
)+ c(OH- )
c.c(Na+) = c( ) + c(
) + c( ) +c(
) +c( ) + c(H3PO4)
) + c(H3PO4)
可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为H3PO4,沸点高,难挥发)有一定关系。
(1)室温下,测得0.1 mol/L H3PO4溶液的pH= 1.5,用电离方程式解释原因:
(2)羟基磷酸钙[Ca5(PO4)3OH]是牙齿表面起保护作用的一层坚硬物质, 在唾液中存在如下平衡:Ca5(PO4)3OH(s)
 5Ca2+(aq) +3
5Ca2+(aq) +3 (aq) + OH-(aq),长期过量饮用可乐会破坏这层坚硬物质,造成龋齿。结合平衡移动原理解释原因:
(aq) + OH-(aq),长期过量饮用可乐会破坏这层坚硬物质,造成龋齿。结合平衡移动原理解释原因:(3)用含氟牙膏刷牙,氟离子会与牙釉质[主要成分为Ca5(PO4)3OH]发生反应: Ca5(PO4)3OH(s)+F-(aq)
 Ca5(PO4)3F(s)+OH-(aq),该反应的平衡常数K=
Ca5(PO4)3F(s)+OH-(aq),该反应的平衡常数K=(4)向磷酸溶液中滴加NaOH溶液,含磷各微粒在溶液中的物质的量分数与pH的关系如图。

①向磷酸溶液中滴加NaOH溶液至pH = 10时发生的主要反应的离子方程式是
②下列关于0.1 mol/L Na2HPO4溶液的说法正确的是
a.Na2HPO4溶液显碱性,原因是
 的水解程度大于其电离程度
的水解程度大于其电离程度b.c(Na+) + c(H+) = c(
 )+ 2c(
)+ 2c( ) + 3c(
) + 3c( )+ c(OH- )
)+ c(OH- )c.c(Na+) = c(
 ) + c(
) + c( ) +c(
) +c( ) + c(H3PO4)
) + c(H3PO4)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.(1)在2L定容密闭容器中通入1molN2(g)和3molH2(g),发生反应:
3H2(g)+N2(g) 2NH3(g)△H<0,测得压强一时间图象如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图象。
2NH3(g)△H<0,测得压强一时间图象如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图象。
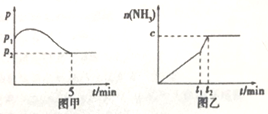
①若图中c=1.6mol,则改变的条件是__________ (填字母,下同);
A.升温 B.降温 C.加压 D.减压 E.加催化剂
②若图中c<1.6mol,则改变的条件是__________ (填字母);此时该反应的平衡常数__________ (填“增大”、“减小”、“不变”)。
(2)如图甲,平衡时氢气的转化率为____________ 。
Ⅱ.粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
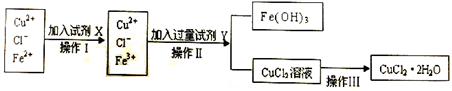
(1)操作Ⅰ时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是__________ 。
A.KMnO4 B.H2O2 C.Cl2 D.HNO3
(2)操作Ⅱ调整溶液的pH的Y试剂可选用下列中的__________ 。
A.NaOH(s) B.氨水 C.CuO(s) D.Cu(OH)2(s)
(3)已知溶度积常数如下表:
将溶液的pH调至pH=4时,使Fe3+完全转化为Fe(OH)3沉淀而除去,此时c(Fe3+)=__________ 。
(4)若将CuCl2溶液蒸干后,再灼烧,得到的固体是__________ (填化学式);操作Ⅲ后由CuCl2·2H2O晶体得到纯净无水CuCl2的合理操作是_____________________________________ 。
3H2(g)+N2(g)
 2NH3(g)△H<0,测得压强一时间图象如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图象。
2NH3(g)△H<0,测得压强一时间图象如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图象。
①若图中c=1.6mol,则改变的条件是
A.升温 B.降温 C.加压 D.减压 E.加催化剂
②若图中c<1.6mol,则改变的条件是
(2)如图甲,平衡时氢气的转化率为
Ⅱ.粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。

(1)操作Ⅰ时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是
A.KMnO4 B.H2O2 C.Cl2 D.HNO3
(2)操作Ⅱ调整溶液的pH的Y试剂可选用下列中的
A.NaOH(s) B.氨水 C.CuO(s) D.Cu(OH)2(s)
(3)已知溶度积常数如下表:
| 物质 | Cu(OH) | Fe(OH)2 | Fe(OH)3 |
| Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
将溶液的pH调至pH=4时,使Fe3+完全转化为Fe(OH)3沉淀而除去,此时c(Fe3+)=
(4)若将CuCl2溶液蒸干后,再灼烧,得到的固体是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】I.研究催化剂使CO2在一定条件下合成有机燃料,是力争2030年前做到碳达峰,2060年前实现碳中和的方向之一、
(1)已知:①CO2(g)+H2(g)=CO(g)+H2O(g) ΔΗ1=+41.2kJ/mol
②CO(g)+2H2(g)= CH2=CH2(g)+H2O(g) ΔΗ2=-166kJ/mol
CH2=CH2(g)+H2O(g) ΔΗ2=-166kJ/mol
则CO2在一种含铁催化剂的条件下与氢气催化合成乙烯的热化学方程式为_______ 。
(2)含铁催化剂可用作CO2与氢气反应的催化剂。已知某种催化剂可用来催化反应CO2(g)+H2(g)→CH2=CH2(g)+H2O(g)(未配平)。在T℃、106Pa时,将1molCO2和3molH2加入容积不变的密闭容器中,实验测得CO2的体积分数φ(CO2)如表所示:
①能判断反应CO2(g)+H2(g)→CH2=CH2(g)+H2O(g)(未配平)达到平衡的是_______ (填字母)。
a.容器内压强不再发生变化
b.混合气体的密度不再发生变化
c.v正(CO2)=3v逆(H2)
d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO2的转化率为_______ %(保留至小数点后1位)。
③一定压强下,将1molCO2和3molH2加入1L容积不变的密闭容器中,已知温度对CO2的平衡转化率、实际转化率和催化剂催化效率的影响如图甲所示,结合图象分析该反应实际反应温度定于250℃的原因是_______ ;250℃时,该反应达到平衡时的平衡常数K=_______ (用最简分式表示)。

II.甲醇是一种可再生能源,具有广阔的开发和应用前景,可用Pt/Al2O3、Pd/C、Rh/SiO2等作催化剂,采用如下反应来合成甲醇:2H2(g)+CO(g)⇌CH3OH(g)。
(3)将CO和H2加入密闭容器中,在一定条件下发生反应:CO(g)+2H2(g)⇌CH3OH(g) ΔH<0。平衡时CO的体积分数(%)与温度和压强的关系如下图所示(虚线框表示没有测定该条件下的数据)。

T1、T2、T3由大到小的关系是_______ ,判断理由是_______ 。
(4)美国的两家公司合作开发了多孔硅甲醇直接燃料电池,其工作原理如图。
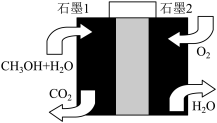
①石墨2为_______ (填“正”或“负”)极。
②石墨1极发生的电极反应式为_______ 。
(1)已知:①CO2(g)+H2(g)=CO(g)+H2O(g) ΔΗ1=+41.2kJ/mol
②CO(g)+2H2(g)=
 CH2=CH2(g)+H2O(g) ΔΗ2=-166kJ/mol
CH2=CH2(g)+H2O(g) ΔΗ2=-166kJ/mol则CO2在一种含铁催化剂的条件下与氢气催化合成乙烯的热化学方程式为
(2)含铁催化剂可用作CO2与氢气反应的催化剂。已知某种催化剂可用来催化反应CO2(g)+H2(g)→CH2=CH2(g)+H2O(g)(未配平)。在T℃、106Pa时,将1molCO2和3molH2加入容积不变的密闭容器中,实验测得CO2的体积分数φ(CO2)如表所示:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| φ(CO2) | 0.25 | 0.23 | 0.214 | 0.202 | 0.200 | 0.200 |
①能判断反应CO2(g)+H2(g)→CH2=CH2(g)+H2O(g)(未配平)达到平衡的是
a.容器内压强不再发生变化
b.混合气体的密度不再发生变化
c.v正(CO2)=3v逆(H2)
d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO2的转化率为
③一定压强下,将1molCO2和3molH2加入1L容积不变的密闭容器中,已知温度对CO2的平衡转化率、实际转化率和催化剂催化效率的影响如图甲所示,结合图象分析该反应实际反应温度定于250℃的原因是

II.甲醇是一种可再生能源,具有广阔的开发和应用前景,可用Pt/Al2O3、Pd/C、Rh/SiO2等作催化剂,采用如下反应来合成甲醇:2H2(g)+CO(g)⇌CH3OH(g)。
(3)将CO和H2加入密闭容器中,在一定条件下发生反应:CO(g)+2H2(g)⇌CH3OH(g) ΔH<0。平衡时CO的体积分数(%)与温度和压强的关系如下图所示(虚线框表示没有测定该条件下的数据)。

T1、T2、T3由大到小的关系是
(4)美国的两家公司合作开发了多孔硅甲醇直接燃料电池,其工作原理如图。

①石墨2为
②石墨1极发生的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】乙醇-水催化重整可获得 。主要发生以下反应:
。主要发生以下反应:
反应Ⅰ:
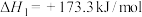
反应Ⅱ:
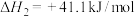
(1)反应Ⅰ自发进行的条件是_______。
(2)500℃时,向体积为VL的恒容密闭容器中充入1mol (g)和3mol
(g)和3mol  (g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%,
(g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%, 的转化率为80%。(CO的选择性=
的转化率为80%。(CO的选择性= )
)
①反应Ⅰ的
_______ (列出计算式即可)。反应Ⅰ的标准平衡常数 ,其中
,其中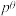 为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
②在下图中画出500℃时,乙醇平衡转化率随[ ]变化而变化的情况
]变化而变化的情况_______ 。 的平衡产率与温度、起始时
的平衡产率与温度、起始时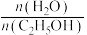 关系如图所示,每条曲线表示
关系如图所示,每条曲线表示 相同的平衡产率。
相同的平衡产率。 的平衡产率:Q点
的平衡产率:Q点_______ N点(填“>”、“=”或“<”);
②M、N两点 的平衡产率相等的原因是
的平衡产率相等的原因是_______ 。
(4)氢气的应用:氢气熔融碳酸盐燃料电池工作原理如图所示。 和
和 经催化重整生成CO和
经催化重整生成CO和 ,CO和
,CO和 全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)
全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)_______ 。
②理论上负极生成的 与正极消耗的
与正极消耗的 的物质的量之比是
的物质的量之比是_______ 。
 。主要发生以下反应:
。主要发生以下反应:反应Ⅰ:

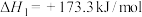
反应Ⅱ:

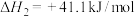
(1)反应Ⅰ自发进行的条件是_______。
| A.低温 | B.高温 | C.低压 | D.高压 |
(2)500℃时,向体积为VL的恒容密闭容器中充入1mol
 (g)和3mol
(g)和3mol  (g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%,
(g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%, 的转化率为80%。(CO的选择性=
的转化率为80%。(CO的选择性= )
)①反应Ⅰ的

 ,其中
,其中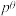 为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。②在下图中画出500℃时,乙醇平衡转化率随[
 ]变化而变化的情况
]变化而变化的情况
 的平衡产率与温度、起始时
的平衡产率与温度、起始时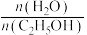 关系如图所示,每条曲线表示
关系如图所示,每条曲线表示 相同的平衡产率。
相同的平衡产率。
 的平衡产率:Q点
的平衡产率:Q点②M、N两点
 的平衡产率相等的原因是
的平衡产率相等的原因是(4)氢气的应用:氢气熔融碳酸盐燃料电池工作原理如图所示。

 和
和 经催化重整生成CO和
经催化重整生成CO和 ,CO和
,CO和 全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)
全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)②理论上负极生成的
 与正极消耗的
与正极消耗的 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
【推荐3】冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一。
(1)使用甲醇汽油可以减少汽车尾气对环境的污染。工业上在 200℃和 10MPa 的条件下可用甲烷和氧气通过铜制管道反应制得甲醇,已知一定条件下,CH4和 CH3OH 的燃烧热分别 784kJ/mol 和 628kJ/mol 则 2CH4(g)+O2(g)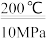 2CH3OH(g) △H=
2CH3OH(g) △H=_____ 。
(2)二甲醚也是清洁能源。用合成气在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g) ⇌CH3OCH3(g) +H2O(g) △H<0。某温度下,,将 2.0molCO(g)和 6.0molH2(g)充入容积为 2L 的密闭容器中,反应到达平衡时, 改变压强和温度,平衡体系中 CH3OCH3(g)的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是_____ 。
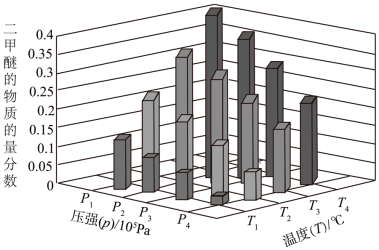
A.p3>p2,T3>T2
B.p1>p3,T1>T3
C.p1>p4,T2>T3
D.p2>p4,T4>T2
(3)汽车尾气净化的主要原理为:2NO(g)+2CO(g) 2CO2(g) +N2(g);
2CO2(g) +N2(g);
①200K、pPa时,在一个容积为 2L的恒温密闭容器中充入 1.5molNO 和 2.0molCO,开始反应至 2min 时测得 CO 转化率为 30%,则用N2表示的平均反应速率为v(N2)=_________ ;反应达到平衡状态时,测得二氧化碳为 0.8mol,则平衡时的压强为起始压强的_________ 倍(保留两位小数)。
②该反应在低温下能自发进行,该反应的ΔH_____ 0(填“>”、“<”)
(4)一定温度下,将NO2与SO2以体积比 1:2 置于密闭容器中发生反应NO2(g)+SO2(g)⇌ SO3(g)+NO(g),达到平衡时SO3的体积分数为 25%。该反应的平衡常数K=______ 。
(5)利用原电池反应可实现NO2的无害化,总反应为6NO2+ 8NH3=7N2+12H2O,电解质溶液为碱性。工作一段时间后,该电池正极区附近溶液 pH____ (填“变大”、“变小”或“不变”),负极电极反应式为 ____ 。
(1)使用甲醇汽油可以减少汽车尾气对环境的污染。工业上在 200℃和 10MPa 的条件下可用甲烷和氧气通过铜制管道反应制得甲醇,已知一定条件下,CH4和 CH3OH 的燃烧热分别 784kJ/mol 和 628kJ/mol 则 2CH4(g)+O2(g)
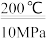 2CH3OH(g) △H=
2CH3OH(g) △H=(2)二甲醚也是清洁能源。用合成气在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g) ⇌CH3OCH3(g) +H2O(g) △H<0。某温度下,,将 2.0molCO(g)和 6.0molH2(g)充入容积为 2L 的密闭容器中,反应到达平衡时, 改变压强和温度,平衡体系中 CH3OCH3(g)的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是

A.p3>p2,T3>T2
B.p1>p3,T1>T3
C.p1>p4,T2>T3
D.p2>p4,T4>T2
(3)汽车尾气净化的主要原理为:2NO(g)+2CO(g)
 2CO2(g) +N2(g);
2CO2(g) +N2(g);①200K、pPa时,在一个容积为 2L的恒温密闭容器中充入 1.5molNO 和 2.0molCO,开始反应至 2min 时测得 CO 转化率为 30%,则用N2表示的平均反应速率为v(N2)=
②该反应在低温下能自发进行,该反应的ΔH
(4)一定温度下,将NO2与SO2以体积比 1:2 置于密闭容器中发生反应NO2(g)+SO2(g)⇌ SO3(g)+NO(g),达到平衡时SO3的体积分数为 25%。该反应的平衡常数K=
(5)利用原电池反应可实现NO2的无害化,总反应为6NO2+ 8NH3=7N2+12H2O,电解质溶液为碱性。工作一段时间后,该电池正极区附近溶液 pH
您最近一年使用:0次



