实验室用含钴废料(主要成分为 ,含有一定量的
,含有一定量的 等)制备钴的氧化物的流程如图。已知:①草酸钴晶体难溶于水②RH为有机物(难电离)。
等)制备钴的氧化物的流程如图。已知:①草酸钴晶体难溶于水②RH为有机物(难电离)。
 ,含有一定量的
,含有一定量的 等)制备钴的氧化物的流程如图。已知:①草酸钴晶体难溶于水②RH为有机物(难电离)。
等)制备钴的氧化物的流程如图。已知:①草酸钴晶体难溶于水②RH为有机物(难电离)。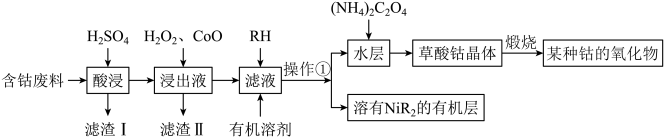
| A.操作①所用的玻璃仪器有漏斗、玻璃棒、烧杯 |
B.滤渣II的成分为 |
C.向操作①后溶有 的有机层中加入硫酸溶液,可重新得到 的有机层中加入硫酸溶液,可重新得到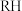 ,该步反应的离子方程式 ,该步反应的离子方程式 |
D.在空气中煅烧 得到 得到 的反应中氧化剂与还原剂的物质的量之比为3:2 的反应中氧化剂与还原剂的物质的量之比为3:2 |
23-24高三上·山东滨州·期中 查看更多[2]
更新时间:2023-12-14 08:55:49
|
相似题推荐
【推荐1】二氧化氯具有杀菌消毒作用,是一种广谱型消毒剂。工业上常用Cl2氧化NaClO2制得,方程式为:Cl2+2NaClO2=2ClO2+2NaCl,下列相关说法正确的是
| A.反应中Cl2被氧化 | B.生成0.1molClO2时,转移0.4mol电子 |
| C.NaClO2是还原剂 | D.还原剂与氧化剂的物质的量之比为1:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】高温下,铝粉与氧化铁的反应可用来焊接钢轨,反应为 ,该反应放出大量的热,下列说法错误的是
,该反应放出大量的热,下列说法错误的是
 ,该反应放出大量的热,下列说法错误的是
,该反应放出大量的热,下列说法错误的是A.16g 的物质的量为0.1mol 的物质的量为0.1mol |
| B.当生成11.2g Fe,此时氧化剂与还原剂的质量之比为27:80 |
C.该反应中, 为氧化产物 为氧化产物 |
| D.进行该反应时,必须做好高温防护措施 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】将一定量Cl2通入体积为40mL、浓度为7.5mol·L-1的苛性钾溶液中,恰好完全反应测得反应后溶液中有三种含氯元素的离子:Cl-、ClO-、ClO3-。下列说法不正确的是
| A.反应过程中氯气消耗0.15mol |
B.当溶液中n(KClO)∶n(KClO3)=2∶1时,该反应的离子方程式为: |
| C.若反应中转移的电子为n mol,则0.15<n<0.3 |
| D.反应生成的ClO-和ClO3-在一定条件下均有氧化性 |
您最近一年使用:0次
【推荐1】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为 、
、 、
、 ,不考虑其他杂质)制备七水合硫酸亚铁
,不考虑其他杂质)制备七水合硫酸亚铁 ,设计了如下流程。下列说法错误的是
,设计了如下流程。下列说法错误的是
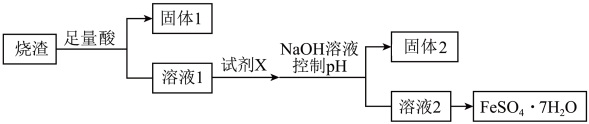
已知: 是酸性氧化物,与酸不反应。
是酸性氧化物,与酸不反应。
 、
、 、
、 ,不考虑其他杂质)制备七水合硫酸亚铁
,不考虑其他杂质)制备七水合硫酸亚铁 ,设计了如下流程。下列说法错误的是
,设计了如下流程。下列说法错误的是
已知:
 是酸性氧化物,与酸不反应。
是酸性氧化物,与酸不反应。A.固体1中一定有 |
B.加入试剂X,可能发生的离子反应为: , ,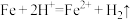 |
C.加入 溶液控制 溶液控制 是为了除去过量的酸 是为了除去过量的酸 |
D.从溶液2中得到 的操作为:蒸发浓缩、冷却结晶 的操作为:蒸发浓缩、冷却结晶 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】习近平主席指出“幸福下会从天降,美好生活靠劳动创造。”下列劳动涉及的化学原理错误的是
| 选项 | 劳动项目 | 化学原理 |
| A | 家务劳动:用热的 溶液洗涤沾有油污的碗筷 溶液洗涤沾有油污的碗筷 | 油脂在碱性条件下水解生成易溶于水的物质 |
| B | 学农活动:帮助果农在储存水果的仓库中放置用酸性高锰酸钾溶液浸泡过的砖瓦 | 乙烯是水果催熟剂,酸性高锰酸钾溶液能除去乙烯 |
| C | 工厂参观:玻璃厂用氢氟酸溶蚀玻璃生产磨砂玻璃 | 氢氟酸具有弱酸性 |
| D | 实践活动:用糯米酿制米酒 | 淀粉水解生成葡萄糖,葡萄糖转变为乙醇 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验中,所采取的分离方法与对应的原理都正确的是
选项 | 目的 | 分离方法 | 原理 |
| A | 分离氢氧化铁胶体和氯离子 | 盐析 | 胶体不能透过半透膜,离子能 |
| B | 分离植物油和水的混合物 | 分液 | 二者互不相溶且密度不同 |
| C | 除去苏打中少量小苏打 | 加热 | 二者的溶解度不同 |
| D | 除去乙酸乙酯中的乙醇和乙酸 | 蒸馏 | 乙酸乙酯与乙醇、乙酸的沸点相差较大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室制备乙酸乙酯,下列实验原理或装置不能达到实验目的的是
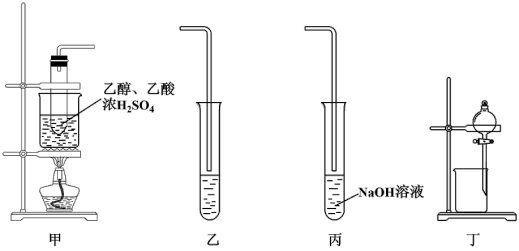

| A.装置甲中水浴加热可使反应物受热均匀,并减少反应物挥发 |
| B.装置乙中使用长导管有利于生成物冷凝 |
| C.装置丙中采用NaOH溶液除去产物中的乙酸和乙醇 |
| D.用装置丁可分离出丙装置中的乙酸乙酯 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列对各实验装置的叙述中,不正确的是


| A.通过装置①向烧瓶中滴加液体时,可以先将颈上的玻璃塞打开或使塞上的凹槽(或小孔)对准瓶颈上的小孔,再拧开分液漏斗下面的活塞 |
| B.装置②的烧杯中装有浓硝酸,在阳光照射下,喷洒有KI-淀粉溶液的白色纸蝴蝶会变成蓝色 |
C.装置③中若X为 ,可用于吸收氨气或者氯化氢,且能防止倒吸 ,可用于吸收氨气或者氯化氢,且能防止倒吸 |
| D.装置④可用于制取、收集氨气,其中蘸有浓氢氧化钠的湿棉花可以有效防止氨气大量逸出污染空气 |
您最近一年使用:0次



