页岩气中含有 、
、 、
、 等气体,是蕴藏于页岩层可供开采的天然气资源。页岩气的有效利用需要处理其中所含的
等气体,是蕴藏于页岩层可供开采的天然气资源。页岩气的有效利用需要处理其中所含的 和
和 。
。
Ⅰ.Ni催化 加
加 形成
形成 ,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中
,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中 的百分含量及
的百分含量及 的转化率随温度的变化如图2所示。
的转化率随温度的变化如图2所示。

(1)260℃时生成主要产物所发生反应的化学方程式为___________ 。
(2)温度高于320℃, 的转化率下降的原因是
的转化率下降的原因是___________ 。
Ⅱ. 的处理:
的处理: 可用作脱除
可用作脱除 气体的脱硫剂。
气体的脱硫剂。 脱硫和
脱硫和 再生的可能反应机理如图3所示。
再生的可能反应机理如图3所示。
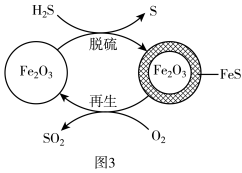
(3)再生时需控制通入 的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是
的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是___________ 。
(4)脱硫剂再生时可以使用水汽代替 。700℃条件下,用水汽代替
。700℃条件下,用水汽代替 再生时,生成
再生时,生成 、
、 和
和 ,
, 也可作脱硫剂。
也可作脱硫剂。
①写出水汽作用条件下脱硫剂再生反应的化学方程式:___________ 。
②用 再生时会生成污染性气体
再生时会生成污染性气体 ,用水汽再生时会排放出有毒的
,用水汽再生时会排放出有毒的 ,采用
,采用 和水汽混合再生的方法,可以将产生的
和水汽混合再生的方法,可以将产生的 和
和 转化为S单质。则为不排放出
转化为S单质。则为不排放出 和
和 ,理论上
,理论上 和水汽的体积比应为
和水汽的体积比应为___________ (写出计算过程)。
 、
、 、
、 等气体,是蕴藏于页岩层可供开采的天然气资源。页岩气的有效利用需要处理其中所含的
等气体,是蕴藏于页岩层可供开采的天然气资源。页岩气的有效利用需要处理其中所含的 和
和 。
。Ⅰ.Ni催化
 加
加 形成
形成 ,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中
,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中 的百分含量及
的百分含量及 的转化率随温度的变化如图2所示。
的转化率随温度的变化如图2所示。
(1)260℃时生成主要产物所发生反应的化学方程式为
(2)温度高于320℃,
 的转化率下降的原因是
的转化率下降的原因是Ⅱ.
 的处理:
的处理: 可用作脱除
可用作脱除 气体的脱硫剂。
气体的脱硫剂。 脱硫和
脱硫和 再生的可能反应机理如图3所示。
再生的可能反应机理如图3所示。
(3)再生时需控制通入
 的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是
的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是(4)脱硫剂再生时可以使用水汽代替
 。700℃条件下,用水汽代替
。700℃条件下,用水汽代替 再生时,生成
再生时,生成 、
、 和
和 ,
, 也可作脱硫剂。
也可作脱硫剂。①写出水汽作用条件下脱硫剂再生反应的化学方程式:
②用
 再生时会生成污染性气体
再生时会生成污染性气体 ,用水汽再生时会排放出有毒的
,用水汽再生时会排放出有毒的 ,采用
,采用 和水汽混合再生的方法,可以将产生的
和水汽混合再生的方法,可以将产生的 和
和 转化为S单质。则为不排放出
转化为S单质。则为不排放出 和
和 ,理论上
,理论上 和水汽的体积比应为
和水汽的体积比应为
更新时间:2023-10-14 10:59:34
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】某电镀厂产生的废水经预处理后含有 和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
①常温下,物质的Ksp数据:
②Cr(OH)3性质与Al(OH)3相似。
③设H2S平衡浓度为1.0×10-6mol/L,已知H2S的K1=1.0×10-7,K2=7.0×10-15。
回答下列问题:
(1)还原池中溶液调pH___________ (填“能”或“否")使用盐酸。
(2)还原池中有Cr3+和CO2气体生成,反应的离子方程式为___________ 。
(3)沉淀池1中溶液的pH应为___________ 时才能使c(Cr3+)降至10-5mol/L,若溶液pH过高将会导致___________ 沉铬率下降。
(4)沉淀池2中加入的Na2S溶液呈碱性,原因是___________ (用主要反应的离子方程式表示),根据溶度积常数可确定沉淀2为___________ 。
(5)沉淀池3中沉淀结束,pH=7时,溶液中主要离子是___________ 。
 和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。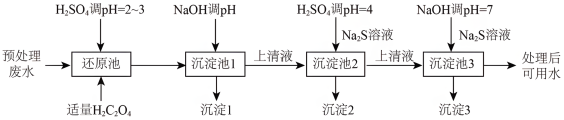
①常温下,物质的Ksp数据:
| 物质 | Cr(OH)3 | CuS | NiS |
| Ksp | 1×10-32 | 6.3×10-36 | 3.0×10-19 |
③设H2S平衡浓度为1.0×10-6mol/L,已知H2S的K1=1.0×10-7,K2=7.0×10-15。
回答下列问题:
(1)还原池中溶液调pH
(2)还原池中有Cr3+和CO2气体生成,反应的离子方程式为
(3)沉淀池1中溶液的pH应为
(4)沉淀池2中加入的Na2S溶液呈碱性,原因是
(5)沉淀池3中沉淀结束,pH=7时,溶液中主要离子是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中ClO2的质量分数高于30%等均有可能引起爆炸,易与碱液反应生成盐和水。
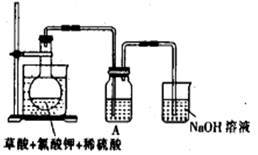
(1)某研究小组设计如图所示实验制备ClO2溶液,其反应的化学方程式为
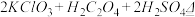
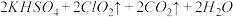
①在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其温度保持在60~80℃之间。控制温度的目的是_________________ ,图示装置中缺少的一种必须的玻璃仪器是____
②装置A用于溶解产生的二氧化氯气体,其中最好盛放______ (填字母)。
A.20mL 60℃的温水 B.100mL冰水
C.100mL饱和食盐水 D.100mL沸水
③在烧瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热,反应后生成ClO2的质量为_________________
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子( )。饮用水中ClO2、
)。饮用水中ClO2、 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:
步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的Na2S2O3溶液滴定至终点;
步骤5:再调节溶液的pH≤2.0;
步骤6:继续用相同浓度的Na2S2O3溶液滴定至终点。
①步骤1中若要量取20.00mL水样,则应选用的仪器是______________
②步骤1~4的目的是测定水样中ClO2的含量,其反应的化学方程式为:
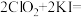
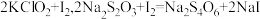 ,则步骤4中加入的指示剂为
,则步骤4中加入的指示剂为____________ ,滴定达到终点时溶液的颜色变化为___________________
③步骤5的目的是使I-将溶液中的 还原为Cl-以测定其含量,该反应的离子方程式为:
还原为Cl-以测定其含量,该反应的离子方程式为:__________________________________ ;
④若饮用水中ClO2-的含量超标,可向其中加入适量的 将ClO2-还原为Cl-,则该反应的氧化产物为
将ClO2-还原为Cl-,则该反应的氧化产物为______________ (填化学式)

(1)某研究小组设计如图所示实验制备ClO2溶液,其反应的化学方程式为
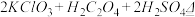
①在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其温度保持在60~80℃之间。控制温度的目的是
②装置A用于溶解产生的二氧化氯气体,其中最好盛放
A.20mL 60℃的温水 B.100mL冰水
C.100mL饱和食盐水 D.100mL沸水
③在烧瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热,反应后生成ClO2的质量为
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(
 )。饮用水中ClO2、
)。饮用水中ClO2、 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的Na2S2O3溶液滴定至终点;
步骤5:再调节溶液的pH≤2.0;
步骤6:继续用相同浓度的Na2S2O3溶液滴定至终点。
①步骤1中若要量取20.00mL水样,则应选用的仪器是
②步骤1~4的目的是测定水样中ClO2的含量,其反应的化学方程式为:
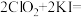
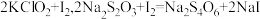 ,则步骤4中加入的指示剂为
,则步骤4中加入的指示剂为③步骤5的目的是使I-将溶液中的
 还原为Cl-以测定其含量,该反应的离子方程式为:
还原为Cl-以测定其含量,该反应的离子方程式为:④若饮用水中ClO2-的含量超标,可向其中加入适量的
 将ClO2-还原为Cl-,则该反应的氧化产物为
将ClO2-还原为Cl-,则该反应的氧化产物为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】某实验室利用 和
和 反应合成硫酰氯(
反应合成硫酰氯( ),并对
),并对 和HClO的酸性强弱进行探究。已知
和HClO的酸性强弱进行探究。已知 的沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl,100℃以上容易分解。实验室合成
的沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl,100℃以上容易分解。实验室合成 的原理:
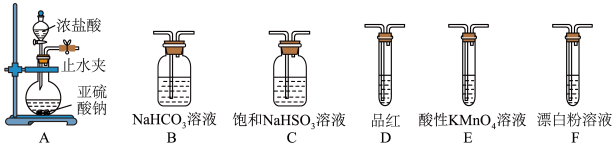
的原理: ,反应会放热。实验装置如图所示,请回答下列问题:
,反应会放热。实验装置如图所示,请回答下列问题:_____
(2)装置戊上方分液漏斗中最好选用_____ (填字母)。
a.蒸馏水 b.饱和食盐水 c.浓氢氧化钠溶液 d. 盐酸
盐酸
(3)装置乙和丁盛放的试剂均是_____ (写名称)。
(4)装置丙放置在冰水浴中的原因是_____ 。
(5) 和水反应的化学方程式为
和水反应的化学方程式为_____
(6)选用下面的装置探究酸性: ,其连接顺序为A→C→B→E→D→Fa'装置E中反应的离子方程式为
,其连接顺序为A→C→B→E→D→Fa'装置E中反应的离子方程式为_____ ,能证明 的酸性强于HClO的实验现象为
的酸性强于HClO的实验现象为_____ (已知: 酸性大于
酸性大于 )
)
 和
和 反应合成硫酰氯(
反应合成硫酰氯( ),并对
),并对 和HClO的酸性强弱进行探究。已知
和HClO的酸性强弱进行探究。已知 的沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl,100℃以上容易分解。实验室合成
的沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl,100℃以上容易分解。实验室合成 的原理:
的原理: ,反应会放热。实验装置如图所示,请回答下列问题:
,反应会放热。实验装置如图所示,请回答下列问题: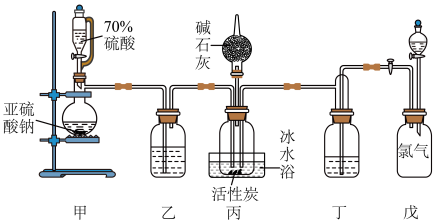
(2)装置戊上方分液漏斗中最好选用
a.蒸馏水 b.饱和食盐水 c.浓氢氧化钠溶液 d.
 盐酸
盐酸(3)装置乙和丁盛放的试剂均是
(4)装置丙放置在冰水浴中的原因是
(5)
 和水反应的化学方程式为
和水反应的化学方程式为(6)选用下面的装置探究酸性:
 ,其连接顺序为A→C→B→E→D→Fa'装置E中反应的离子方程式为
,其连接顺序为A→C→B→E→D→Fa'装置E中反应的离子方程式为 的酸性强于HClO的实验现象为
的酸性强于HClO的实验现象为 酸性大于
酸性大于 )
)
您最近一年使用:0次
【推荐1】亚硝酰氯(NOCl)是有机合成中的重要试剂。实验室中可用如下反应合成亚硝酰氯。
反应I:Cl2(g) + 2NO(g) 2NOCl(g)
2NOCl(g)
反应II:2CuCl(s) 2CuCl(s)+Cl2(g)
2CuCl(s)+Cl2(g) 
(1)T℃下,向某真空恒容密闭容器中加入足量的 (s)并充入一定量的NO(g),发生反应I和反应II,测得起始压强为b kPa,达到平衡时NOCl(g)的压强为c kPa,若此温度下,反应II的平衡常数
(s)并充入一定量的NO(g),发生反应I和反应II,测得起始压强为b kPa,达到平衡时NOCl(g)的压强为c kPa,若此温度下,反应II的平衡常数 ,则平衡时NO的转化率为
,则平衡时NO的转化率为_______ ;该温度下,反应I的平衡常数
_______ 。(用气体物质的平衡分压代替平衡浓度,分压=总压×物质的量分数,用含a、b、c的代数式表示)
(2)反应 的速率方程式可表示为
的速率方程式可表示为 ,
, ,其中
,其中 、
、 代表正、逆反应的速率常数,其与温度、催化剂等有关,与浓度无关。已知:pk=-lgk。如图所示有2条直线分别代表p
代表正、逆反应的速率常数,其与温度、催化剂等有关,与浓度无关。已知:pk=-lgk。如图所示有2条直线分别代表p 、p
、p 与
与 的关系,其中代表p
的关系,其中代表p 与
与 关系的直线是
关系的直线是_______ (填字母),理由是_______ 。

(3)一定条件下向恒容密闭容器中按一定比例 充入NO(g)和
充入NO(g)和 (g)发生反应I,平衡时体系中体积分数
(g)发生反应I,平衡时体系中体积分数 (NOCl)随
(NOCl)随 的变化如图所示,则NO转化率最大的是
的变化如图所示,则NO转化率最大的是_______ (填“B”或“C”)点,当 时,表示平衡状态时的
时,表示平衡状态时的 (NOCl)可能是
(NOCl)可能是_______ (填“D”“E”或“F”)点。

反应I:Cl2(g) + 2NO(g)
 2NOCl(g)
2NOCl(g)
反应II:2CuCl(s)
 2CuCl(s)+Cl2(g)
2CuCl(s)+Cl2(g) 
(1)T℃下,向某真空恒容密闭容器中加入足量的
 (s)并充入一定量的NO(g),发生反应I和反应II,测得起始压强为b kPa,达到平衡时NOCl(g)的压强为c kPa,若此温度下,反应II的平衡常数
(s)并充入一定量的NO(g),发生反应I和反应II,测得起始压强为b kPa,达到平衡时NOCl(g)的压强为c kPa,若此温度下,反应II的平衡常数 ,则平衡时NO的转化率为
,则平衡时NO的转化率为
(2)反应
 的速率方程式可表示为
的速率方程式可表示为 ,
, ,其中
,其中 、
、 代表正、逆反应的速率常数,其与温度、催化剂等有关,与浓度无关。已知:pk=-lgk。如图所示有2条直线分别代表p
代表正、逆反应的速率常数,其与温度、催化剂等有关,与浓度无关。已知:pk=-lgk。如图所示有2条直线分别代表p 、p
、p 与
与 的关系,其中代表p
的关系,其中代表p 与
与 关系的直线是
关系的直线是
(3)一定条件下向恒容密闭容器中按一定比例
 充入NO(g)和
充入NO(g)和 (g)发生反应I,平衡时体系中体积分数
(g)发生反应I,平衡时体系中体积分数 (NOCl)随
(NOCl)随 的变化如图所示,则NO转化率最大的是
的变化如图所示,则NO转化率最大的是 时,表示平衡状态时的
时,表示平衡状态时的 (NOCl)可能是
(NOCl)可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命。
(1)以甲醇为原料制取高纯H2是重要研究方向。甲醇水蒸气重整制氢主要发生以下两个反应:
主反应:CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H=+49 kJ•mol-1
CO2(g)+3H2(g) △H=+49 kJ•mol-1
副反应:H2(g)+CO2(g) CO(g)+H2O(g) △H=+41 kJ•mol-1
CO(g)+H2O(g) △H=+41 kJ•mol-1
①甲醇在催化剂作用下裂解可得到H2和CO,则该反应的化学方程式为_________________________ ,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是_________________________ 。
②分析适当增大水醇比(nH2O∶nCH3OH)对甲醇水蒸气重整制氢的好处_________________________ 。
③某温度下,将nH2O∶nCH3OH =1∶1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为_________________________ 。(忽略副反应)
(2)工业常用CH4 与水蒸气在一定条件下来制取H2,其原理为:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+203kJ·mol-1
①该反应的逆反应速率表达式为; V逆=k·c(CO)·c3(H2),k为速率常数,在某温度下,测得实验数据如表:
由上述数据可得该温度下,上述反应的逆反应速率常数k 为__________ L3·mol-3·min-1。
②在体积为3L的密闭容器中通入物质的量均为3mol 的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示,则压强Pl_____ P2(填“大于”或“小于”)温度T3_______ T4(填“大于”或“小于”);压强为P1时,在N点; v正_______ v逆(填“大于”或“小于”或“等于”)。求N点对应温度下该反应的平衡常数 K=_____________________ 。

(1)以甲醇为原料制取高纯H2是重要研究方向。甲醇水蒸气重整制氢主要发生以下两个反应:
主反应:CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) △H=+49 kJ•mol-1
CO2(g)+3H2(g) △H=+49 kJ•mol-1副反应:H2(g)+CO2(g)
 CO(g)+H2O(g) △H=+41 kJ•mol-1
CO(g)+H2O(g) △H=+41 kJ•mol-1①甲醇在催化剂作用下裂解可得到H2和CO,则该反应的化学方程式为
②分析适当增大水醇比(nH2O∶nCH3OH)对甲醇水蒸气重整制氢的好处
③某温度下,将nH2O∶nCH3OH =1∶1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为
(2)工业常用CH4 与水蒸气在一定条件下来制取H2,其原理为:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+203kJ·mol-1
①该反应的逆反应速率表达式为; V逆=k·c(CO)·c3(H2),k为速率常数,在某温度下,测得实验数据如表:
| CO浓度(mol·L-1) | H2浓度(mol·L-1) | 逆反应速率(mol·L-1·min-1) |
| 0.05 | C1 | 4.8 |
| c2 | C1 | 19.2 |
| c2 | 0.15 | 8.1 |
由上述数据可得该温度下,上述反应的逆反应速率常数k 为
②在体积为3L的密闭容器中通入物质的量均为3mol 的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示,则压强Pl

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】甲烷、甲醇( )、甲醛(
)、甲醛( )等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。
)等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。
(1)工业上合成甲醇的反应: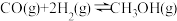 ,在一个恒容密闭容器中,充入
,在一个恒容密闭容器中,充入 和
和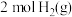 发生反应,测得平衡时
发生反应,测得平衡时 的体积分数与温度、压强的关系如图所示:
的体积分数与温度、压强的关系如图所示:
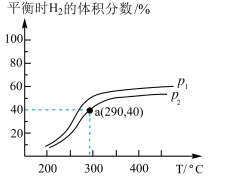
①压强
_____  (填“大于”或“小于”),该反应达到平衡的标志是
(填“大于”或“小于”),该反应达到平衡的标志是_____ (填字母)。
A.反应速率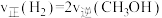
B.容器内 和
和 物质的量之比为
物质的量之比为
C.混合气体的密度不再变化
D.混合气体的平均摩尔质量不再变化
②a点条件下, 的平衡转化率为
的平衡转化率为_____ (填分数),该温度下达到平衡后,在容积不变的条件下再充入 和
和 ,平衡
,平衡_____ (填“正向”、“逆向”或“不”)移动,新平衡时的逆反应速率_____ (填“大于”、“等于”或“小于”)原平衡。
(2)工业上用甲醇可以制备甲胺(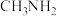 ),甲胺与氨在水中的电离方式相似。则甲胺在水中的电离方程式为
),甲胺与氨在水中的电离方式相似。则甲胺在水中的电离方程式为_____ ,常温下,反应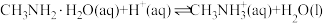 的平衡常数
的平衡常数 ,
,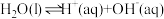 的平衡常数
的平衡常数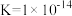 。该温度下,甲胺的电离常数
。该温度下,甲胺的电离常数
_____ 。
(3)电喷雾电离等方法得到的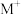 (
(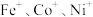 等)与
等)与 反应可得
反应可得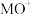 。
。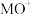 与
与 反应能高选择性地生成甲醇。分别在
反应能高选择性地生成甲醇。分别在 和
和 下(其他反应条件相同)进行反应
下(其他反应条件相同)进行反应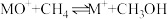 ,结果如图所示:
,结果如图所示:
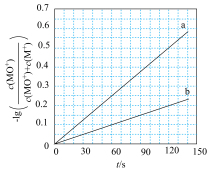
 ,
,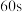 时
时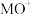 的转化率为
的转化率为_____ 。
 )、甲醛(
)、甲醛( )等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。
)等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。(1)工业上合成甲醇的反应:
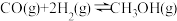 ,在一个恒容密闭容器中,充入
,在一个恒容密闭容器中,充入 和
和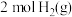 发生反应,测得平衡时
发生反应,测得平衡时 的体积分数与温度、压强的关系如图所示:
的体积分数与温度、压强的关系如图所示:
①压强

 (填“大于”或“小于”),该反应达到平衡的标志是
(填“大于”或“小于”),该反应达到平衡的标志是A.反应速率
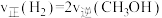
B.容器内
 和
和 物质的量之比为
物质的量之比为
C.混合气体的密度不再变化
D.混合气体的平均摩尔质量不再变化
②a点条件下,
 的平衡转化率为
的平衡转化率为 和
和 ,平衡
,平衡(2)工业上用甲醇可以制备甲胺(
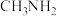 ),甲胺与氨在水中的电离方式相似。则甲胺在水中的电离方程式为
),甲胺与氨在水中的电离方式相似。则甲胺在水中的电离方程式为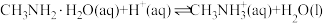 的平衡常数
的平衡常数 ,
,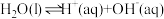 的平衡常数
的平衡常数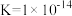 。该温度下,甲胺的电离常数
。该温度下,甲胺的电离常数
(3)电喷雾电离等方法得到的
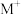 (
(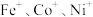 等)与
等)与 反应可得
反应可得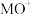 。
。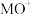 与
与 反应能高选择性地生成甲醇。分别在
反应能高选择性地生成甲醇。分别在 和
和 下(其他反应条件相同)进行反应
下(其他反应条件相同)进行反应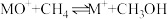 ,结果如图所示:
,结果如图所示:
 ,
,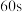 时
时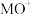 的转化率为
的转化率为
您最近一年使用:0次



