 和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。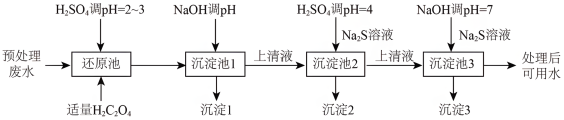
①常温下,物质的Ksp数据:
| 物质 | Cr(OH)3 | CuS | NiS |
| Ksp | 1×10-32 | 6.3×10-36 | 3.0×10-19 |
③设H2S平衡浓度为1.0×10-6mol/L,已知H2S的K1=1.0×10-7,K2=7.0×10-15。
回答下列问题:
(1)还原池中溶液调pH
(2)还原池中有Cr3+和CO2气体生成,反应的离子方程式为
(3)沉淀池1中溶液的pH应为
(4)沉淀池2中加入的Na2S溶液呈碱性,原因是
(5)沉淀池3中沉淀结束,pH=7时,溶液中主要离子是
相似题推荐
 、有机物等)中回收钌的工艺流程如下:
、有机物等)中回收钌的工艺流程如下: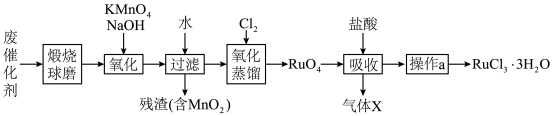
 的沸点为40℃,温度高于108℃分解。②氧化性:
的沸点为40℃,温度高于108℃分解。②氧化性: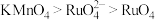
(1)“煅烧”的目的是
(2)“氧化”过程需在650℃下熔融反应5小时。
①单质Ru被氧化为
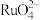 的化学方程式为
的化学方程式为②
 固体过量会导致钌的回收率降低,原因是
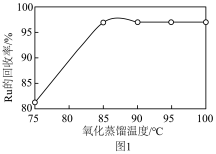
固体过量会导致钌的回收率降低,原因是(3)“氧化蒸馏”时,测得钌的回收率随温度变化曲线如图1所示。工业上保证钌回收率较高的情况下,选择在95℃进行氧化蒸馏的原因是
(5)钌多活性位点催化剂(
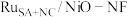 )可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。
)可用于催化水的多步碱性析氢反应。该催化剂存在钌单原子、钌团簇、NiO三种活性位点,不同位点的催化特点不同。图2为反应历程中微粒在不同位点的自由能的变化,其中吸附在催化剂表面的微粒用*标注。
②催化剂的活性位点在催化过程中的主要作用是
③分析图2-a推测
 的“吸附解离”主要发生在
的“吸附解离”主要发生在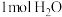 参与该过程,则变化的能量为
参与该过程,则变化的能量为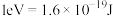 )。
)。④分析图2-b并说明
 的脱附主要发生在NiO表面的原因
的脱附主要发生在NiO表面的原因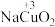 )的制备和性质。
)的制备和性质。资料:高铜酸钠为棕黑色固体,难溶于水。
实验I.向
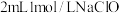 溶液中滴加
溶液中滴加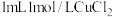 溶液,迅速产生蓝绿色沉淀,振荡后得到棕黑色的浊液a,将其等分成2份。
溶液,迅速产生蓝绿色沉淀,振荡后得到棕黑色的浊液a,将其等分成2份。(1)蓝绿色沉淀中含有
 ,用离子方程式表示
,用离子方程式表示 溶液显碱性的原因:
溶液显碱性的原因:(2)探究棕黑色沉淀的组成。
实验II.将一份浊液a过滤、洗涤、干燥,得到固体b;取少量固体b,滴加稀
 ,沉淀溶解,有气泡产生,得到蓝色溶液。
,沉淀溶解,有气泡产生,得到蓝色溶液。①另取少量固体b进行实验,证实了
 中钠元素的存在,实验操作的名称是
中钠元素的存在,实验操作的名称是②进一步检验,棕黑色固体是
 ,
, 与稀
与稀 反应的离子方程式是
反应的离子方程式是(3)探究实验条件对
 制备的影响。
制备的影响。实验III.向另一份浊液a中继续滴加
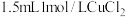 溶液,沉淀由棕黑色变为蓝绿色,溶液的
溶液,沉淀由棕黑色变为蓝绿色,溶液的 约为5,有
约为5,有 产生。
产生。①对
 的来源,甲同学认为是
的来源,甲同学认为是 和
和 反应生成了
反应生成了 ,乙同学认为该说法不严谨,提出了生成
,乙同学认为该说法不严谨,提出了生成 的其他原因:
的其他原因:②探究“继续滴加
 溶液,
溶液, 能氧化
能氧化 的原因。
的原因。ⅰ.提出假设1:
 增大,
增大, 的还原性增强,实验证明假设成立,操作和现象是:取少量
的还原性增强,实验证明假设成立,操作和现象是:取少量 固体于试管中,
固体于试管中,ⅱ.提出假设2:
(4)改进实验方案,进行实验。
实验IV,向
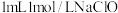 溶液中滴加
溶液中滴加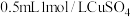 溶液,迅速生成蓝色沉淀,振荡后得到棕黑色浊液。浊液放置过程中,沉淀表面缓慢产生气泡并出现蓝色固体,该气体不能使湿润的淀粉
溶液,迅速生成蓝色沉淀,振荡后得到棕黑色浊液。浊液放置过程中,沉淀表面缓慢产生气泡并出现蓝色固体,该气体不能使湿润的淀粉 试纸变蓝。
试纸变蓝。 放置过程中产生气体的化学方程式是
放置过程中产生气体的化学方程式是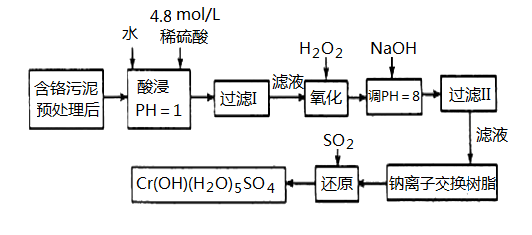
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | — | 一 | — |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 9 (>9溶解) |
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏大的操作是
a.转移溶液时,没有等溶液冷却至室温b.量取浓硫酸时,俯视刻度线
c.当容量瓶中液体占容积2/3左右时,未振荡摇匀d.定容时俯视刻度线
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42-或Cr2O72-),以便于与杂质离子分离;另一方面是
(4)调节溶液的pH=8除去的杂质离子是
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是
(6)通SO2气体时,其化学方程式为

①取mg甲的晶体溶于蒸馏水,配成500 mL溶液;
②取少量甲溶液于试管中,逐滴滴入Ba(OH)2溶液,生成沉淀的物质的量与滴入Ba(OH)2溶液体积的关系如图所示;
③取20 mL甲溶液于试管中,加入过量NaOH溶液后加热并收集产生的气体,然后折算成标准状况下的体积为224 mL。
回答下列问题:
(1)D在元素周期表中的位置为
(2)经测定晶体甲的摩尔质量为453 g·mol-1,其中阳离子和阴离子物质的量之比为1:1。 则晶体甲的化学式为
(3)图象中V(Oa):V(ab):V(bc)=
(4)写出ab段发生反应的离子方程式:
(5)配成的甲溶液物质的量浓度是
 、
、 、
、 )制备软磁性材料
)制备软磁性材料 。主要转化流程如下:
。主要转化流程如下:
①酸浸。写出烧渣酸浸时
 与稀硫酸反应的化学方程式
与稀硫酸反应的化学方程式②还原。向“酸浸”后的溶液中加入过量铁粉,使
 完全转化为
完全转化为 ,该过程除生成
,该过程除生成 外,还会生成
外,还会生成 是否还原完全的实验操作是
是否还原完全的实验操作是③除杂。向“还原”后滤液中加入NaOH溶液,调节pH为
 除去完全。[已知:
除去完全。[已知: 时
时 沉淀完全,
沉淀完全, 时
时 开始沉淀。]
开始沉淀。]④结晶。结合题图所示的绿矾溶解度曲线,补充完整获得
 晶体的实验操作。向
晶体的实验操作。向 溶液中再加入稀硫酸酸化,
溶液中再加入稀硫酸酸化, 晶体。
晶体。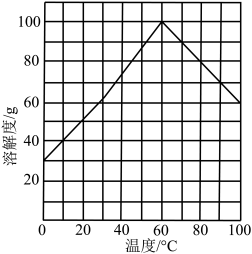
 。将
。将 溶液与氨水
溶液与氨水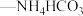 混合溶液中的一种加入到三颈瓶中(装置见图),通过分液漏斗缓慢滴加另一种溶液,充分反应,过滤。
混合溶液中的一种加入到三颈瓶中(装置见图),通过分液漏斗缓慢滴加另一种溶液,充分反应,过滤。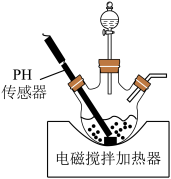
 的离子方程式为
的离子方程式为②生成的
 沉淀需“洗涤完全”,检验方法是
沉淀需“洗涤完全”,检验方法是(3)制
 。将纯净的
。将纯净的 放入管式炉内煅烧2h,获得产品
放入管式炉内煅烧2h,获得产品 。下图为其他条件相同时不同煅烧温度对产品中
。下图为其他条件相同时不同煅烧温度对产品中 质量分数的影响,当煅烧温度高于800℃时,产品中
质量分数的影响,当煅烧温度高于800℃时,产品中 质量分数降低,铁元素质量分数升高,其可能原因是
质量分数降低,铁元素质量分数升高,其可能原因是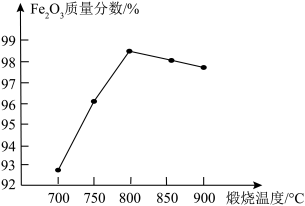
(1)在A、C、F三种溶液中,水的电离程度由大到小的顺序为
(2)常温下,将等物质的量浓度,等体积的B、E两溶液相混合,所得混合溶液的pH
(3)常温下,若C溶液中c(OH-)与D溶液中c(H+)相等,将二者等体积混合,所得混合溶液的pH
(4)常温下,若B溶液中c(H+)与C溶液中的c(OH-)相等,现将B、C溶液都稀释10倍,稀释后B溶液的pH值用pHB表示,C溶液的pH值用pHC表示,则pHB+pHC
(1)常温下浓度均为
 的8种溶液:①
的8种溶液:① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液;④
溶液;④ 溶液;⑤
溶液;⑤ 溶液;⑥
溶液;⑥ 溶液;⑦
溶液;⑦ 溶液;⑧
溶液;⑧ 溶液,这些溶液的pH由小到大的顺序是
溶液,这些溶液的pH由小到大的顺序是(2)常温下,
 的盐酸和
的盐酸和 的
的 溶液中,水电离出的
溶液中,水电离出的 分别为
分别为 和
和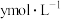 ,二者的关系正确的是
,二者的关系正确的是a.
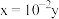 b.
b.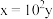 c.
c. d.
d.
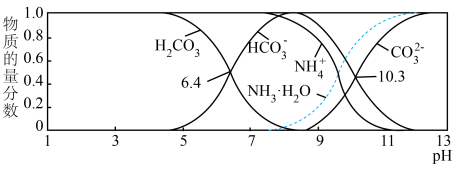
(3)室温下,测得用氨水吸收
 时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液
时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液 ,则溶液中
,则溶液中 =
= )。
)。
(4)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体
 ,其产物之一是
,其产物之一是 。已知常温下碳酸的电离常数
。已知常温下碳酸的电离常数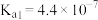 ,
,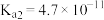 ,
, 的电离常数
的电离常数 ,则所得
,则所得 溶液中
溶液中
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(5)常温下,将
 的氨水溶液加水稀释,下列数值一定减小的是____________(填字母)。
的氨水溶液加水稀释,下列数值一定减小的是____________(填字母)。A. | B. | C. | D. |
(6)某温度下,测得
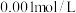 的
的 溶液中水电离出的
溶液中水电离出的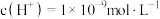 ,将
,将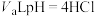 溶液和
溶液和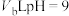 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
(7)常温下,若在
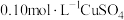 溶液中加入
溶液中加入 稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的
稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的 时,
时,
 。
。
Ⅰ.化学家研究发现,SbF5能将MnF4从离子[MnF6]2-的盐中反应得到,SbF5转化成稳定离子[SbF6]-的盐。而MnF4很不稳定,受热易分解为MnF3和F2。根据以上研究写出以K2MnF6和SbF5为原料,在 423 K 的温度下制备F2的化学方程式:

现代工业以电解熔融的氟氢化钾(KHF2)和氟化氢(HF)混合物制备氟单质,电解制氟装置如图所示。
已知KHF2是一种酸式盐,写出阴极上发生的电极反应式
Ⅱ.①卤化氢的熔沸点随相对分子质量增加而升高,而HF熔沸点高于HCl的原因是
②已知25 ℃时,氢氟酸(HF)的电离平衡常数Ka=3.6×10-4。
某pH=2的氢氟酸溶液,由水电离出的c(H+)=
③又已知25 ℃时,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol/L HF溶液中加入 1 L 0.2 mol/L CaCl2 溶液,通过列式计算说明是否有沉淀产生:

请回答下列问题:
(1)操作I的名称
(2)已知:VOSO4(水层)+2HA(有机层)
 VOA2(有机层)+H2SO4(水层)。步骤②中必须加入适量碱,其原因是;步骤③中反萃取所用的试剂X为
VOA2(有机层)+H2SO4(水层)。步骤②中必须加入适量碱,其原因是;步骤③中反萃取所用的试剂X为(3)步骤④中的反应的离子方程式:ClO
 +
+(4)沉淀Y的摩尔质量为598g·mol—1,且仅含有四种元素。取59.8g沉淀Y的样品充分焙烧,得到产品54.6g,将产生的气体通过足量碱石灰,碱石灰增重1.8g,剩余的气体再通入稀硫酸被完全吸收。通过计算确定沉淀Y的化学式为
(5)钒沉淀率和溶液pH之间关系如下

⑤中加入氨水,调节溶液的最佳pH为;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<。(已知:25℃时,Ksp[Fe(OH)3]=2.6×l0—39)
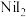 )可用于制陶瓷等。以废镍催化剂(主要成分是Ni,含少量Zn、Fe、CaO、
)可用于制陶瓷等。以废镍催化剂(主要成分是Ni,含少量Zn、Fe、CaO、 等杂质)为原料制备碘化镍的流程如下:
等杂质)为原料制备碘化镍的流程如下: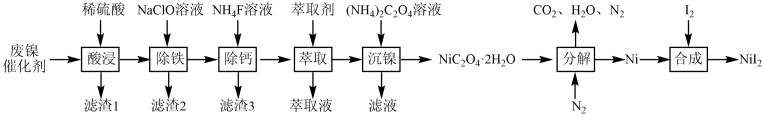
 。
。回答下列问题:
(1)滤渣1的成分是
 、
、(2)“除铁”中可通过先加入
 溶液再加入NiO替代NaClO溶液,
溶液再加入NiO替代NaClO溶液, 的作用是
的作用是(3)“除钙”时,为确保滤液中
 ,溶液中
,溶液中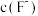 至少为
至少为 (保留两位有效数字)。
(保留两位有效数字)。(4)“萃取”过程主要除去的金属杂质离子是
(5)“分解”过程中通入
 的作用是
的作用是(6)在空气中加热一定量的
 (相对分子质量为183)晶体,测得固体失重率(固体失重率=
(相对分子质量为183)晶体,测得固体失重率(固体失重率= )与温度的关系如图所示,300~400℃时发生反应的化学方程式为
)与温度的关系如图所示,300~400℃时发生反应的化学方程式为
| NH3•H2O | Kb=1.8×10-5 |
| H2CO3 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
| HF | Ka=6.8×10-4 |
| H2S | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| H2O | Kw=10-14 |
| Cu(OH)2 | Ksp=2.2×10-20 |
| Fe(OH)3 | Ksp=4.0×10-38 |
| CuS | Ksp=6.3×10-36 |
| FeS | Ksp=3.6×10-18 |
| 常用对数 | lg2=0.3 lg2.2=0.34 lg3=0.48 |
(1)NH4F溶液显
(2)NH4HCO3 溶液与少量NaOH溶液反应时,
(3)①反应 CuS(s) + H2SO4(aq)⇌H2S(aq) + CuSO4(aq)的 K=
②反应 CuS(s)+Fe2+(aq)⇌FeS(s)+Cu2+(aq)的 K=
③由计算结果可以知道实验室制备H2S气体应选用
(4)除去废水中的Cu2+使用过量的FeS固体的优点有:
①可以除去废水中的Cu2+,过量的FeS和生成的CuS可以通过过滤一并除去;
②




