Cu(II)可形成多种配合物,呈现出多样化的性质和用途。
(1)向盛有硫酸铜水溶液的试管中加入少量氨水生成蓝色沉淀,继续加入过量氨水,得到深蓝色透明溶液,最后向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
① 产生蓝色沉淀的离子方程式是___________ 。
② [Cu(NH3)4]SO4在水中电离的方程式是___________ 。
(2)如下图所示,Cu(II)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热致变色材料,在温度传感器、变色涂料等领域应用广泛。

①Cu2+的价层电子排布式为___________ 。
②A中氮原子与其它原子(或离子)之间存在的作用力类型有___________ ,氢原子与其它原子之间存在的作用力类型有___________ 。
③已知:当Cu(II)配合物A和B配位构型由八面体转变为四方平面时,吸收光谱蓝移,配合物颜色紫色变为橙色。
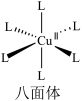
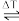

想将配合物的颜色由紫色调整为橙色,需要进行的简单操作为___________ 。
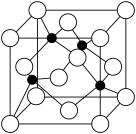
(3)CuCl2和CuCl是铜常见的两种氯化物,下面示意图表示的是___________ 的晶胞。已知晶胞的边长为a pm,阿伏伽德罗常数为NA mol-1,则该晶体的密度为___________ g·cm-3。
(1)向盛有硫酸铜水溶液的试管中加入少量氨水生成蓝色沉淀,继续加入过量氨水,得到深蓝色透明溶液,最后向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
① 产生蓝色沉淀的离子方程式是
② [Cu(NH3)4]SO4在水中电离的方程式是
(2)如下图所示,Cu(II)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热致变色材料,在温度传感器、变色涂料等领域应用广泛。

①Cu2+的价层电子排布式为
②A中氮原子与其它原子(或离子)之间存在的作用力类型有
③已知:当Cu(II)配合物A和B配位构型由八面体转变为四方平面时,吸收光谱蓝移,配合物颜色紫色变为橙色。

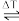

想将配合物的颜色由紫色调整为橙色,需要进行的简单操作为
(3)CuCl2和CuCl是铜常见的两种氯化物,下面示意图表示的是

更新时间:2023-10-28 09:48:34
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
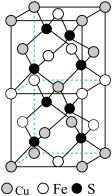
【推荐1】黄铜矿(CuFeS2)是炼铜的主要矿物,在野外很容易被误会为黄金,因此被称为愚人金。回答下列问题:
(1)处于激发态的S原子,其中1个3s电子跃迁到3p轨道上,该激发态S原子的核外电子排布式为__ 。同族元素的氢化物中,H2O比H2Te沸点高的原因是__ 。
(2)检验Fe2+的试剂有多种,其中之一是铁氰化钾(K3[Fe(CN)6]),又称赤血盐。
①在配合物K3[Fe(CN)6]中,易提供孤电子对的成键原子是__ (填元素名称),含有12molσ键的K3[Fe(CN)6]的物质的量为__ mol。
②赤血盐中C原子的杂化方式为__ ;C、N、O三种元素第一电离能由大到小的排序为___ ;写出与CN-互为等电子体的一种化合物的化学式__ 。
③Fe、Na、K的晶胞结构相同,但钠的熔点比钾更高,原因是___ 。
(3)CuFeS2的晶胞结构如图所示。已知:晶胞参数a=0.524nm,c=1.032nm。则CuFeS2的晶胞中每个Cu原子与__ 个S原子相连,晶体密度ρ=__ g·cm-3(列出计算表达式)。
(1)处于激发态的S原子,其中1个3s电子跃迁到3p轨道上,该激发态S原子的核外电子排布式为
(2)检验Fe2+的试剂有多种,其中之一是铁氰化钾(K3[Fe(CN)6]),又称赤血盐。
①在配合物K3[Fe(CN)6]中,易提供孤电子对的成键原子是
②赤血盐中C原子的杂化方式为
③Fe、Na、K的晶胞结构相同,但钠的熔点比钾更高,原因是
(3)CuFeS2的晶胞结构如图所示。已知:晶胞参数a=0.524nm,c=1.032nm。则CuFeS2的晶胞中每个Cu原子与

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】碘及其化合物在生产、生活中有着广泛的应用。回答下列问题:
电负性:H 2.20;C 2.55;F 3.98;P 2.19;I 2.66
(1)人工合成的131I是医疗上常用的放射性同位素,碘在周期表中位于_______ 区。
(2)碘单质在CS2中的溶解度比在水中的大,解释原因_______ 。
(3)HI主要用于药物合成,通常用I2和P反应生成PI3,PI3再水解制备HI。PI3水解生成HI的化学方程式是_______ 。
(4)已知键角PI3 > H2O。从结构角度解释其原因:_______ 。
(5)CH3I是一种甲基化试剂,CF3I可用作制冷剂,CH3I和CF3I发生水解时的主要反应分别是:CH3I + H2O → CH3OH + HI和CF3I + H2O → CF3H + HIO。CF3I的水解产物是HIO,结合电负性解释原因_______ 。
(6)KIO3晶体是一种性能良好的光学材料,其晶胞为立方体,边长为a nm,晶胞中K、I、O分别处于顶点、体心、面心位置,结构如图。

①与K原子紧邻的O原子有_______ 个。
②KIO3的摩尔质量为214 g·mol-1,阿伏加德罗常数为NA.该晶体的密度是_______ g·cm-3(1 nm = 10−9 m)。
电负性:H 2.20;C 2.55;F 3.98;P 2.19;I 2.66
(1)人工合成的131I是医疗上常用的放射性同位素,碘在周期表中位于
(2)碘单质在CS2中的溶解度比在水中的大,解释原因
(3)HI主要用于药物合成,通常用I2和P反应生成PI3,PI3再水解制备HI。PI3水解生成HI的化学方程式是
(4)已知键角PI3 > H2O。从结构角度解释其原因:
(5)CH3I是一种甲基化试剂,CF3I可用作制冷剂,CH3I和CF3I发生水解时的主要反应分别是:CH3I + H2O → CH3OH + HI和CF3I + H2O → CF3H + HIO。CF3I的水解产物是HIO,结合电负性解释原因
(6)KIO3晶体是一种性能良好的光学材料,其晶胞为立方体,边长为a nm,晶胞中K、I、O分别处于顶点、体心、面心位置,结构如图。

①与K原子紧邻的O原子有
②KIO3的摩尔质量为214 g·mol-1,阿伏加德罗常数为NA.该晶体的密度是
您最近一年使用:0次
【推荐3】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______ (填序号,以下同),含有金属离子的物质是__ ,分子间可形成氢键的物质是________ ,属于离子晶体的是__ ,属于原子晶体的是__ ,①~⑤五种物质的熔点由高到低的顺序是__ 。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__ ;B.__ ;C.__ ;D.__ 。
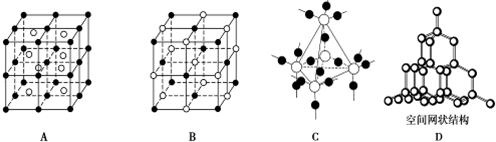
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__ ;B.__ ;C.__ D.____ 。
.
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.
.

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】合成氨是人类科学技术上的一项重大突破,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①基态氮原子的价电子轨道表示式为______ 。
②自然固氮过程中生成的 的VSEPR模型名称为
的VSEPR模型名称为______ 。
(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是______ 。
②基态铬原子的电子排布式为______ 。
③下列比较正确的是______ 。
A.第一电离能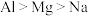 B.熔点:
B.熔点: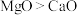
C.离子半径: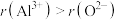 D.键角:
D.键角: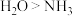
④ⅤA族元素的气态氢化物中NH3沸点最高的原因是______ 。
⑤NH3、H2O和PH3分子的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是______ 、______ 。

(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①基态氮原子的价电子轨道表示式为
②自然固氮过程中生成的
 的VSEPR模型名称为
的VSEPR模型名称为(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②基态铬原子的电子排布式为
③下列比较正确的是
A.第一电离能
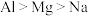 B.熔点:
B.熔点: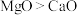
C.离子半径:
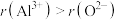 D.键角:
D.键角: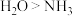
④ⅤA族元素的气态氢化物中NH3沸点最高的原因是
⑤NH3、H2O和PH3分子的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】W、X、Y、Z、N是原子序数依次增大 的五种短周期元素
回答下列问题。
(1)X元素基态原子的电子排布式为______ 。
(2)位于周期表P区的元素有______ (填元素符号,下同)
(3)X、Y两种元素的原子半径:______ >_____ ;电负性______ >_____ 。
(4)由Y、Z、N组成的化合物ZNY溶于水后,滴加酚酞呈红色,振荡后又褪色,结合化学用语解释原因______ 。
元素 | 元素性质或原子结构 |
W | 电子只有一种自旋取向 |
X | 基态原子的最外层有3个未成对电子 |
Y | 原子核外s能级上的电子总数与p能级上的电子总数相等 |
Z | 在同周期元素中,第一电离能最小 |
N | 最高能级有两对成对电子 |
(1)X元素基态原子的电子排布式为
(2)位于周期表P区的元素有
(3)X、Y两种元素的原子半径:
(4)由Y、Z、N组成的化合物ZNY溶于水后,滴加酚酞呈红色,振荡后又褪色,结合化学用语解释原因
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】红蓝宝石、祖母绿、金绿猫眼、钻石为举世公认的珍贵宝石。
(1)红宝石是刚玉的一种,主要成分为氧化铝( ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为___________ 。
(2)祖母绿主要成分的化学式为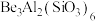 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)___________ I(Al)。Be和Al一样,能与NaOH溶液反应,请简单说明判断依据:___________ 。
(3)金绿猫眼主要成分的化学式为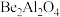 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为___________ 。 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式:
的结构式:___________ 。 分子中铝的杂化类型
分子中铝的杂化类型___________ 。
(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为___________ 。金刚石晶胞结构如图所示,与晶胞面心处碳原子距离最近且等距离的碳原子数为___________ 。
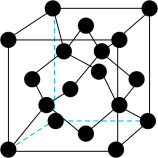
(5)该晶胞空间利用率___________ (用含的π式子表示)。
(1)红宝石是刚玉的一种,主要成分为氧化铝(
 ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为(2)祖母绿主要成分的化学式为
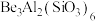 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)(3)金绿猫眼主要成分的化学式为
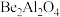 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式:
的结构式: 分子中铝的杂化类型
分子中铝的杂化类型(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为

(5)该晶胞空间利用率
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为_____________ 。
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是_______ (填化学式),呈现如此递变规律的原因是_______________ 。
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为__________ ,另一种的晶胞如图二所示,该晶胞的空间利用率为__________ ,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为________ 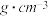 (保留两位有效数字)。(
(保留两位有效数字)。(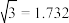 )。
)。
(4)D元素形成的单质,其晶体内含有的微粒间作用力是_________ ,D的醋酸盐晶体局部结构如图三,请用箭头标出图中的配位键。_____

(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为
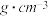 (保留两位有效数字)。(
(保留两位有效数字)。(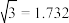 )。
)。(4)D元素形成的单质,其晶体内含有的微粒间作用力是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ氢、碳、氮都是重要的非金属元素,它们的单质及其化合物在科学研究和工业生产中有重要的应用。
(1)下列微粒基态的电子排布中未成对电子数最多的是__ (填序号)
a.N3- b.Fe3+ c.Cu d.Cr e.C
(2)第一电离能介于B、N之间的第二周期元素有_____ 种。
(3)已知HCO3-在水溶液中可通过氢键成为二聚体(八元环结构),试画出该二聚体的结构式:____________________________ 。
(4)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O [Zn(H2O)4]2++4HOCH2CN
[Zn(H2O)4]2++4HOCH2CN
①Zn2+基态核外电子排布式为____ 。1 mol HCHO分子中含有σ键的物质的量为____ mol。
②HOCH2CN分子中碳原子轨道的杂化类型是__ 。与H2O分子互为等电子体的阴离子为__ 。
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为______ 。
Ⅱ.由原子序数由小到大的A、B、C、D、E五种元素构成某配位化合物X,其原子个数比为14∶4∶5∶1∶1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6ns1,回答下列问题。
(1)该配位化合物X的化学式为________ 。
(2)元素B、C、D的第一电离能由小到大排列顺序为________ 。(用元素符号表示)
(3)D元素原子的最外层电子轨道表示式为________ 。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可任意比互溶,解释其主要原因为_______________________ 。
(5)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1∶1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式_____________________________ 。
(1)下列微粒基态的电子排布中未成对电子数最多的是
a.N3- b.Fe3+ c.Cu d.Cr e.C
(2)第一电离能介于B、N之间的第二周期元素有
(3)已知HCO3-在水溶液中可通过氢键成为二聚体(八元环结构),试画出该二聚体的结构式:
(4)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O
 [Zn(H2O)4]2++4HOCH2CN
[Zn(H2O)4]2++4HOCH2CN①Zn2+基态核外电子排布式为
②HOCH2CN分子中碳原子轨道的杂化类型是
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
Ⅱ.由原子序数由小到大的A、B、C、D、E五种元素构成某配位化合物X,其原子个数比为14∶4∶5∶1∶1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6ns1,回答下列问题。
(1)该配位化合物X的化学式为
(2)元素B、C、D的第一电离能由小到大排列顺序为
(3)D元素原子的最外层电子轨道表示式为
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可任意比互溶,解释其主要原因为
(5)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1∶1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铁、钴、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)铁、钴、镍的基态原子核外未成对电子数最多的是_________ 。
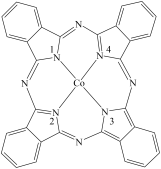
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是_______ (填1、2、3、4),三种非金属原子的电负性由大到小的顺序为_______ (用相应的元素符号表示);氮原子的杂化轨道类型为________ 。

(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x,晶体属于_______ (填晶体类型),若配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=________ 。
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO______ FeO(填“>”“<”或“=”),原因是_________ 。
(5)NiAs的晶胞结构如图所示:①镍离子的配位数为_________ 。
②若阿伏伽德罗常数的值为NA,晶体密度为pg·cm-3,则该晶胞中最近的Ni2+之间的距离为________ cm。(写出计算表达式)
(1)铁、钴、镍的基态原子核外未成对电子数最多的是
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是


(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x,晶体属于
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
(5)NiAs的晶胞结构如图所示:①镍离子的配位数为
②若阿伏伽德罗常数的值为NA,晶体密度为pg·cm-3,则该晶胞中最近的Ni2+之间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。请回答:
(1) 和
和 中心原子的杂化方式分别为
中心原子的杂化方式分别为________ 和_______ 。第一电离能介于B、N之间的第二周期元素有______ 种。
(2)卤化物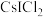 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为____ (写化学式)。解释X的熔点比Y高的原因_____ 。
(3)一种铜的溴化物立方晶胞如图所示。

该化合物的化学式为______ ,在晶体中与Cu距离最近且相等的Cu有___ 个,若该晶体密度为
 ,化合物式量为M,则该晶体中Cu原子与Br原子的最小核间距为
,化合物式量为M,则该晶体中Cu原子与Br原子的最小核间距为______ pm(写出表达式,阿伏加德罗常数为 )。
)。
(1)
 和
和 中心原子的杂化方式分别为
中心原子的杂化方式分别为(2)卤化物
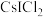 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为(3)一种铜的溴化物立方晶胞如图所示。

该化合物的化学式为

 ,化合物式量为M,则该晶体中Cu原子与Br原子的最小核间距为
,化合物式量为M,则该晶体中Cu原子与Br原子的最小核间距为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】据文献报道:用作锂离子电池正极材料的磷酸亚铁锂(LiFePO4)可采用FeCl3、NH4H2PO4、LiCl和苯胺( )等作为原料制备。回答下列问题:
)等作为原料制备。回答下列问题:
(1)在元素周期表中,Li属于_______ 区元素,与Li的化学性质最相似的邻族元素是_______ ,该元素基态原子核外M层电子的自旋状态_______ (填“相同”或“相反”)。
(2)在NH4H2PO4中,电负性值最高的元素是_______ ;P原子的_______ 杂化轨道与O原子的2p轨道形成_______ 键。
(3)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为_______ 。
(4)苯胺的晶体类型是_______ ,苯胺与甲苯的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,记为原子坐标。已知LiCl·3H2O属正交晶系(长方体形),晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子坐标。据此可推断该晶胞中Cl原子的数目为_______ 。设LiCl·3H2O的摩尔质量为Mg·mol-1,NA为阿伏加德罗常数的值,则LiCl·3H2O晶体的密度为_______ g·cm-3(列出计算表达式,不必化简)。

 )等作为原料制备。回答下列问题:
)等作为原料制备。回答下列问题:(1)在元素周期表中,Li属于
(2)在NH4H2PO4中,电负性值最高的元素是
(3)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(4)苯胺的晶体类型是
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,记为原子坐标。已知LiCl·3H2O属正交晶系(长方体形),晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子坐标。据此可推断该晶胞中Cl原子的数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】半导体在集成电路、消费电子、通信系统、光伏发电、照明、大功率电源转换等领域都有应用。
(1)硅是常见的半导体材料。金刚石和硅相比较,熔点更高的是_______ ,原因是_______ 。硅有晶体硅和无定形硅,可以用_______ (填方法名称)来区分晶体硅和无定形硅。
(2)2022年,科研人员发现立方砷化硼是科学界已知的最好的半导体之一,其结构如图所示。基态 原子的简化电子排布式为
原子的简化电子排布式为_______ ,立方砷化硼中,_______ (填“含有”或“不含有”)配位键。
(4)砷化镓被誉为“半导体贵族”,是雷达、电子计算机、人造卫星、宇宙飞船等高新产品中不可或缺的材料。已知 立方晶胞结构如图所示,其晶胞参数为
立方晶胞结构如图所示,其晶胞参数为 。1号原子和2号原子之间的距离为
。1号原子和2号原子之间的距离为_______  ;晶胞密度为
;晶胞密度为_______  (阿伏加德罗常数的值用
(阿伏加德罗常数的值用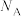 表示)。
表示)。
(1)硅是常见的半导体材料。金刚石和硅相比较,熔点更高的是
(2)2022年,科研人员发现立方砷化硼是科学界已知的最好的半导体之一,其结构如图所示。基态
 原子的简化电子排布式为
原子的简化电子排布式为
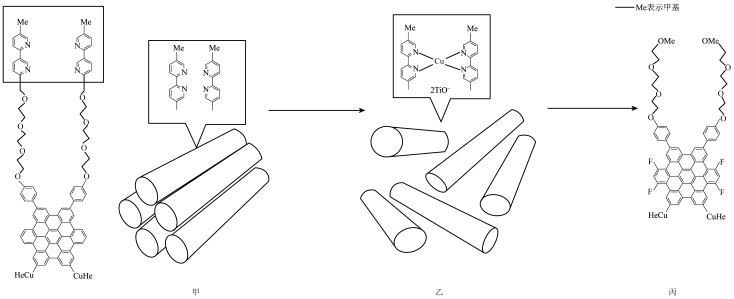
| A.分子识别和自组装是超分子的重要特征 |
B.甲分子中的氮原子的杂化方式均为 |
C.乙分子图示结构部分中,1个 形成了2个配位键 形成了2个配位键 |
| D.丙分子中存在氢键 |
(4)砷化镓被誉为“半导体贵族”,是雷达、电子计算机、人造卫星、宇宙飞船等高新产品中不可或缺的材料。已知
 立方晶胞结构如图所示,其晶胞参数为
立方晶胞结构如图所示,其晶胞参数为 。1号原子和2号原子之间的距离为
。1号原子和2号原子之间的距离为 ;晶胞密度为
;晶胞密度为 (阿伏加德罗常数的值用
(阿伏加德罗常数的值用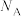 表示)。
表示)。
您最近一年使用:0次



