Ⅰ.在密闭容器中充入1mol H2和1mol I2,一定温度下发生反应:H2(g)+I2(g)  2HI(g)
2HI(g)
(1)保持容器内气体压强不变,向其中充入1 mol N2,反应速率___________ 。(填“变大”“变小”或“不变”,下同);
(2)保持容器体积不变,向其中充入1 mol N2,反应速率___________ 。
Ⅱ.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:
(3)该反应化学平衡常数的表达式:K=___________ ;
(4)该反应为___________ (填“吸热”或“放热”)反应;
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为___________ ℃。
 2HI(g)
2HI(g)(1)保持容器内气体压强不变,向其中充入1 mol N2,反应速率
(2)保持容器体积不变,向其中充入1 mol N2,反应速率
Ⅱ.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)该反应化学平衡常数的表达式:K=
(4)该反应为
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为
更新时间:2023-10-28 09:52:04
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】某温度时,在2 L恒容密闭容器中充入0.9 mol A(g)、0.6 mol B(g)、0.3 mol C(g),发生反应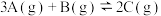 ,各物质物质的量的变化关系如图所示,回答下列问题:
,各物质物质的量的变化关系如图所示,回答下列问题:___________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
(2)0~5 min内,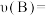
___________ mol∙L−1∙min−1。
(3)反应达到平衡时,
___________ mol∙L−1。
(4)若仅改变下列一个条件,推测该反应的速率发生的变化 (填“增大”、“减小”或“不变”):
①降低温度,化学反应速率___________ ;
②充入少量不参加反应的稀有气体,化学反应速率___________ ;
③将容器的体积压缩至原来的一半,化学反应速率___________ 。
(5) min时,反应
min时,反应___________ (填“达到”或“没有达到”)化学平衡;5 min时,υ(正)___________ (填“>”、“<”或“=”) υ(逆)。
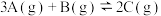 ,各物质物质的量的变化关系如图所示,回答下列问题:
,各物质物质的量的变化关系如图所示,回答下列问题: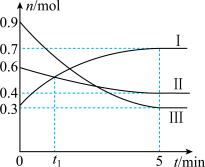
(2)0~5 min内,
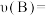
(3)反应达到平衡时,

(4)若仅改变下列一个条件,推测该反应的速率发生的变化 (填“增大”、“减小”或“不变”):
①降低温度,化学反应速率
②充入少量不参加反应的稀有气体,化学反应速率
③将容器的体积压缩至原来的一半,化学反应速率
(5)
 min时,反应
min时,反应
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定条件下CO2会和H2反应合成CH3OH。方程式为:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) 。现向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10s后反应达到平衡,此时容器内CH3OH的浓度为0.5mol·L-1,请回答以下问题:
CH3OH(g)+H2O(g) 。现向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10s后反应达到平衡,此时容器内CH3OH的浓度为0.5mol·L-1,请回答以下问题:
(1)前10s内的平均反应速率v(H2O)=___________ ;平衡时c(H2)=___________ 。
(2)其它条件不变的情况下,在10s时往容器中再加入一定量H2,此时该反应正向速率将___________ (填“增大”或“减小”或“不变”)。
(3)下列叙述能说明原反应达到平衡状态的是___________ 。
a.单位时间内消耗n mol CH3OH的同时生成n mol CO2
b.1mol CO2生成的同时有3mol H-H键断裂
c.CO2和H2的浓度保持不变
d.容器内压强保持不变
e.CO2和H2的物质的量之比保持不变
(4)甲醇(CH3OH)性质类似乙醇,请写出甲醇与乙酸形成乙酸甲酯的反应方程式:___________
 CH3OH(g)+H2O(g) 。现向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10s后反应达到平衡,此时容器内CH3OH的浓度为0.5mol·L-1,请回答以下问题:
CH3OH(g)+H2O(g) 。现向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10s后反应达到平衡,此时容器内CH3OH的浓度为0.5mol·L-1,请回答以下问题:(1)前10s内的平均反应速率v(H2O)=
(2)其它条件不变的情况下,在10s时往容器中再加入一定量H2,此时该反应正向速率将
(3)下列叙述能说明原反应达到平衡状态的是
a.单位时间内消耗n mol CH3OH的同时生成n mol CO2
b.1mol CO2生成的同时有3mol H-H键断裂
c.CO2和H2的浓度保持不变
d.容器内压强保持不变
e.CO2和H2的物质的量之比保持不变
(4)甲醇(CH3OH)性质类似乙醇,请写出甲醇与乙酸形成乙酸甲酯的反应方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】一定条件下,在 密闭容器中发生反应:
密闭容器中发生反应: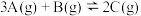 。开始时加入
。开始时加入 、
、 、
、 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 。
。
(1)用 的浓度变化表示反应的平均速率:
的浓度变化表示反应的平均速率:
_______ 。
(2)在 末,
末, 的浓度为
的浓度为_______ 。
(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①升高温度,化学反应速率_______ ;
②充入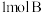 ,化学反应速率
,化学反应速率_______ ;
③将容器的体积变为 ,化学反应速率
,化学反应速率_______ 。
 密闭容器中发生反应:
密闭容器中发生反应: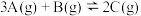 。开始时加入
。开始时加入 、
、 、
、 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 。
。(1)用
 的浓度变化表示反应的平均速率:
的浓度变化表示反应的平均速率:
(2)在
 末,
末, 的浓度为
的浓度为(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①升高温度,化学反应速率
②充入
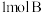 ,化学反应速率
,化学反应速率③将容器的体积变为
 ,化学反应速率
,化学反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】T℃时,向体积为1L的恒容密闭容器中通入1molH2和1molCl2,一定条件下发生反应H2(g)+Cl2(g) 2HCl(g), HCl的物质的量随时间变化如图所示。
2HCl(g), HCl的物质的量随时间变化如图所示。

回答下列问题:
(1) tm时,υ正_______ υ逆(填“>”、“<”或“=”)。
(2) 0~tm内H2的平均反应速率υ(H2)=__________ 。
(3)若要增大HCl的生成速率可以采取的措施有____ 、____ 。(填写两种措施)
(4)下列说法能表明该反应已达到平衡状态的是___ (填序号)。
①生成2 mol HCl的同时消耗1 mol H2
②混合气体中HCl的物质的量分数保持不变
③混合气体中各物质的浓度保持不变
④混合气体中H2、Cl2的浓度之比为1∶1
(5)达到平衡后,升高反应温度,再次达到平衡后,测得HCl的物质的量分数为20%。则升高反应温度,该反应向___ (填“正反应”、 “逆反应”或“不移动”)方向发生移动。
 2HCl(g), HCl的物质的量随时间变化如图所示。
2HCl(g), HCl的物质的量随时间变化如图所示。
回答下列问题:
(1) tm时,υ正
(2) 0~tm内H2的平均反应速率υ(H2)=
(3)若要增大HCl的生成速率可以采取的措施有
(4)下列说法能表明该反应已达到平衡状态的是
①生成2 mol HCl的同时消耗1 mol H2
②混合气体中HCl的物质的量分数保持不变
③混合气体中各物质的浓度保持不变
④混合气体中H2、Cl2的浓度之比为1∶1
(5)达到平衡后,升高反应温度,再次达到平衡后,测得HCl的物质的量分数为20%。则升高反应温度,该反应向
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定温度下,反应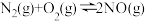 在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
(1)缩小容器体积使压强增大:______ ;
(2)恒容条件下充入N2:______ ;
(3)恒容条件下充入He:______ ;
(4)恒压条件下充入He:______ 。
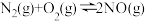 在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。(1)缩小容器体积使压强增大:
(2)恒容条件下充入N2:
(3)恒容条件下充入He:
(4)恒压条件下充入He:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) ⇌2C(g)+2D(g),反应进行到10s末,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
(1)用C表示10s内反应的平均反应速率为__ ;
(2)10s末,生成物D的浓度为__ ;
(3)若改变下列条件,生成D的速率如何变化(用“增大”“减小”或“不变”填空)。
(1)用C表示10s内反应的平均反应速率为
(2)10s末,生成物D的浓度为
(3)若改变下列条件,生成D的速率如何变化(用“增大”“减小”或“不变”填空)。
| 编号 | 改变的条件 | 生成D的速率 |
| ① | 降低温度 | |
| ② | 增大A的浓度 | |
| ③ | 使用正催化剂 | |
| ④ | 恒容下充入Ne (不参与体系反应) |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】研究二氧化碳的转化是实现“双碳”目标的途径之一。可通过电化学、热化学等方法,将 转化为
转化为 等化学品。现有反应过程如下:
等化学品。现有反应过程如下:
①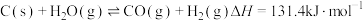
②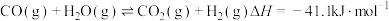
(1)写出 的结构式
的结构式___________ ,写出 的电离方程式
的电离方程式___________ 。
(2)反应①的平衡常数表达式
___________ 。
 转化为
转化为 等化学品。现有反应过程如下:
等化学品。现有反应过程如下:①
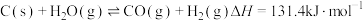
②
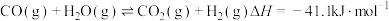
(1)写出
 的结构式
的结构式 的电离方程式
的电离方程式(2)反应①的平衡常数表达式

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】 可用FeO吸收获得
可用FeO吸收获得 .有关反应:
.有关反应:
①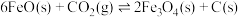
②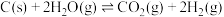
(1)反应①的化学平衡常数表达式为________ 。
(2)若 时反应①达到平衡,此时
时反应①达到平衡,此时 的浓度为
的浓度为 ,保持其他条件不变,再加入一定量的
,保持其他条件不变,再加入一定量的 ,再次达到平衡后
,再次达到平衡后 的浓度为
的浓度为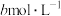 ,则a
,则a________ b(选填“>”、“<”或“=”)。请说明理由________ 。
 可用FeO吸收获得
可用FeO吸收获得 .有关反应:
.有关反应:①
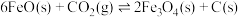
②
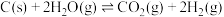
(1)反应①的化学平衡常数表达式为
(2)若
 时反应①达到平衡,此时
时反应①达到平衡,此时 的浓度为
的浓度为 ,保持其他条件不变,再加入一定量的
,保持其他条件不变,再加入一定量的 ,再次达到平衡后
,再次达到平衡后 的浓度为
的浓度为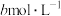 ,则a
,则a
您最近一年使用:0次

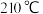 达到平衡:
达到平衡: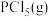

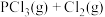



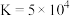


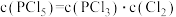
 浓度,反应③的K值
浓度,反应③的K值

