室温下,通过下列实验探究NaHCO3的性质。
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测得0.1 mol/LNaHCO3溶液的pH约为8 |
| 2 | 向10 mL 0.1 mol/LNaHCO3溶液中加入10 mL 0.1 mol/L NaOH溶液,测得溶液pH约11.3 |
| 3 | 向0.1 mol/L NaHCO3溶液中加入过量0.1 mol/LCaCl2溶液,产生白色沉淀 |
| 4 | 向10 mL 0.1 mol/LNaHCO3溶液中加入10 mL 0.1 mol/L盐酸,产生无色气泡 |
A.实验1的溶液中有:c(Na+)>c( )>c( )>c( ) >c(H2CO3) ) >c(H2CO3) |
B.实验2得到的溶液中有 c(OH-)=c(H+)+c( )+2c(H2CO3) )+2c(H2CO3) |
C.实验3中两溶液混合时有:c(Ca2+)c( )<Ksp(CaCO3) )<Ksp(CaCO3) |
D.实验4中反应的离子方程式: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
更新时间:2023-12-06 21:11:14
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列指定反应的离子方程式书写正确的是
A. 溶液与过量NaOH溶液反应: 溶液与过量NaOH溶液反应: |
B. 溶液与 溶液与 溶液反应: 溶液反应: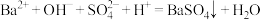 |
C.酸性条件下 溶液与KI溶液发生反应生成 溶液与KI溶液发生反应生成 : : |
D.MgO与稀盐酸反应: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】海水提溴过程中,将溴吹入吸收塔,使蒸气和吸收剂二氧化硫发生作用以达到富集的目的,化学反应为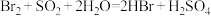 。下列说法不正确的是
。下列说法不正确的是
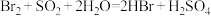 。下列说法不正确的是
。下列说法不正确的是| A.该反应既是氧化还原反应又是化合反应 |
| B.二氧化硫在反应中作还原剂 |
C.该反应的离子方程式为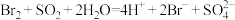 |
| D.溴单质发生了还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列反应的离子方程式中正确的是
| A.过量铁粉加入稀硝酸中:Fe+2H+=Fe2++H2↑ |
B.向AlCl3溶液中滴加过量氨水:Al3++4NH3•H2O=AlO +4NH +4NH +2H2O +2H2O |
C.向水中通入氯气:Cl2+H2O 2H++Cl-+ClO- 2H++Cl-+ClO- |
D.饱和Na2CO3溶液与CaSO4固体反应:CO +CaSO4 +CaSO4 CaCO3+SO CaCO3+SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某研究小组欲用锂离子电池正极废料(含LiCoO2、铁的氧化物)制备CoSO4⋅7H2O晶体。下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol⋅L-1计算)
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Co2+ | 6.9 | 9.4 |
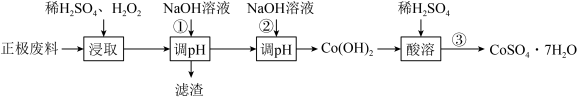
| A.H2O2只做还原剂,浸取温度不宜过高 |
| B.①调节pH约为5,②调节pH至9.4 |
| C.滤渣主要为Fe(OH)3 |
| D.操作③为蒸发浓缩、冷却结晶 |
您最近一年使用:0次
【推荐2】下列实验操作和现象,得出的相应结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用pH计分别测定饱和SO2溶液和饱和CO2溶液的pH | 前者pH较小 | 酸性:H2SO3>H2CO3 |
| B | 向滴有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅并且有白色沉淀生成 | Na2CO3溶液中存在水解平衡 |
| C | 向KCl、KI的混合溶液中滴入AgNO3溶液 | 有黄色沉淀生成 | Ksp(AgI)<Ksp(AgCl) |
| D | 分别测定浓度均为 的CH3COONH4和NaHCO3溶液的pH 的CH3COONH4和NaHCO3溶液的pH | 后者大于前者 | 水解常数:Kh(HCO )>Kh(CH3COO-) )>Kh(CH3COO-) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下,用0.1mol·L-1的NaOH溶液滴定20mL0.1mol·L-1HA溶液,测得混合溶液的pH与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是

 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
| A.导电能力:a>b |
| B.室温下,Ka(HA)=10-3.8 |
| C.b点时,V(NaOH)=20mL |
| D.c点时,c(A-)>c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于电解质溶液的说法中正确的是
| A.用等浓度的硫酸中和等体积、pH相同的氨水和氢氧化钠溶液,消耗的硫酸体积相等 |
B.某温度下纯水中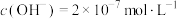 ,则该温度下 ,则该温度下 NaOH的pH=13 NaOH的pH=13 |
C.NaHA溶液呈酸性,说明H2A为弱酸,且 的电离程度大于其水解程度 的电离程度大于其水解程度 |
D. NH4HS溶液中: NH4HS溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】食用磷酸钾(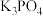 )可用作食品乳化剂,工业制备原理为:
)可用作食品乳化剂,工业制备原理为:
ⅰ. ,控制
,控制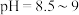 左右;
左右;
ⅱ.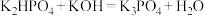 ,控制pH=14左右。
,控制pH=14左右。
已知常温下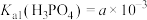 、
、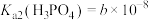 、
、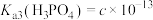 。
。
常温下,下列说法正确的是
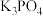 )可用作食品乳化剂,工业制备原理为:
)可用作食品乳化剂,工业制备原理为:ⅰ.
 ,控制
,控制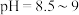 左右;
左右;ⅱ.
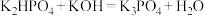 ,控制pH=14左右。
,控制pH=14左右。已知常温下
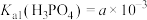 、
、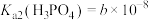 、
、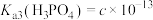 。
。常温下,下列说法正确的是
A. 溶液中由水电离出的氢离子浓度一定大于 溶液中由水电离出的氢离子浓度一定大于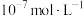 |
B.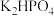 溶液中 溶液中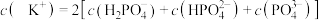 |
C.向 溶液中滴加少量KOH溶液,反应的离子方程式为 溶液中滴加少量KOH溶液,反应的离子方程式为 |
D.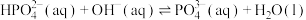 的化学平衡常数为10c 的化学平衡常数为10c |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列叙述正确的是
| A.10 mL 0.1 mol/L NH4Cl溶液与5 mL 0.2 mol/L NaOH溶液混合:c(Cl-)=c(Na+)>c(OH-)>c(H+) |
| B.0.1mol/L pH为4的NaHB的溶液中,c(HB—)> c(H2B)> c(B2—) |
| C.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42- |
| D.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将 醋酸与
醋酸与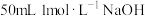 溶液混合,在所得溶液中,下列关系成立的是
溶液混合,在所得溶液中,下列关系成立的是
 醋酸与
醋酸与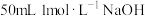 溶液混合,在所得溶液中,下列关系成立的是
溶液混合,在所得溶液中,下列关系成立的是A.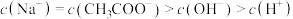 |
B.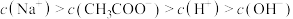 |
C.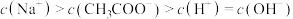 |
D. |
您最近一年使用:0次

 放入水中:
放入水中: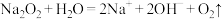
 通入水中:
通入水中:



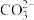 )>c(
)>c( )>c(OH−)
)>c(OH−) )+c(OH−)
)+c(OH−)

