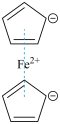
 )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。(1)Fe在周期表中的
(2)羰基铁粉【Fe(CO)5】中铁元素的配位数是
(3)二茂铁的衍生物可和H3O+等微粒产生静电作用,H、O和C的电负性由大到小的顺序为
(4)T-碳是碳的一种同素异形体,其晶体结构可以看成是金刚石晶体(如图甲)中每 个碳原子被一个由四个碳原子组成的正四面体结构单元(
 )所取代(如图乙)。
)所取代(如图乙)。
一个T-碳晶胞中含有
相似题推荐
(1)Fe的基态原子的核外电子排布式为
(2)在C、N、O、P、S五种元素中,第一电离能最大的元素是
(3)氨基乙酸(H2NCH2COOH)是蛋白质完全水解的产物之一,其中C原子的杂化轨道类型为
(4)蛋白质在体内部分被氧化生成尿素[CO(NH2)2]、二氧化碳、水等排出体外。
①H2O分子的空间构型为
②尿素易溶于水,其原因除都是极性分子外,还有
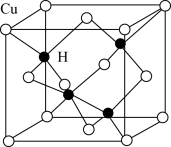
(5)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为
(1)对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为

B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(3)
 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应键角如图所示。
的空间结构和相应键角如图所示。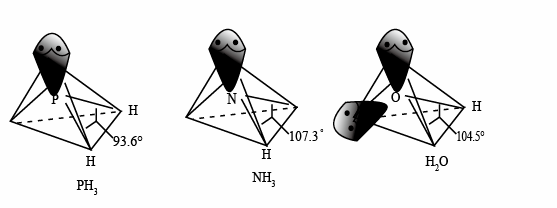
 中P的杂化类型是
中P的杂化类型是 的沸点比
的沸点比 的
的 的键角小于
的键角小于 的键角,分析原因
的键角,分析原因(4)
 和NaClO均可作化工生产的氧化剂或氯化剂.制备
和NaClO均可作化工生产的氧化剂或氯化剂.制备 的反应为
的反应为 。
。①上述描述中涉及的非金属元素电负性由大到小的顺序是
②常温时
 是一种易溶于
是一种易溶于 的液体,则
的液体,则 分子属于
分子属于③配合物
 中心离子
中心离子 的配位数为6,向含
的配位数为6,向含 的溶液中滴加
的溶液中滴加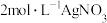 溶液,反应完全后共消耗
溶液,反应完全后共消耗 溶液50mL,则配合物的化学式应该写为
溶液50mL,则配合物的化学式应该写为(1)铁元素基态原子的电子排布式为
(2)Fe3+可用KSCN溶液检验,形成的配合物颜色为
(3)氮元素的最简单氢化物为氨,氨的沸点
(4)铁的第三电离能(I3),第四电离能(I4)分别为2957kJ/mol,5290kJ/mol,I4远大于I3的原因是
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
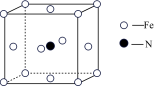
(1)基态Ni原子的价电子电子排布式为
(2)已知镍与铜的第二电离能分别为INi= 1753 kJ·mol-1,ICu= 1958 kJ·mol-1,ICu>INi的原因是
(3)Ni2+常与丁二酮肟(
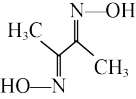 )形成图A所示的配合物,图B是硫代氧的结果:
)形成图A所示的配合物,图B是硫代氧的结果: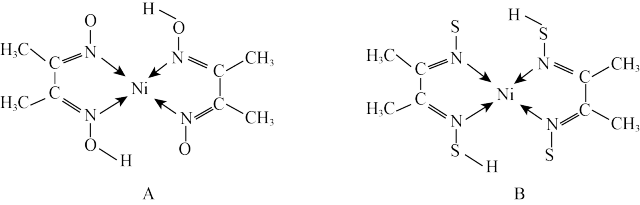
①熔点大小: A
②Ni2+与丁二酮肟之间形成的化学键称为
③B中碳原子的杂化轨道类型是
(4)硫酸镍[NiSO4J]常用于有机化学合成中,阴离子的空间构型为
(5)NiO,FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
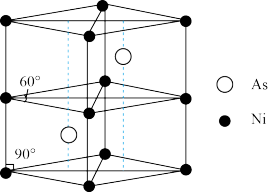
(6)某砷镍合金的密度为ρg·cm-3,其晶胞结构如图所示。As和Ni的原子半径分别为rAs pm和rNi pm,阿伏加德罗常数的值为NA,则该晶胞中原子的体积占晶胞体积的百分率为
(1)基态Cu原子的价电子有
(2)碳和氢形成的最简单碳正离子
 ,该阳离子的空间构型为
,该阳离子的空间构型为(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是
(4)金属晶体铜的晶胞如图所示。铜原子间的最短距离为a pm,密度为pg/cm3,NA为阿伏加德罗常数。铜的相对原子质量为

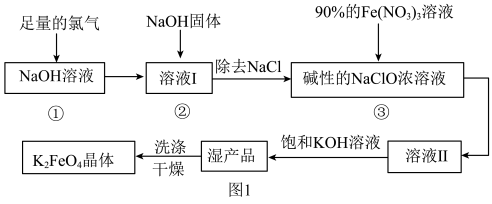
回答下列问题:
(1)Fe(NO3)3中
 的空间结构名称为
的空间结构名称为(2)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,取某温度下反应液,测得ClO-与
 的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为
的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为(3)反应③的离子方程式为
(4)往溶液II中加入饱和KOH溶液得到湿产品的原因是
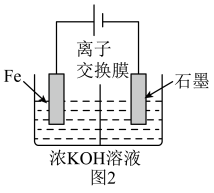
(5)高铁酸钾还可以通过电解法制备,其原理如图2所示:阳极的电极反应式为
【推荐1】第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)镓的基态原子电子排布式是
(2)多酚氧化酶与植物的抗病性有关。配合物
 是多酚氧化酶的模型配合物(如图所示)。
是多酚氧化酶的模型配合物(如图所示)。
①EDTA中N的杂化轨道类型为
②一个邻苯二胺分子中σ键的数目为
③EDTB分子中所含元素的电负性由小到大的顺序为
④配离子 中的配位原子是
中的配位原子是
(3)向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解得到深蓝色透明溶液,蓝色沉淀溶解的原因是
(4)铁和氮组成一种过渡金属氮化物,其结构如图所示。直六棱柱的底边边长为xpm,高为ypm,阿伏加德罗常数的值为NA,则晶体的密度表达式为

【推荐2】《旧唐书·舆服志》中关于白铜的记载:“自馀一品乘白铜饰犊车”,古时云南所产的镍白铜(铜镍合金)最为有名,称为“云白铜”,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)基态Cu原子的核外电子排布式为[Ar]
(2)向CuSO4溶液中逐滴加入氨水,首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色透明溶液。
①在[Cu(NH3)4]2+中 Cu2+和NH3之间形成的化学键为
②[Cu(NH3)4]SO4中含有的四种非金属元素中电负性最大的是 、SO2、SO3三种微粒中,中心原子价层电子对数不同于其他微粒的是
、SO2、SO3三种微粒中,中心原子价层电子对数不同于其他微粒的是
③在[Cu(NH3)4]SO4中,NH3的中心原子的杂化轨道类型为
(3)某镍白铜合金的立方晶胞结构如图所示。

①在镍白铜合金中金属原子的堆积方式为
②若合金晶胞密度为 d g·cm-3,阿伏加德罗常数为NA,则晶胞边长为
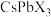 (
( 、
、 和I)和二维钙钛矿
和I)和二维钙钛矿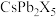 以来,因其优异的光电子学性能和优越的物理化学稳定性,受到材料、能源和光学等领域学者的广泛关注。请回答下列问题:
以来,因其优异的光电子学性能和优越的物理化学稳定性,受到材料、能源和光学等领域学者的广泛关注。请回答下列问题:(1)基态氯原子核外电子有
 原子的价电子排布式为
原子的价电子排布式为(2)人们最早研究的钙钛矿太阳能电池材料是用“光敏材料”和“卤素材料”合成出来的,如
 和
和 。
。①
 结合
结合 得到
得到 ,
, 结合
结合 形成的化学键是
形成的化学键是A.配位键 B.
 键 C.氢键 D.
键 C.氢键 D. 键
键②已知:
 为推电子基团,
为推电子基团, 原子电子云密度越大,碱性越强,则
原子电子云密度越大,碱性越强,则 、
、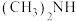 中碱性较强的物质是
中碱性较强的物质是(3)钙钛矿的一种晶胞结构如图1所示,晶胞中钛原子处于氧原子围成的
 处于顶点位置,则该晶胞中氧原子的位置是
处于顶点位置,则该晶胞中氧原子的位置是(4)一种
 的晶胞结构如图2所示,已知原子1、原子2的分数坐标分别是
的晶胞结构如图2所示,已知原子1、原子2的分数坐标分别是 和
和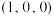 ,原子3的分数坐标是
,原子3的分数坐标是 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。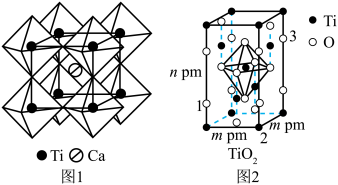

(1)F原子的核外电子排布式为
(2)C的氧化物的熔点远高于E的氧化物的熔点,原因是
(3)比较B、E的氢化物的沸点
(4)A的最高价含氧酸根离子中,其中心原子是
(5)A、D形成某种化合物的晶胞结构如图1,则其化学式为
(6)F单质的晶体的晶胞结构如图2。若F原子的半径是r cm,则F单质的密度的计算公式是

(1)基态P原子中,电子占据的最高能级符号为
(2)磷酸氯喹中N-H键是
(3)PO
 的空间构型是
的空间构型是 互为等电子体的分子是
互为等电子体的分子是(4)磷化镓是人工合成的III-V族化合物半导体材料。其晶胞结构可看作金刚石晶胞内部的碳原子被Ga原子代替,顶点和面心的碳原子被P原子代替。
①磷化镓晶体中含有的化学键类型为
A.离子键 B.配位键 C.σ键 D.π键 E.极性键F.非极性键
②设磷化镓的晶体密度为ag·cm-3,阿伏加德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为
(1)钛元素位于元素周期表的
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)TiCl4可以与胺形成配合物,如[TiCl4(CH3NH2)2]、[TiCl4(H2NCH2CH2NH2)]等。
①[TiCl4(H2NCH2CH2NH2)]中Ti的配位数是
②1 mol H2NCH2CH2NH2中含有的σ键物质的量为
③配合物[TiCl4(H2NCH2CH2NH2)]与游离的H2NCH2CH2NH2分子相比,其H-N-H键角
(4)TiO2的一种晶胞具有典型的四方晶系结构(如图所示),以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。晶胞中A、B的原子坐标为(0.31,0.31,0),(0.81,0.19,0.5)。已知晶胞含对称中心,则C、D原子坐标为




