高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示:
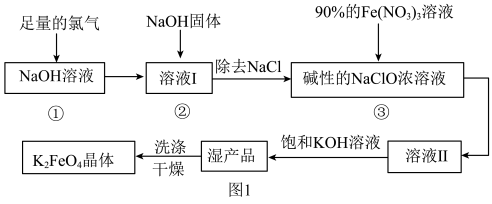
回答下列问题:
(1)Fe(NO3)3中 的空间结构名称为
的空间结构名称为_______ 氮原子的杂化轨道类型为_______
(2)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,取某温度下反应液,测得ClO-与 的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为
的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为_______ 。
(3)反应③的离子方程式为_______ ,制备时,两溶液混合的操作为_______ 。
(4)往溶液II中加入饱和KOH溶液得到湿产品的原因是_______ 。该工艺流程中可循环使用的物质是_______ (填化学式)。
(5)高铁酸钾还可以通过电解法制备,其原理如图2所示:阳极的电极反应式为_______ 。
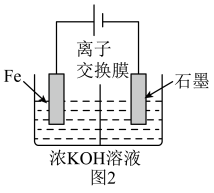

回答下列问题:
(1)Fe(NO3)3中
 的空间结构名称为
的空间结构名称为(2)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,取某温度下反应液,测得ClO-与
 的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为
的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被氧化的氯原子与被还原的氯原子的物质的量之比为(3)反应③的离子方程式为
(4)往溶液II中加入饱和KOH溶液得到湿产品的原因是
(5)高铁酸钾还可以通过电解法制备,其原理如图2所示:阳极的电极反应式为

22-23高三上·辽宁盘锦·期末 查看更多[3]
辽宁省辽河油田第二高级中学2022-2023学年高三上学期期末考试化学试题(已下线)北京市海淀区2022届高三一模(工业流程题)湖南省常德市汉寿县第一中学2023-2024学年高三上学期10月月考化学试题
更新时间:2023-01-18 20:39:43
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】黄铁矿的主要成分是 ,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:
,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:

(1)研究表明,随着磨矿细度的增加,铜、钴的浸出率都会相应增加,其主要原因是:___________
(2)黄铁矿的氧化焙烧是制硫酸工艺的重要一步,其产物之一是 ,反应的化学方程式为:
,反应的化学方程式为:___________ ;制硫酸工艺中涉及反应2SO2+O2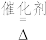 2SO3 ΔH<0,该反应需将温度控制在
2SO3 ΔH<0,该反应需将温度控制在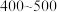 ℃,原因是
℃,原因是___________ 。
(3)氧化还原焙烧渣仍有少量CuS,已知CuS不溶于 ,但当浸出过程含有硫酸铁时,也可氧化浸出,其反应的离子方程式为:
,但当浸出过程含有硫酸铁时,也可氧化浸出,其反应的离子方程式为:___________ 。
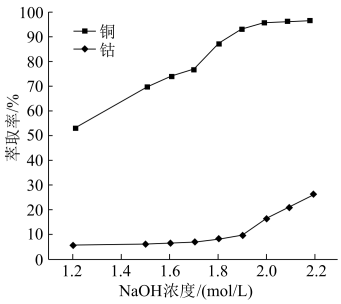
(4)浸液通过加入萃取剂可实现铜和钴的分离,在萃取前加入NaOH溶液乳化可提高分离效率,不同浓度的溶液对萃取率的影响如图,则NaOH溶液最佳的浓度为___________ 。
用硫酸浸取后的浸渣能用磁选法分离,则该氧化物为___________ (填化学式)
已知黄铁矿氧化焙烧前后主要元素质量分数如图:
为测定铜的浸出率,取50g焙烧后的烧渣,经处理后测得 物质的量为
物质的量为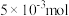 ,则铜离子的浸出率为
,则铜离子的浸出率为___________ (结果保留三位有效数字)。
 ,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:
,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:
(1)研究表明,随着磨矿细度的增加,铜、钴的浸出率都会相应增加,其主要原因是:
(2)黄铁矿的氧化焙烧是制硫酸工艺的重要一步,其产物之一是
 ,反应的化学方程式为:
,反应的化学方程式为: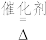 2SO3 ΔH<0,该反应需将温度控制在
2SO3 ΔH<0,该反应需将温度控制在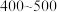 ℃,原因是
℃,原因是(3)氧化还原焙烧渣仍有少量CuS,已知CuS不溶于
 ,但当浸出过程含有硫酸铁时,也可氧化浸出,其反应的离子方程式为:
,但当浸出过程含有硫酸铁时,也可氧化浸出,其反应的离子方程式为:(4)浸液通过加入萃取剂可实现铜和钴的分离,在萃取前加入NaOH溶液乳化可提高分离效率,不同浓度的溶液对萃取率的影响如图,则NaOH溶液最佳的浓度为

用硫酸浸取后的浸渣能用磁选法分离,则该氧化物为
已知黄铁矿氧化焙烧前后主要元素质量分数如图:
| 项目 | Fe | S | Cu | Co |
| 焙烧前(%) | 40.28 | 42.55 | 0.53 | 0.022 |
| 焙烧后(%) | 53.08 | 0.96 | 0.76 | 0.047 |
 物质的量为
物质的量为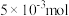 ,则铜离子的浸出率为
,则铜离子的浸出率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】现有下列短周期元素性质的有关数据:
(1)根据元素周期律确定a至h8种元素在周期表中的位置,将它们的元素编号填入如表相应的空格内_______ 。
(2)上述元素形成的氢化物中,分子间存在氢键的有_______ (填氢化物的化学式)。
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。
①氢化铝锂易水解(与水反应),最初得三种产物,请写出其水解反应化学方程式:_______ 。
②与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式:_______ ,写出该物质受热分解的反应方程式:_______ 。
| 元素编号 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低 | +1 | -1 | -3 | +3 | -2 | +3 | +1 | +1 |
| Ⅰ族 | Ⅱ族 | Ⅲ族 | Ⅳ族 | Ⅴ族 | Ⅵ族 | Ⅶ族 | Ⅷ族 | |
| 第一周期 | _____ | |||||||
| 第二周期 | _____ | _____ | _____ | _____ | ||||
| 第三周期 | _____ | _____ | _____ |
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。
①氢化铝锂易水解(与水反应),最初得三种产物,请写出其水解反应化学方程式:
②与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】高锰酸钾是锰的重要化合物和常用的氧化剂。下列是工业上用软锰矿(主要成分为 )制备高锰酸钾的流程图。请回答下列问题:
)制备高锰酸钾的流程图。请回答下列问题:
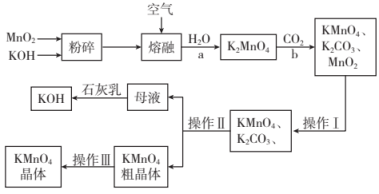
(1)软锰矿和 的混合物在空气中加热熔融反应生成
的混合物在空气中加热熔融反应生成 的化学方程式为
的化学方程式为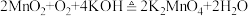 。
。
① 中
中 元素的化合价为
元素的化合价为_______ 价,由流程中的信息分析, 具有
具有_______ 性。
②该反应中氧化剂和还原剂的物质的量之比为_______ 。
(2)操作Ⅰ的名称为_______ 。
(3)母液中加入石灰乳后发生反应的离子方程式为_______ 。该反应所属的反应类型为_______ 。
(4)将 加入浓盐酸中可以制备氯气,写出该反应的化学方程式:
加入浓盐酸中可以制备氯气,写出该反应的化学方程式:_______ 。该反应中作还原剂的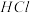 占总反应的
占总反应的_______ 。当消耗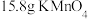 时,产生标准状况下
时,产生标准状况下_______ 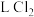 。
。
 )制备高锰酸钾的流程图。请回答下列问题:
)制备高锰酸钾的流程图。请回答下列问题:
(1)软锰矿和
 的混合物在空气中加热熔融反应生成
的混合物在空气中加热熔融反应生成 的化学方程式为
的化学方程式为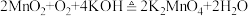 。
。①
 中
中 元素的化合价为
元素的化合价为 具有
具有②该反应中氧化剂和还原剂的物质的量之比为
(2)操作Ⅰ的名称为
(3)母液中加入石灰乳后发生反应的离子方程式为
(4)将
 加入浓盐酸中可以制备氯气,写出该反应的化学方程式:
加入浓盐酸中可以制备氯气,写出该反应的化学方程式: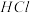 占总反应的
占总反应的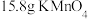 时,产生标准状况下
时,产生标准状况下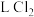 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】I.已知K、L、M、P、Q、R是原子序数依次增大的短周期主族元素。K和Q同主族,L是可以形成化合物种类最多的元素,M与K形成的化合物常作制冷剂,P元素原子的最外层电子数是电子层数的3倍,R是地壳中含量最丰富的金属元素。回答下列问题:
(1)L元素在元素周期表中的位置是___________ 。
(2)Q元素的最高价氧化物对应的水化物与R单质反应的离子方程式为___________ ;向反应后的溶液中持续滴加稀盐酸,能看到的现象是___________ 。
(3)K与P形成的原子个数比为1∶1的物质的电子式为___________ 。
II.氮及其化合物在生产、生活与环境中有着重要的研究和应用价值。
(4) 是制碱工业中不可缺少的物质,写出实验室制备
是制碱工业中不可缺少的物质,写出实验室制备 的化学反应方程式
的化学反应方程式___________ ;验证 已经集满的方法是
已经集满的方法是___________ 。
(5) 是一种强氧化剂,常与肼
是一种强氧化剂,常与肼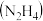 组成双组元液体推进剂,用于火箭发射,二者反应生成无毒无污染的物质,则该反应的化学方程式为
组成双组元液体推进剂,用于火箭发射,二者反应生成无毒无污染的物质,则该反应的化学方程式为___________ 。
(6)一种电解处理含氮废水的方法如图所示,写出阴极的电极反应式___________ 。

(1)L元素在元素周期表中的位置是
(2)Q元素的最高价氧化物对应的水化物与R单质反应的离子方程式为
(3)K与P形成的原子个数比为1∶1的物质的电子式为
II.氮及其化合物在生产、生活与环境中有着重要的研究和应用价值。
(4)
 是制碱工业中不可缺少的物质,写出实验室制备
是制碱工业中不可缺少的物质,写出实验室制备 的化学反应方程式
的化学反应方程式 已经集满的方法是
已经集满的方法是(5)
 是一种强氧化剂,常与肼
是一种强氧化剂,常与肼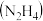 组成双组元液体推进剂,用于火箭发射,二者反应生成无毒无污染的物质,则该反应的化学方程式为
组成双组元液体推进剂,用于火箭发射,二者反应生成无毒无污染的物质,则该反应的化学方程式为(6)一种电解处理含氮废水的方法如图所示,写出阴极的电极反应式

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】一种利用电化学方法同时脱除NO/SO2的工艺如图所示:
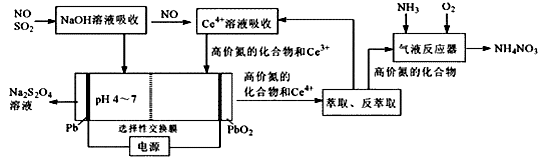
已知SO2水溶液中含硫微粒分布分数(Xi)与pH关系如图所示
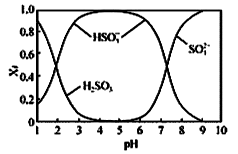
(1)NaOH溶液吸收SO2时,溶液的pH由9→6时,主要发生反应的离子方程式为________ 。
(2)含Ce4+的溶液吸收NO,若高价氮中的NO2、N2O3、NO2-、NO3-各1mol,则消耗0.5mol·L-1的含Ce4+溶液的体积为________ L;其中NO转化NO3-的离子方程式为________ 。
(3)电解槽中,阴极电极反应式主要为________ ,阳极电极反应式为________ 。
(4)在“气液反应器”中高价氮中的N2O3化合为NH4NO3的化学方程式为________ 。

已知SO2水溶液中含硫微粒分布分数(Xi)与pH关系如图所示

(1)NaOH溶液吸收SO2时,溶液的pH由9→6时,主要发生反应的离子方程式为
(2)含Ce4+的溶液吸收NO,若高价氮中的NO2、N2O3、NO2-、NO3-各1mol,则消耗0.5mol·L-1的含Ce4+溶液的体积为
(3)电解槽中,阴极电极反应式主要为
(4)在“气液反应器”中高价氮中的N2O3化合为NH4NO3的化学方程式为
您最近一年使用:0次
【推荐3】氢能是极具发展潜力的清洁能源,2021年我国制氢量位居世界第一、请回答:
(1)氢化铝钠(NaAlH4)是一种重要的储氢材料,已知:
NaAlH4(s)= Na3AlH6(s)+
Na3AlH6(s)+ Al(s)+H2(g),△H=+37kJ•mol-1
Al(s)+H2(g),△H=+37kJ•mol-1
Na3AlH6(s)=3NaH(s)+Al(s)+ H2(g),△H=+70.5kJ•mol-1
H2(g),△H=+70.5kJ•mol-1
则NaAlH4(s)=NaH(s)+Al(s)+ H2(g),△H=
H2(g),△H=___________ 。
(2)工业上,常用 与
与 重整制备
重整制备 。500℃时,主要发生下列反应:
。500℃时,主要发生下列反应:
Ⅰ.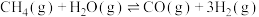 Ⅱ.
Ⅱ.
①已知: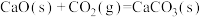
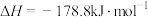 。向重整反应体系中加入适量多孔CaO,其优点是
。向重整反应体系中加入适量多孔CaO,其优点是___________ 。
②下列操作中,能提高CH4(g)平衡转化率的是___________ (填标号)。
A.加催化剂 B.增加CH4(g)用量 C.移除H2(g) D.恒温恒压,通入惰性气体
③500℃、恒压(Po)条件下,1 mol CH4(g)和1 mol H2O(g)反应达平衡时,CH4(g)的转化率为0.5,CO2(g)的物质的量为0.25 mol,则反应Ⅱ的平衡常数KP=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)实现碳达峰、碳中和是贯彻新发展理念的内在要求,因此二氧化碳的合理利用成为研究热点。可用氢气和二氧化碳在催化剂作用下合成甲醇: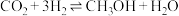 。
。
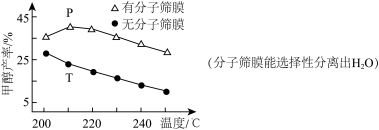
恒压下,CO2和H2的起始物质的量之比为1∶3时,该反应甲醇的平衡产率随温度的变化如图所示。该反应的
___________ 0,甲醇的产率P点高于T点的原因为___________ 。
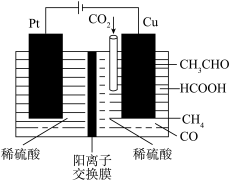
(4)利用电催化可将CO2同时转化为多种燃料,装置如图:铜电极上产生CH4的电极反应式为___________ 。
(1)氢化铝钠(NaAlH4)是一种重要的储氢材料,已知:
NaAlH4(s)=
 Na3AlH6(s)+
Na3AlH6(s)+ Al(s)+H2(g),△H=+37kJ•mol-1
Al(s)+H2(g),△H=+37kJ•mol-1Na3AlH6(s)=3NaH(s)+Al(s)+
 H2(g),△H=+70.5kJ•mol-1
H2(g),△H=+70.5kJ•mol-1则NaAlH4(s)=NaH(s)+Al(s)+
 H2(g),△H=
H2(g),△H=(2)工业上,常用
 与
与 重整制备
重整制备 。500℃时,主要发生下列反应:
。500℃时,主要发生下列反应:Ⅰ.
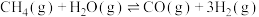 Ⅱ.
Ⅱ.
①已知:
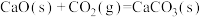
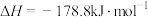 。向重整反应体系中加入适量多孔CaO,其优点是
。向重整反应体系中加入适量多孔CaO,其优点是②下列操作中,能提高CH4(g)平衡转化率的是
A.加催化剂 B.增加CH4(g)用量 C.移除H2(g) D.恒温恒压,通入惰性气体
③500℃、恒压(Po)条件下,1 mol CH4(g)和1 mol H2O(g)反应达平衡时,CH4(g)的转化率为0.5,CO2(g)的物质的量为0.25 mol,则反应Ⅱ的平衡常数KP=
(3)实现碳达峰、碳中和是贯彻新发展理念的内在要求,因此二氧化碳的合理利用成为研究热点。可用氢气和二氧化碳在催化剂作用下合成甲醇:
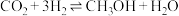 。
。恒压下,CO2和H2的起始物质的量之比为1∶3时,该反应甲醇的平衡产率随温度的变化如图所示。该反应的


(4)利用电催化可将CO2同时转化为多种燃料,装置如图:铜电极上产生CH4的电极反应式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,它们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为_______ ,W3分子的空间构型为_______ ;
(2)X单质与水发生主要反应的化学方程式为_______ ;
(3)化合物M的化学式为_______ ,其晶体结构与NaCl相同。将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有_______ ,O—C—O的键角约为_______ ;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X∶Y∶Z=_______ ;
(5)含有元素Z的盐的焰色反应为___ 色。许多金属盐都可以发生焰色反应,其原因是____ 。
(1)W元素原子的L层电子排布式为
(2)X单质与水发生主要反应的化学方程式为
(3)化合物M的化学式为
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X∶Y∶Z=
(5)含有元素Z的盐的焰色反应为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁被誉为“第一金属”,铁及其化合物在生活中被广泛应用。
(1)基态 的简化电子排布式为
的简化电子排布式为_______ 。
(2)实验室可用KSCN、苯酚( )来检验
)来检验 。N、O、S三种元素的第一电离能由大到小的顺序为
。N、O、S三种元素的第一电离能由大到小的顺序为_______ (用元素符号表示),苯酚中碳原子的杂化轨道类型为_______ 。
(3)FeCl3的熔点为306℃,沸点为315℃。 的晶体类型是
的晶体类型是_______ 。 常作补铁剂,
常作补铁剂, 的立体构型是
的立体构型是_______ 。
(4)羰基铁[ ]可用作催化剂、汽油抗爆剂等。1mol
]可用作催化剂、汽油抗爆剂等。1mol  分子中含
分子中含_______ mol 键。
键。
(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为 ,
, 代表阿伏加德罗常数的值。在该晶胞中,与
代表阿伏加德罗常数的值。在该晶胞中,与 紧邻且等距离的
紧邻且等距离的 数目为
数目为_______ ; 与
与 最短核间距为
最短核间距为_______ pm(列出表达式即可)。

(1)基态
 的简化电子排布式为
的简化电子排布式为(2)实验室可用KSCN、苯酚(
 )来检验
)来检验 。N、O、S三种元素的第一电离能由大到小的顺序为
。N、O、S三种元素的第一电离能由大到小的顺序为(3)FeCl3的熔点为306℃,沸点为315℃。
 的晶体类型是
的晶体类型是 常作补铁剂,
常作补铁剂, 的立体构型是
的立体构型是(4)羰基铁[
 ]可用作催化剂、汽油抗爆剂等。1mol
]可用作催化剂、汽油抗爆剂等。1mol  分子中含
分子中含 键。
键。(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为
 ,
, 代表阿伏加德罗常数的值。在该晶胞中,与
代表阿伏加德罗常数的值。在该晶胞中,与 紧邻且等距离的
紧邻且等距离的 数目为
数目为 与
与 最短核间距为
最短核间距为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题:
(1)根据价层电子对互斥模型,H2S 、SO2 、SO3 的气态分子中,中心原子价层电子对数不同于其他分子的是___________ 。
(2)晶体中H2O 和 中心原子的杂化轨道类型分别为
中心原子的杂化轨道类型分别为___________ ,试判断 H2O 和  的键角大小关系并说明原因:
的键角大小关系并说明原因:___________ 。
(3)成语“信口雌黄 ”中的雌黄分子式为 As2S3,分子结构如图,As 原子的杂化方式为___________ , 雌黄和 SnCl2 在盐酸中反应转化为雄黄(As4S4)和 SnCl4 并放出 H2S 气体。___________ 。
(5)Zn2+的核外电子排布式为___________ ,在元素周期表中,该元素在___________ (填“s”“p”“d”“f”或“ds”)区。。
(6)S8与热的浓NaOH 溶液反应的产物之一为Na2S3,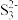 的空间结构为
的空间结构为___________ 。
(7)[H2F]+[SbF6]-(氟酸锑)是一种超强酸,则[H2F]+ 的空间结构为___________ 。
(8)Na3AsO4 中含有的化学键类型包括___________ ; 的空间结构为
的空间结构为 ___________ 。
(1)根据价层电子对互斥模型,H2S 、SO2 、SO3 的气态分子中,中心原子价层电子对数不同于其他分子的是
(2)晶体中H2O 和
 中心原子的杂化轨道类型分别为
中心原子的杂化轨道类型分别为 的键角大小关系并说明原因:
的键角大小关系并说明原因:(3)成语“信口雌黄 ”中的雌黄分子式为 As2S3,分子结构如图,As 原子的杂化方式为

(5)Zn2+的核外电子排布式为
(6)S8与热的浓NaOH 溶液反应的产物之一为Na2S3,
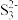 的空间结构为
的空间结构为(7)[H2F]+[SbF6]-(氟酸锑)是一种超强酸,则[H2F]+ 的空间结构为
(8)Na3AsO4 中含有的化学键类型包括
 的空间结构为
的空间结构为
您最近一年使用:0次
【推荐1】聚合氯化铝化学式为[Al2(OH)aCl6-a]n,是一种无机高分子铝的聚合物,已广泛用于生活废水处理。由偏铝酸钙[Ca(AlO2)2]制备聚合氯化铝的一种工艺流程如下:
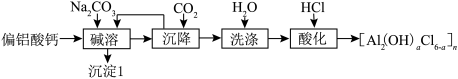
(1)经测定“碱溶”后溶液的pH=12,要使“沉淀Ⅰ”中不含有Ca(OH)2,则溶液中的c( )>
)>_________ mol·L-1。{Ksp[Ca(OH)2]=6×10-6,Ksp(CaCO3)=3×10-9}
(2)“沉降”的温度控制在40℃左右,主要原因是_________ ,“沉降”时的离子方程式为_________ 。
(3)“酸化”时的装置如图所示,先将氢氧化铝滤饼分散在水中,然后向其中滴加定量的盐酸,相比与直接向滤饼加盐酸的优点是_________ ,若要使聚合氯化铝[Al2(OH)aCl6-a]n中a=2,则实验过程中需要控制条件除温度外,还要控制条件是_________ 。
(4)已知溶液pH不同时,钒元素与铝元素存在形式如下表所示,请完成利用(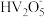 、
、 )碱性废水制备聚合氯化铝的实验步骤:
)碱性废水制备聚合氯化铝的实验步骤:
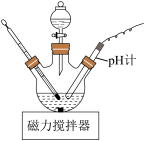
取适量废水_________ ,将纯净的氢氧化铝滤饼分散到水中,向其中滴加盐酸,得到聚合氯化铝。(实验中须使用的试剂有:0.1 mol·L-1HCl、5%的双氧水、蒸馏水)

(1)经测定“碱溶”后溶液的pH=12,要使“沉淀Ⅰ”中不含有Ca(OH)2,则溶液中的c(
 )>
)>(2)“沉降”的温度控制在40℃左右,主要原因是
(3)“酸化”时的装置如图所示,先将氢氧化铝滤饼分散在水中,然后向其中滴加定量的盐酸,相比与直接向滤饼加盐酸的优点是
(4)已知溶液pH不同时,钒元素与铝元素存在形式如下表所示,请完成利用(
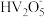 、
、 )碱性废水制备聚合氯化铝的实验步骤:
)碱性废水制备聚合氯化铝的实验步骤:
| 钒的化合价 | pH=5 | pH=13 |
| +4价V | VO(OH)2沉淀 | HV2O5- |
| +5价V | 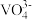 | 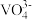 |
| +3价Al | Al(OH)3沉淀 |  |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】钛矿工业中的硫酸酸性废水富含Ti、Fe等元素,其综合利用如下:
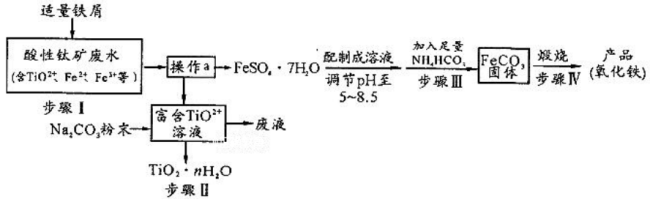
已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为________________________ 。
(2)步骤Ⅰ中检验钛矿废水中加入铁屑是否足量的试剂是________________________ 。
(3)操作a是蒸发浓缩、冷却结晶、______________________________________________ 。
(4)步骤Ⅲ中发生反应的化学方程式为________________________ ;反应温度一般需控制在35℃以下,其目的是____________________________________ 。
(5)已知Ksp=[Fe(OH)2] = 8×10-16。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5, c(Fe2+) = 1×10-6mol/L。试判断所得的FeCO3中________ (填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是_________________ 。
(6)向“富含TiO2+溶液”中加入Na2CO3粉末易得到固体TiO2• nH2O。请结合原理和化学用语解释其原因_________________________________ 。

已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为
(2)步骤Ⅰ中检验钛矿废水中加入铁屑是否足量的试剂是
(3)操作a是蒸发浓缩、冷却结晶、
(4)步骤Ⅲ中发生反应的化学方程式为
(5)已知Ksp=[Fe(OH)2] = 8×10-16。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5, c(Fe2+) = 1×10-6mol/L。试判断所得的FeCO3中
(6)向“富含TiO2+溶液”中加入Na2CO3粉末易得到固体TiO2• nH2O。请结合原理和化学用语解释其原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某工厂的原料Fe2O3(粉末状)中混入了铜粉,现要测定混合物中的铜粉质量分数并将它们分离,请回答下列问题:
(1)如果要通过化学方法从混合物中分离得到Fe2O3和铜粉,请依次写出分离该混合物操作中涉及的化学方程式___________ (可选择的试剂是:硫酸溶液、硝酸银溶液、氢氧化钠溶液)
(2)若要测定混合物中铜粉的质量分数,可用多种方法,请按测定步骤依次选择下列所示的实验步骤(填编号字母),列举三种方法.提供可选择的实验操作步骤是:(可重复选用)
A.用天平称取混合物W克
B.在空气中充分加热W克混合物
C.将混合物W克加到足量的氯化锌溶液中
D.将混合物W克加到足量的硝酸银溶液中
E.小心过滤
F.在高温加热W克混合物的条件下通入充足的CO
G.根据混合物反应前后的质量变化进行计算
H.用天平称量加热冷却后的混合物质量
I.用天平称量洗涤、干燥后的滤出物质量
方法一:_______________ ;
方法二:________________ ;
方法三:___________________
(1)如果要通过化学方法从混合物中分离得到Fe2O3和铜粉,请依次写出分离该混合物操作中涉及的化学方程式
(2)若要测定混合物中铜粉的质量分数,可用多种方法,请按测定步骤依次选择下列所示的实验步骤(填编号字母),列举三种方法.提供可选择的实验操作步骤是:(可重复选用)
A.用天平称取混合物W克
B.在空气中充分加热W克混合物
C.将混合物W克加到足量的氯化锌溶液中
D.将混合物W克加到足量的硝酸银溶液中
E.小心过滤
F.在高温加热W克混合物的条件下通入充足的CO
G.根据混合物反应前后的质量变化进行计算
H.用天平称量加热冷却后的混合物质量
I.用天平称量洗涤、干燥后的滤出物质量
方法一:
方法二:
方法三:
您最近一年使用:0次



