新型半导体材料如碳化硅(SiC)、氮化镓(GaN)等在国防技术、航空航天及5G技术等领域扮演着重要的角色。
(1)基态Si原子中,核外电子占据的最高能层的符号为______ ,占据最高能级的电子的电子云轮廓图形状为______ 。
(2)基态Ga原子的核外电子排布为[Ar]3d104s2p1,其转化为下列激发态时,吸收能量最少的是______(填选项字母)。
(3)硼(B)与Ga是同主族元素,硼氢化钠(NaBH4)是有机合成中重要的还原剂,基态B原子核外电子有______ 种不同的空间运动状态,其负离子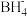 的空间结构为
的空间结构为______ ;另一种含硼负离子的结构如下图所示,其中B原子的杂化轨道类型为______ 。
(4)NH4H2PO4中,除磷元素外,其余三种元素电负性由大到小的顺序是______ (填元素符号),N、P和S第一电离能由大到小的顺序是______ (填元素符号)。
(1)基态Si原子中,核外电子占据的最高能层的符号为
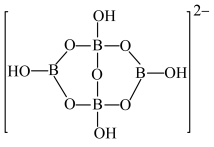
(2)基态Ga原子的核外电子排布为[Ar]3d104s2p1,其转化为下列激发态时,吸收能量最少的是______(填选项字母)。
A.[Ar]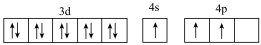 |
B.[Ar]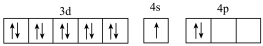 |
C.[Ar]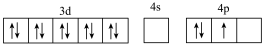 |
D.[Ar]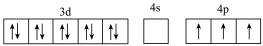 |
(3)硼(B)与Ga是同主族元素,硼氢化钠(NaBH4)是有机合成中重要的还原剂,基态B原子核外电子有
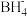 的空间结构为
的空间结构为
(4)NH4H2PO4中,除磷元素外,其余三种元素电负性由大到小的顺序是
更新时间:2023-12-21 12:14:50
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】双奥之城北京,将2008年奥运会的“水立方”进行改造成2022年冬奥会上华的“冰立方”,实现了奥运场馆的再利用。其美丽的透光气囊材料由乙烯(CH2=CH2)与四氟乙烯(CF2=CF2)的聚合物(ETFE)制成。回答下列问题:
(1)F原子价层电子轨道表示式为___________ 。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是___________ (填标号),判断的根据是___________ ;

(3)CF2=CF2和ETFE分子中C的杂化轨道类型分别为___________ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因___________ 。
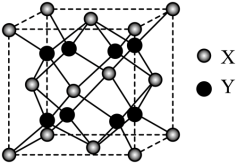
(4)萤石(CaF2)是自然界中常见的含氟矿物,其晶胞结构如图所示,Y代表的离子是___________ ;若该立方晶胞棱长为a pm,该晶体的密度为___________ g/cm3 (列出算式即可,阿伏伽德罗常数用NA表示)
(1)F原子价层电子轨道表示式为
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(3)CF2=CF2和ETFE分子中C的杂化轨道类型分别为
(4)萤石(CaF2)是自然界中常见的含氟矿物,其晶胞结构如图所示,Y代表的离子是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大。元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同。
请回答下列问题:(答题时,X、Y、Z、W、K用所对应的元素符号表示)
(1)Y、Z、W元素的第一电离能由大到小的顺序是_______________ 。
(2)K的电子排布式是___________ 。
(3)Y、Z元素的某些氢化物的分子中均含有18个电子,则Y的这种氢化物的化学式是_______ ;Y、Z的这些氢化物的沸点相差较大的主要原因是__
(4)若X、Y、W形成的某化合物(相对分子质量为46)呈酸性,则该化合物分子中Y原子轨道的杂化类型是____________ ;1 mol该分子中含有 σ键的数目是____________ 。
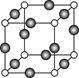
(5)Z、K两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是_______ ,Z原子的配位数是_____ 。
请回答下列问题:(答题时,X、Y、Z、W、K用所对应的元素符号表示)
(1)Y、Z、W元素的第一电离能由大到小的顺序是
(2)K的电子排布式是
(3)Y、Z元素的某些氢化物的分子中均含有18个电子,则Y的这种氢化物的化学式是
(4)若X、Y、W形成的某化合物(相对分子质量为46)呈酸性,则该化合物分子中Y原子轨道的杂化类型是
(5)Z、K两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁元素不仅可以与SCN-、CN-等离子形成配合物,还可以与CO、NO等分子以及许多有机试剂形成配合物.回答下列问题:
(1)基态铁原子有_____________ 个未成对电子;
(2)CN-有毒,含CN-的工业废水必须处理,用TiO2作光催化剂可将废水中的CN-转化为OCN-,并最终氧化为N2、CO2
①C、N、O三种元素的第一电离能由大到小的顺序是_____________ ;
②1molFe(CN)32-中含有σ键的数目为_____________ ;
③铁与CO形成的配合物Fe(CO)3的熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)3晶体属于_____________ (填晶体类型)
(3)乙二胺四乙酸能和Fe2+形成稳定的水溶性配合物乙二胺四乙酸铁钠,原理如图1:
①乙二胺四乙酸中碳原子的杂化轨道类型是_____________ ;
②乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)2]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_____________ ;
(4)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成,小立方体如图2所示,则该合金的化学式为_____________ ,已知小立方体边长为acm,此铁铝合金的密度为_____________ g•cm-3。

(1)基态铁原子有
(2)CN-有毒,含CN-的工业废水必须处理,用TiO2作光催化剂可将废水中的CN-转化为OCN-,并最终氧化为N2、CO2
①C、N、O三种元素的第一电离能由大到小的顺序是
②1molFe(CN)32-中含有σ键的数目为
③铁与CO形成的配合物Fe(CO)3的熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)3晶体属于
(3)乙二胺四乙酸能和Fe2+形成稳定的水溶性配合物乙二胺四乙酸铁钠,原理如图1:
①乙二胺四乙酸中碳原子的杂化轨道类型是
②乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)2]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是
(4)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成,小立方体如图2所示,则该合金的化学式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮、铜及其化合物以及乙醇、氯化钠的用途广泛。回答下列问题:
(1)基态氮原子中含有______ 种运动状态不同的电子,与N3-含有相同电子数的四原子分子是_______ (写化学式),其立体构型是________ 。
(2)C、N、O、F四种元素的第一电离能由小到大的顺序为_____ 。
(3)Cu+价层电子的轨道表达式(电子排布图)为______ 。CuO在高温下能分解生成Cu2O,其原因是_______ 。
(4)在加热和Cu的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是____ ,乙醛分子中H一C—O的键角____ (填“大于”等于”或“小于”)乙醇分子中的H—C—O的键角。
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代后有两种不同的结构,其中[Cu( H2O)2(Cl)2]是非极性分子的结构式为________ 。
(6)如图所示为NaCl晶体的晶胞结构图和晶胞截面图(截面图中的大球为Cl-,小球为Na+);

①晶胞中距离1个Na+最近的Cl-有_____ 个 ,这些C1-围成的图形是___________ 。
②若晶体密度为ρg●cm-3,阿伏加 德罗常数的值用NA表示,则Na+的离子半径为_______ pm(列出计算表达式)。
(1)基态氮原子中含有
(2)C、N、O、F四种元素的第一电离能由小到大的顺序为
(3)Cu+价层电子的轨道表达式(电子排布图)为
(4)在加热和Cu的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代后有两种不同的结构,其中[Cu( H2O)2(Cl)2]是非极性分子的结构式为
(6)如图所示为NaCl晶体的晶胞结构图和晶胞截面图(截面图中的大球为Cl-,小球为Na+);

①晶胞中距离1个Na+最近的Cl-有
②若晶体密度为ρg●cm-3,阿伏加 德罗常数的值用NA表示,则Na+的离子半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】磷及其化合物用途广泛。回答下列问题:
(1)基态P原子核外电子的运动状态有___________ 种,其最高能级的电子云轮廓图为___________ 形。
(2)氟磷酸钙也称氟磷灰石,它的化学式为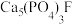 ,是牙釉的主要成分。
,是牙釉的主要成分。
①基态F原子价层电子的轨道表达式为___________ 。
②组成该化合物的四种元素电负性从大到小的顺序为___________ 。
(3)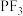 在常温常压下为无色无味的有毒气体,在空气中相当稳定,常用作氟化剂,其与
在常温常压下为无色无味的有毒气体,在空气中相当稳定,常用作氟化剂,其与 的空间结构及相应的键角如图一所示。
的空间结构及相应的键角如图一所示。

①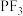 分子中中心原子的杂化方式为
分子中中心原子的杂化方式为___________ 杂化,其空间构型为___________ 。
②稳定性: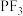
___________ (填“>”“<”或“=”) ;键角:
;键角: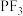 <
< 的原因是
的原因是___________ 。
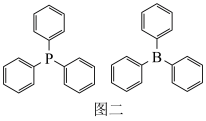
(4)三苯基磷与三苯基硼的结构简式如图二所示。下列说法正确的是___________(填字母)。
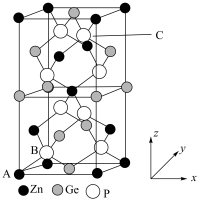
(5)磷锗锌晶体是一种红外非线性晶体,其晶胞结构如图所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,图中A点Zn原子的分数坐标为(0,0,0),B点P原子的坐标为(0.25,0.25,0.125)。
①C点P原子的坐标为___________ 。
②磷锗锌晶体的化学式为___________ 。
(1)基态P原子核外电子的运动状态有
(2)氟磷酸钙也称氟磷灰石,它的化学式为
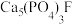 ,是牙釉的主要成分。
,是牙釉的主要成分。①基态F原子价层电子的轨道表达式为
②组成该化合物的四种元素电负性从大到小的顺序为
(3)
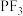 在常温常压下为无色无味的有毒气体,在空气中相当稳定,常用作氟化剂,其与
在常温常压下为无色无味的有毒气体,在空气中相当稳定,常用作氟化剂,其与 的空间结构及相应的键角如图一所示。
的空间结构及相应的键角如图一所示。
①
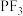 分子中中心原子的杂化方式为
分子中中心原子的杂化方式为②稳定性:
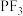
 ;键角:
;键角: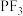 <
< 的原因是
的原因是(4)三苯基磷与三苯基硼的结构简式如图二所示。下列说法正确的是___________(填字母)。

| A.均为极性分子 | B.B、P的杂化方式相同 |
| C.两种分子中所有原子均可共面 | D.三苯基磷的沸点比三苯基硼的高 |
(5)磷锗锌晶体是一种红外非线性晶体,其晶胞结构如图所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,图中A点Zn原子的分数坐标为(0,0,0),B点P原子的坐标为(0.25,0.25,0.125)。

①C点P原子的坐标为
②磷锗锌晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖。
(1)基态Fe2+的核外电子排布式为_________________ 。
(2)氟、氧、砷三种元素中电负性值由大到小的顺序是__________ (用相应的元素符号填空)。
(3)Fe(SCN)3溶液中加入NH4F,发生如下反应:Fe(SCN)3+6NH4F=(NH4)3FeF6+3NH4SCN。
①(NH4)3FeF6存在的微粒间作用力除共价键外还有_________ (选填序号,下同)。
a.配位键 b.氢键 c.金属键 d.离子键
②已知SCN一中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为_____________ ,该原子团中 键与
键与 个数的比值为
个数的比值为___________________ 。
(4)FeCl3晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:_______________________________ 。
(5)氮、磷、砷虽为同主族元素,但其化合物的结构与性质是多样化的。
①该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示,则Y轴可表示的氢化物(RH3)性质可能有________ 。
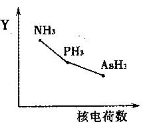
a.稳定性 b.沸点 c.R—H键能 d.分子间作用力
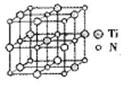
②碳氮化钛化合物在汽车制造和航空航天等领域有广泛的应用,其结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,据此分析,这种碳氮化钛化台物的化学式为______ 。
(1)基态Fe2+的核外电子排布式为
(2)氟、氧、砷三种元素中电负性值由大到小的顺序是
(3)Fe(SCN)3溶液中加入NH4F,发生如下反应:Fe(SCN)3+6NH4F=(NH4)3FeF6+3NH4SCN。
①(NH4)3FeF6存在的微粒间作用力除共价键外还有
a.配位键 b.氢键 c.金属键 d.离子键
②已知SCN一中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为
 键与
键与 个数的比值为
个数的比值为(4)FeCl3晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:
(5)氮、磷、砷虽为同主族元素,但其化合物的结构与性质是多样化的。
①该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示,则Y轴可表示的氢化物(RH3)性质可能有

a.稳定性 b.沸点 c.R—H键能 d.分子间作用力
②碳氮化钛化合物在汽车制造和航空航天等领域有广泛的应用,其结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,据此分析,这种碳氮化钛化台物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】元素A、B、C、D、E、F、G在元素周期表中的位置如图所示,回答下列问题:

(1) 的基态原子核外电子排布式为
的基态原子核外电子排布式为___________ 。原子的第一电离能:D___________ E(填“>”或“<”)。
(2)根据价层电子对互斥理论,价层电子对之间的斥力大小有如下顺序: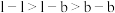 (l为孤电子对,
(l为孤电子对, 为键合电子对),则关于
为键合电子对),则关于 中的
中的 键角可得出的结论是___________。
键角可得出的结论是___________。
(3)化合物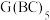 中存在的化学键类型有
中存在的化学键类型有___________ ,它在空气中燃烧生成红棕色氧化物,反应的化学方程式为___________ 。
(4)化合物 的立体构型为
的立体构型为___________ ,其中B原子的杂化轨道类型是___________ ,写出两个与 具有相同立体构型的含氧酸根离子
具有相同立体构型的含氧酸根离子___________ 。

(1)
 的基态原子核外电子排布式为
的基态原子核外电子排布式为(2)根据价层电子对互斥理论,价层电子对之间的斥力大小有如下顺序:
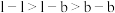 (l为孤电子对,
(l为孤电子对, 为键合电子对),则关于
为键合电子对),则关于 中的
中的 键角可得出的结论是___________。
键角可得出的结论是___________。A. | B.接近 ,但小于 ,但小于 |
C.接近 ,但大于 ,但大于 | D.接近 ,但小于 ,但小于 |
(3)化合物
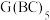 中存在的化学键类型有
中存在的化学键类型有(4)化合物
 的立体构型为
的立体构型为 具有相同立体构型的含氧酸根离子
具有相同立体构型的含氧酸根离子
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】Ⅰ.硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为______ ,基态S原子电子占据最高能级的电子云轮廓图为______ 形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同其他分子的是______ 。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为______ 。
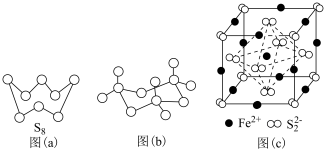
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为______ 形,其中共价键的类型有______ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为______
Ⅱ.
(5)气态氢化物热稳定性HF大于HCl的主要原因是______ 。
(6)CaCN2是离子化合物。各原子均满足8电子稳定结构,CaCN2的电子式是______ 。
(7)常温下,在水中的溶解度乙醇大于氯乙烷,原因是______ 。
Ⅲ.
(8)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为______ 。
(9)NH3、PH3、AsH3的沸点由高到低的顺序为______ (填化学式。下同)。还原性由强到弱的顺序为______ 。键角由大到小的顺序为______ 。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同其他分子的是
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
Ⅱ.
(5)气态氢化物热稳定性HF大于HCl的主要原因是
(6)CaCN2是离子化合物。各原子均满足8电子稳定结构,CaCN2的电子式是
(7)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
Ⅲ.
(8)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为
(9)NH3、PH3、AsH3的沸点由高到低的顺序为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为____ 。(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是____________________ 。
(3)E的最高价氧化物分子的空间构型是__________ ,是____ 分子(填“极性”“非极性”)。
(4)F原子的核外电子排布式是________________ 。
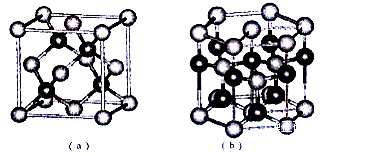
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子),其化学式为_________ 。(a)中E原子的配位数为____ 。若在(b)的结构中取出一个平行六面体作为晶胞,则平均一个晶胞中含有____ 个F原子。结构(a)与(b)中晶胞的原子空间利用率相比,(a)____ (b)(填“>”“<”或“=”)。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是
(3)E的最高价氧化物分子的空间构型是
(4)F原子的核外电子排布式是
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子),其化学式为

您最近一年使用:0次
【推荐1】Co2+能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:

(1)Co2+的基态核外电子排布式为_________ 。
(2)H、N、O电负性大小关系是_________ 。
(3)1mol水杨醛中的σ键的数目为_________ mol。水杨醛缩对氯苯胺中的C原子的杂化方式_________ 。
(4)与H2O互为等电子体的阴离子是_________ 。
(5)Co、Mn、Al形成的合金薄膜的晶胞如图所示,该合金薄膜的化学式为_________ 。
 。
。

(1)Co2+的基态核外电子排布式为
(2)H、N、O电负性大小关系是
(3)1mol水杨醛中的σ键的数目为
(4)与H2O互为等电子体的阴离子是
(5)Co、Mn、Al形成的合金薄膜的晶胞如图所示,该合金薄膜的化学式为
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】 与
与 反应合成HCOOH,是实现“碳中和”的有效途径。回答下列问题:
反应合成HCOOH,是实现“碳中和”的有效途径。回答下列问题:
(1)HCOOH中碳原子的杂化类型为______ 。
(2)已知:
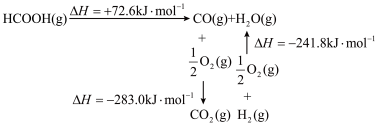

______ 。
(3)在催化作用下,温度为 时,将一定量
时,将一定量 和
和 充入密闭容器中发生如下反应:
充入密闭容器中发生如下反应:
主反应Ⅰ:

副反应Ⅱ:
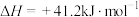 。
。
①下图是不同催化剂电化学还原 生产HCOOH的催化性能及机理,并通过DFT计算催化剂表面该还原过程的物质的相对能量,如图所示(带“*”表示物质处于吸附态)。
生产HCOOH的催化性能及机理,并通过DFT计算催化剂表面该还原过程的物质的相对能量,如图所示(带“*”表示物质处于吸附态)。
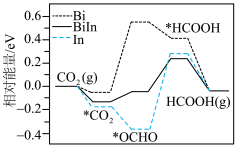
电化学还原 生产HCOOH,使用
生产HCOOH,使用______ 作催化剂较优。
②实验测得反应Ⅰ: ,
, ,
, 、
、 为速率常数。温度为
为速率常数。温度为 时,
时,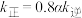 ,则
,则
______  (填“大于”“小于”“等于”),判断依据是
(填“大于”“小于”“等于”),判断依据是______ 。
③实验测得平衡时 的转化率及HCOOH和CO的选择性(产物的选择性:生成的HCOOH或CO与转化的
的转化率及HCOOH和CO的选择性(产物的选择性:生成的HCOOH或CO与转化的 的比值)随温度变化如图所示。
的比值)随温度变化如图所示。
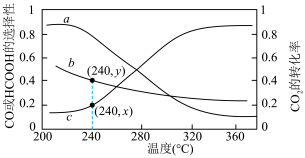
曲线b表示______ ,200℃~360℃,升高温度曲线b对应纵坐标值减小的原因是______ 。240℃时,平衡体系中氢气的分压为 kPa,主反应Ⅰ的
kPa,主反应Ⅰ的
______  (用x、y、
(用x、y、 表示)。
表示)。
 与
与 反应合成HCOOH,是实现“碳中和”的有效途径。回答下列问题:
反应合成HCOOH,是实现“碳中和”的有效途径。回答下列问题:(1)HCOOH中碳原子的杂化类型为
(2)已知:


(3)在催化作用下,温度为
 时,将一定量
时,将一定量 和
和 充入密闭容器中发生如下反应:
充入密闭容器中发生如下反应:主反应Ⅰ:


副反应Ⅱ:

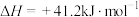 。
。①下图是不同催化剂电化学还原
 生产HCOOH的催化性能及机理,并通过DFT计算催化剂表面该还原过程的物质的相对能量,如图所示(带“*”表示物质处于吸附态)。
生产HCOOH的催化性能及机理,并通过DFT计算催化剂表面该还原过程的物质的相对能量,如图所示(带“*”表示物质处于吸附态)。
电化学还原
 生产HCOOH,使用
生产HCOOH,使用②实验测得反应Ⅰ:
 ,
, ,
, 、
、 为速率常数。温度为
为速率常数。温度为 时,
时,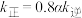 ,则
,则
 (填“大于”“小于”“等于”),判断依据是
(填“大于”“小于”“等于”),判断依据是③实验测得平衡时
 的转化率及HCOOH和CO的选择性(产物的选择性:生成的HCOOH或CO与转化的
的转化率及HCOOH和CO的选择性(产物的选择性:生成的HCOOH或CO与转化的 的比值)随温度变化如图所示。
的比值)随温度变化如图所示。
曲线b表示
 kPa,主反应Ⅰ的
kPa,主反应Ⅰ的
 (用x、y、
(用x、y、 表示)。
表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物。
(1) 是一种很好的配体,
是一种很好的配体, 的VSEPR构型是
的VSEPR构型是_______ 。
(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:
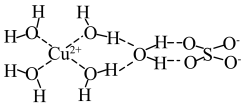
图中虚线表示的作用力为_______ 。
A.氢键 B.离子键 C.配位键
(3)胆矾溶液与氨水在一定条件下可以生成 晶体。在
晶体。在 晶体中,含有的原子团或分子有
晶体中,含有的原子团或分子有 、
、 、
、 、
、 ,
, 为平面正方形结构,中心
为平面正方形结构,中心 能否是
能否是 杂化
杂化_______ (填“是”或“否”),理由是_______ 。请写出该配离子的结构简式:_______ (必须将配位键表示出来)。
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态 ,呈正四面体构型。
,呈正四面体构型。 易溶于
易溶于_______ (填标号)。
A.四氯化碳 B.水 C.硫酸镍溶液 D.苯 E.CS₂
(5)已知1 mol化学键断开时吸收或生成时释放的能量如下: 436 kJ,
436 kJ, 193 kJ,
193 kJ, 946 kJ,
946 kJ, 391 kJ。求:
391 kJ。求: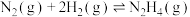 的焓变
的焓变
_______ kJ⋅mol 。
。
(1)
 是一种很好的配体,
是一种很好的配体, 的VSEPR构型是
的VSEPR构型是(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:

图中虚线表示的作用力为
A.氢键 B.离子键 C.配位键
(3)胆矾溶液与氨水在一定条件下可以生成
 晶体。在
晶体。在 晶体中,含有的原子团或分子有
晶体中,含有的原子团或分子有 、
、 、
、 、
、 ,
, 为平面正方形结构,中心
为平面正方形结构,中心 能否是
能否是 杂化
杂化(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态
 ,呈正四面体构型。
,呈正四面体构型。 易溶于
易溶于A.四氯化碳 B.水 C.硫酸镍溶液 D.苯 E.CS₂
(5)已知1 mol化学键断开时吸收或生成时释放的能量如下:
 436 kJ,
436 kJ, 193 kJ,
193 kJ, 946 kJ,
946 kJ, 391 kJ。求:
391 kJ。求: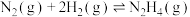 的焓变
的焓变
 。
。
您最近一年使用:0次



