氮、铜及其化合物以及乙醇、氯化钠的用途广泛。回答下列问题:
(1)基态氮原子中含有______ 种运动状态不同的电子,与N3-含有相同电子数的四原子分子是_______ (写化学式),其立体构型是________ 。
(2)C、N、O、F四种元素的第一电离能由小到大的顺序为_____ 。
(3)Cu+价层电子的轨道表达式(电子排布图)为______ 。CuO在高温下能分解生成Cu2O,其原因是_______ 。
(4)在加热和Cu的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是____ ,乙醛分子中H一C—O的键角____ (填“大于”等于”或“小于”)乙醇分子中的H—C—O的键角。
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代后有两种不同的结构,其中[Cu( H2O)2(Cl)2]是非极性分子的结构式为________ 。
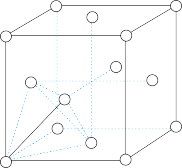
(6)如图所示为NaCl晶体的晶胞结构图和晶胞截面图(截面图中的大球为Cl-,小球为Na+);

①晶胞中距离1个Na+最近的Cl-有_____ 个 ,这些C1-围成的图形是___________ 。
②若晶体密度为ρg●cm-3,阿伏加 德罗常数的值用NA表示,则Na+的离子半径为_______ pm(列出计算表达式)。
(1)基态氮原子中含有
(2)C、N、O、F四种元素的第一电离能由小到大的顺序为
(3)Cu+价层电子的轨道表达式(电子排布图)为
(4)在加热和Cu的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代后有两种不同的结构,其中[Cu( H2O)2(Cl)2]是非极性分子的结构式为
(6)如图所示为NaCl晶体的晶胞结构图和晶胞截面图(截面图中的大球为Cl-,小球为Na+);

①晶胞中距离1个Na+最近的Cl-有
②若晶体密度为ρg●cm-3,阿伏加 德罗常数的值用NA表示,则Na+的离子半径为
2020·黑龙江齐齐哈尔·一模 查看更多[3]
黑龙江省齐齐哈尔市八中2019-2020学年高三一模考试理综化学试题(已下线)押广东卷化学第20题 物质结构与性质综合题-备战2022年高考化学临考题号押题(广东卷)(已下线)专题19 物质结构与性质综合题-备战2023年高考化学母题题源解密(广东卷)
更新时间:2020-03-11 08:40:43
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】科学家预测21 世纪中叶将进入“氢能经济”时代,许多化合物或合金都是具有广阔应用前景的储氢材料。回答下列问题:
(1)基态Li原子核外电子有___ 种不同的运动状态,占据最高能层电子的电子云轮廓图形状为____________ 。
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为___________________ 。
(3)亚氨基锂(Li2NH) 中所含的元素,电负性由大到小排列的顺序是_________ 。
(4)咔唑(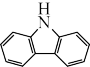 )的沸点比芴(
)的沸点比芴( 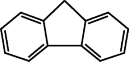 )高的主要原因是
)高的主要原因是___________________ 。
(5)NH3BH3(氨硼烷,熔点104℃)与______ (写出一种分子)互为等电子体。可通过红外光谱测定该分子的立体构型,NH3BH3中B的杂化轨道类型为____________ 。
(6)一种储氢合金的晶胞结构如图所示。在晶胞中Cu 原子处于面心,Au 原子处于顶点位置。该晶体中,原子之间的作用力是___________ 。实现储氢功能时,氢原子可进入到由Cu 原子与Au 原子构成的四面体空隙中心(如图),若所有四面体空隙都填满,该晶体储氢后的化学式为__________ 。已知该晶胞的晶胞参数为a nm,阿伏加 德罗常数值为NA,则密度ρ为__________ g/cm3(用NA和a的代数式表示)
(1)基态Li原子核外电子有
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为
(3)亚氨基锂(Li2NH) 中所含的元素,电负性由大到小排列的顺序是
(4)咔唑(
 )的沸点比芴(
)的沸点比芴(  )高的主要原因是
)高的主要原因是(5)NH3BH3(氨硼烷,熔点104℃)与
(6)一种储氢合金的晶胞结构如图所示。在晶胞中Cu 原子处于面心,Au 原子处于顶点位置。该晶体中,原子之间的作用力是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】[物质结构与性质]
I . 固体二氧化碳外形似冰,受热汽化无液体产生,俗称“干冰”,根据干冰晶胞结构回答:
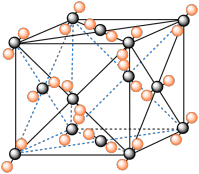
(1)干冰中一个分子周围有__________个紧邻分子。
(2)堆积方式与干冰晶胞类型相同的金属有_________(从“Cu、Mg、K、Po”中选出正确的),其空间利用率为_______。
(3)CO2中心原子的杂化方式为_______,有一种与CO2互为等电子体的离子,能用于鉴别Fe3+ ,写出其电子式______________________。
II. 钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态,+2价和+3价。

(4)写出Cu3+的电子排布式: 。
(5)根据图示晶胞结构,推算晶体中Y,Cu,Ba和O原子个数比,确定其化学式为: 。
(6)根据(5)所推出的化合物的组成,(该化合物中各元素的化合价为Y +3、Ba +2),计算该物质中+2价和+3价的Cu离子个数比为:_______________。
I . 固体二氧化碳外形似冰,受热汽化无液体产生,俗称“干冰”,根据干冰晶胞结构回答:

(1)干冰中一个分子周围有__________个紧邻分子。
(2)堆积方式与干冰晶胞类型相同的金属有_________(从“Cu、Mg、K、Po”中选出正确的),其空间利用率为_______。
(3)CO2中心原子的杂化方式为_______,有一种与CO2互为等电子体的离子,能用于鉴别Fe3+ ,写出其电子式______________________。
II. 钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态,+2价和+3价。

(4)写出Cu3+的电子排布式: 。
(5)根据图示晶胞结构,推算晶体中Y,Cu,Ba和O原子个数比,确定其化学式为: 。
(6)根据(5)所推出的化合物的组成,(该化合物中各元素的化合价为Y +3、Ba +2),计算该物质中+2价和+3价的Cu离子个数比为:_______________。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰: 4Mn(NO3)2·6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH。
(1)Mn3+基态价层电子排布图为________ 。
(2)Mn(NO3)2·6H2O中非金属元素第一电离能从大到小的顺序__________ 。从电子云重叠的方式看N中存在的化学键类型有__________ 。
(3)与NO2-互为等电子体的一种分子的化学式为________ 。
(4)1molCH3COOH中含有的σ键数目为___________ 。CH3COOH分子通过氢键形成环状二聚物,写出含氢键表示的环状二聚物的结构简式___________ 。
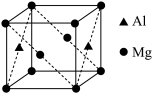
(5)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为_________ 。镁铝合金密度为ρg/cm3,则该晶胞的边长为__________ nm(阿伏加 德罗常数的值为N)。
(1)Mn3+基态价层电子排布图为
(2)Mn(NO3)2·6H2O中非金属元素第一电离能从大到小的顺序
(3)与NO2-互为等电子体的一种分子的化学式为
(4)1molCH3COOH中含有的σ键数目为
(5)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为

您最近一年使用:0次
【推荐1】已知A、B、C、D、E、F、G、H为原子序数依次增大的前36号元素,A的一种同位素原子无中子;B元素基态原子的核外电子数是其能级数的2倍,且含有未成对的电子;D的基态原子2p轨道中含有两种不同自旋方向的电子,且电子数之比为3∶1;E为周期表中电负性最强的元素;F、H与D元素同主族;G位于第四周期第IB族。回答下列问题(用元素符号或化学式表示):
(1)G+的价层电子排布式为_______
(2)B、C、F的原子半径由大到小的顺序为_______ (填元素符号)。
(3)C、D、E的第一电离能由大到小排序是_______ (填元素符号)。
(4)从分子结构与性质角度分析CA3气体易溶于水的原因是_______ ,_______ 。
(5)由A、B、D三种元素形成的餐桌上常见的化合物B2A4D2,一个该分子中含_______ 个键,该分子中所含的化学键的类型为_______ (填序号)。
A.离子键 B.极性共价键 C.非极性共价键
(1)G+的价层电子排布式为
(2)B、C、F的原子半径由大到小的顺序为
(3)C、D、E的第一电离能由大到小排序是
(4)从分子结构与性质角度分析CA3气体易溶于水的原因是
(5)由A、B、D三种元素形成的餐桌上常见的化合物B2A4D2,一个该分子中含
A.离子键 B.极性共价键 C.非极性共价键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】研究发现,在CO2低压合成甲醇反应中(CO2+3H2=CH3OH+H2O),Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景.回答下列问题:
(1)Mn原子价电子排布式为________ ,3d能级上的未成对电子数为________ .
(2)C、H、O 三种元素的电负性由小到大的顺序为______ .
(3)水的沸点________ (填“高于”或“低于”)H2S,原因是________ ;水是________ 分子(填“极性”或“非极性”)
(4)单质铜及镍都是由________ 键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1 958kJ•mol﹣1、INi=1 753kJ•mol﹣1,ICu>INi的原因是________ .
(5)某镍白铜合金的立方晶胞结构如图所示.
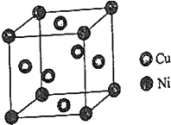
晶胞中铜原子与镍原子的数量比为________ .
②若合金的密度为d g•cm﹣3,晶胞参数a=________ cm.(用含NA和d的式子回答;铜和镍的相对原子质量分别为64、59)
(1)Mn原子价电子排布式为
(2)C、H、O 三种元素的电负性由小到大的顺序为
(3)水的沸点
(4)单质铜及镍都是由
(5)某镍白铜合金的立方晶胞结构如图所示.

晶胞中铜原子与镍原子的数量比为
②若合金的密度为d g•cm﹣3,晶胞参数a=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】镁、铁、铜等在工农业生产中有着广泛的应用。回答下列问题:
(1)铜元素位于元素周期表中的___ 区,其基态原子的价电子排布图为_________ 。
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]SO4溶液,该溶液可用于溶解纤维素。
①[Cu(NH3)4]SO4中阴离子的立体构型是_______ 。
②在[Cu(NH3)4]SO4中,配离子所含有的化学键为________ ,提供孤电子对的成键原子是_______ 。
③ 除硫元素外,[Cu(NH3)4]SO4中所含元素的电负性由小到大的顺序为_______ 。
④NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为_____ 。但NF3不易与Cu2+形成化学键,其原因是____________ 。
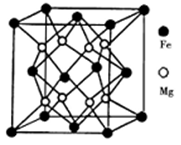
(3)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。则铁镁合金的化学式为________ ,若该晶胞的参数为dnm,则该合金的密度为____ g/cm3(不必化简,用NA表示阿伏伽德罗常数)。
(1)铜元素位于元素周期表中的
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]SO4溶液,该溶液可用于溶解纤维素。
①[Cu(NH3)4]SO4中阴离子的立体构型是
②在[Cu(NH3)4]SO4中,配离子所含有的化学键为
③ 除硫元素外,[Cu(NH3)4]SO4中所含元素的电负性由小到大的顺序为
④NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为
(3)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。则铁镁合金的化学式为

您最近一年使用:0次
【推荐1】第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途。
(1)砷元素的基态原子价电子排布图为_____________ ;
(2)氮元素的单质除了N2外,还有N4,则N4中的N原子的轨道杂化方式为____________ ;
(3)对氨基苯甲醛与邻氨基苯甲醛相比,沸点较高的是_________ (填空“前者”或“后者”),原因是________ ;
(4)王水溶解黄金的反应如下:Au+HNO3+4HCl=H[AuCl4]+NO+2H2O,产物中的H[AuCl4]是配合物,它的配位体是____________ ,Au元素提供_________ ;
(5)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是变通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。已知砷化镓的晶胞结构如图,晶胞参数α=565pm。(黑球:Ga, 白球:As)
(1)砷元素的基态原子价电子排布图为
(2)氮元素的单质除了N2外,还有N4,则N4中的N原子的轨道杂化方式为
(3)对氨基苯甲醛与邻氨基苯甲醛相比,沸点较高的是
(4)王水溶解黄金的反应如下:Au+HNO3+4HCl=H[AuCl4]+NO+2H2O,产物中的H[AuCl4]是配合物,它的配位体是
(5)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是变通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。已知砷化镓的晶胞结构如图,晶胞参数α=565pm。(黑球:Ga, 白球:As)
砷化镓的化学式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为_______ ;单晶硅的晶体类型为_______ 。SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为_______ 。SiCl4可发生水解反应,机理如图:
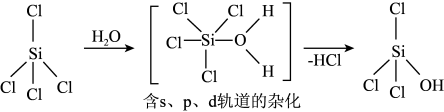
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为_______ (填序号)。
(2)CO2分子中存在_______ 个 键和
键和_______ 个 键。
键。
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是_______ 。
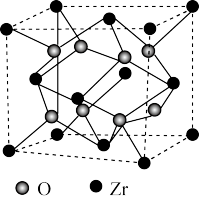
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数是_______ ,晶胞参数为a pm、a pm、c pm,该晶体密度为_______ g·cm-3(写出表达式)。提示:1 pm=1.0×10-1 0cm
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(2)CO2分子中存在
 键和
键和 键。
键。(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝) +3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式_________ 。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有______ 和________ 。含有12mol σ键的K4[Fe(CN)6的物质的量为________ mol。
(3)黄血盐中N原子的杂化方式为______ ;C、N、O的第一电离能由大到小的排序为_____ ,电负性由大到小的排序为________ 。
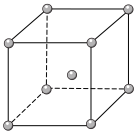
(4)Fe、Na、K的晶体结构如图所示:
① 钠的熔点比钾更高,原因是__________________________ 。
② Fe原子半径是r cm,阿伏加 德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是_______ g/cm3。
(1)写出基态Fe3+的核外电子排布式
(2)K4[Fe(CN)6]中的作用力除共价键外,还有
(3)黄血盐中N原子的杂化方式为
(4)Fe、Na、K的晶体结构如图所示:

① 钠的熔点比钾更高,原因是
② Fe原子半径是r cm,阿伏加 德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】原子序数小于36的X、Y、Z、W四种元素,其中X原子在元素周期表中半径最小,Y原子基态时最外层电子数是其内层电子总数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。
回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为______ , 1 mol Y2X2含有σ键的数目为______ 。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是______ 。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是_______ 。
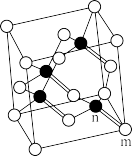
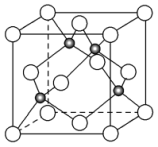
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是___________ ,它可与浓盐酸发生非氧化还原反应,生成配合物HnWCl3,反应的化学方程式为_____________________ 。
回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是

您最近一年使用:0次
【推荐2】氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到 和BN,如图所示:
和BN,如图所示:
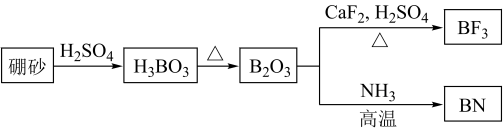
请回答下列问题:
(1) 的电子式为
的电子式为___________ 。
(2)由 制备
制备 的化学方程式是
的化学方程式是___________ , 的结构式为
的结构式为___________ 。
(3)根据对角线规则,B的一些化学性质与元素___________ 的相似。 分子中,
分子中,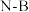 化学键称为
化学键称为___________ 键,其电子对由___________ 提供。氨硼烷在催化剂作用下水解释放氢气: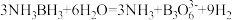 ,
, 的结构如图所示:在该反应中,B原子的杂化轨道类型由
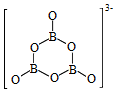
的结构如图所示:在该反应中,B原子的杂化轨道类型由___________ 变为___________ 。与 互为等电子体的阳离子
互为等电子体的阳离子___________ (写一种即可)。
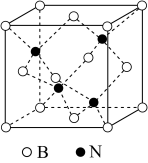
(4)氮化硼晶体有多种结构,如立方氮化硼和六方氮化硼等。立方氮化硼结构与金刚石相似(如图),晶胞边长为apm,立方氮化硼的密度是 。设阿伏加德罗常数值为
。设阿伏加德罗常数值为 。则a=
。则a=___________ (用 、
、 表示)。
表示)。
 和BN,如图所示:
和BN,如图所示:
请回答下列问题:
(1)
 的电子式为
的电子式为(2)由
 制备
制备 的化学方程式是
的化学方程式是 的结构式为
的结构式为(3)根据对角线规则,B的一些化学性质与元素
 分子中,
分子中, 化学键称为
化学键称为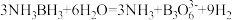 ,
, 的结构如图所示:在该反应中,B原子的杂化轨道类型由
的结构如图所示:在该反应中,B原子的杂化轨道类型由 互为等电子体的阳离子
互为等电子体的阳离子
(4)氮化硼晶体有多种结构,如立方氮化硼和六方氮化硼等。立方氮化硼结构与金刚石相似(如图),晶胞边长为apm,立方氮化硼的密度是
 。设阿伏加德罗常数值为
。设阿伏加德罗常数值为 。则a=
。则a= 、
、 表示)。
表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硅烷广泛应用在现代高科技领域。
制备硅烷的反应为 。
。
(1)①基态硅原子的价层电子轨道表示式为___________ 。
② 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是___________ 。
③下列说法正确的是___________ (填字母)。
a. 的稳定性比
的稳定性比 的差
的差
b. 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c. 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键
④ 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是___________ 。
(2) 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为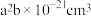 。
。 的
的 模型名称为
模型名称为___________ 。
②用 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为___________  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
制备硅烷的反应为
 。
。(1)①基态硅原子的价层电子轨道表示式为
②
 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是③下列说法正确的是
a.
 的稳定性比
的稳定性比 的差
的差b.
 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c.
 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键④
 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是(2)
 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为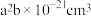 。
。
 的
的 模型名称为
模型名称为②用
 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次



