硅烷广泛应用在现代高科技领域。
制备硅烷的反应为 。
。
(1)①基态硅原子的价层电子轨道表示式为___________ 。
② 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是___________ 。
③下列说法正确的是___________ (填字母)。
a. 的稳定性比
的稳定性比 的差
的差
b. 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c. 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键
④ 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是___________ 。
(2) 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为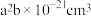 。
。 的
的 模型名称为
模型名称为___________ 。
②用 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为___________  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
制备硅烷的反应为
 。
。(1)①基态硅原子的价层电子轨道表示式为
②
 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是③下列说法正确的是
a.
 的稳定性比
的稳定性比 的差
的差b.
 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c.
 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键④
 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是(2)
 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为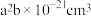 。
。
 的
的 模型名称为
模型名称为②用
 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
更新时间:2024-05-21 11:28:39
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硼(B)和硅(Si)在周期表中处于一条对角线上,有许多相似的性质。请回答:
(1)基态B原子的价层电子轨道表示式是___________ 。
(2)硼与硅相似,也能与氢形成一类化合物——硼烷。常见的有乙硼烷( )、丁硼烷(
)、丁硼烷( )、己硼烷(
)、己硼烷(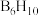 )等。
)等。
①乙硼烷( )分子中的B原子通过氢桥键(
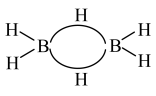
)分子中的B原子通过氢桥键(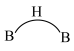 )形成一个四元环,结构式如下图。丁硼烷(
)形成一个四元环,结构式如下图。丁硼烷( )分子中存在4个氢桥键且有两个五元环,写出其结构式
)分子中存在4个氢桥键且有两个五元环,写出其结构式___________ 。
②下列说法不正确 的是___________ 。
A.在自然界中没有游离态的硼,它易与氧化合形成含氧矿物
B.上述硼烷的沸点:乙硼烷<丁硼烷<己硼烷
C. 与
与 中硼原子的杂化方式相同
中硼原子的杂化方式相同
D.硼烷的通式为
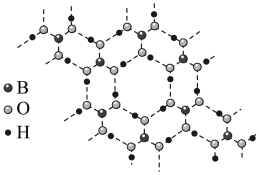
③乙硼烷水解生成硼酸( ),常温常压下硼酸晶体结构为层状,其二维平面结构如图,含
),常温常压下硼酸晶体结构为层状,其二维平面结构如图,含 的晶体中有
的晶体中有___________ mol氢键。
硼酸是一元弱酸,它本身不给出质子,但是溶于水后能给出 。请解释硼酸水溶液呈酸性的原因(用方程式表示)
。请解释硼酸水溶液呈酸性的原因(用方程式表示)___________ 。
(3)磷化硼(BP)是一种重要的半导体材料,在电子学、能源等领域有广泛应用。某种磷化硼晶体的晶胞如图。

①P原子的配位数(紧邻的B原子数)为___________ 。
②图中原子a的坐标为(0,0,1),则原子b的坐标为___________ 。
(1)基态B原子的价层电子轨道表示式是
(2)硼与硅相似,也能与氢形成一类化合物——硼烷。常见的有乙硼烷(
 )、丁硼烷(
)、丁硼烷( )、己硼烷(
)、己硼烷(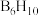 )等。
)等。①乙硼烷(
 )分子中的B原子通过氢桥键(
)分子中的B原子通过氢桥键( )形成一个四元环,结构式如下图。丁硼烷(
)形成一个四元环,结构式如下图。丁硼烷( )分子中存在4个氢桥键且有两个五元环,写出其结构式
)分子中存在4个氢桥键且有两个五元环,写出其结构式
②下列说法
A.在自然界中没有游离态的硼,它易与氧化合形成含氧矿物
B.上述硼烷的沸点:乙硼烷<丁硼烷<己硼烷
C.
 与
与 中硼原子的杂化方式相同
中硼原子的杂化方式相同D.硼烷的通式为

③乙硼烷水解生成硼酸(
 ),常温常压下硼酸晶体结构为层状,其二维平面结构如图,含
),常温常压下硼酸晶体结构为层状,其二维平面结构如图,含 的晶体中有
的晶体中有
硼酸是一元弱酸,它本身不给出质子,但是溶于水后能给出
 。请解释硼酸水溶液呈酸性的原因(用方程式表示)
。请解释硼酸水溶液呈酸性的原因(用方程式表示)(3)磷化硼(BP)是一种重要的半导体材料,在电子学、能源等领域有广泛应用。某种磷化硼晶体的晶胞如图。

①P原子的配位数(紧邻的B原子数)为
②图中原子a的坐标为(0,0,1),则原子b的坐标为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】[化学—选修物质结构和性质]
下表为部分短周期元素的性质或原子结构,已知A—D的原子序数依次增大。
请结合表中信息完成下列各小题(答题时用所对应的元素符号)
A:(1)写出C原子的电子排布图___________
(2)A、B、C、D的第一电离能由大到小的顺序为___________
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因___________
B:按照共价键理论,分子中每个原子的最外电子层电子数均已饱和。已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发。
(4)ABC的结构式是___________ 。向其中插入一个D原子,若形成配位键(用→表示)则ABCD的结构式为___________ ,分子中C的原子的杂化类型是___________ ;若无配位键则ABCD的结构式为___________ 分子中D原子的杂化类型为___________ 。
(5)BD2的电子式是___________ 将D原子换成等电子的 所得ABCD的结构式为
所得ABCD的结构式为___________ ,分子中C原子的杂化类型是___________ 。
(6)在ABCD的三种可能结构中B原子的杂化类型___________ (填“相同”或“不相同”)
下表为部分短周期元素的性质或原子结构,已知A—D的原子序数依次增大。
| 元素编号 | 元素性质或原子结构 |
| A | A原子所处的周期数、族序数、原子序数均相等 |
| B | 核外电子有6种不同运动状态 |
| C | 最简单氢化物的水溶液呈碱性 |
| D | 基态原子的S轨道电子数等于P轨道电子数 |
A:(1)写出C原子的电子排布图
(2)A、B、C、D的第一电离能由大到小的顺序为
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因
B:按照共价键理论,分子中每个原子的最外电子层电子数均已饱和。已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发。
(4)ABC的结构式是
(5)BD2的电子式是
 所得ABCD的结构式为
所得ABCD的结构式为(6)在ABCD的三种可能结构中B原子的杂化类型
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期。
(1) 原子基态时外围电子轨道表示式为
原子基态时外围电子轨道表示式为______ ;
(2)由A、B、C形成的离子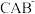 与
与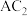 互为等电子体,则
互为等电子体,则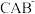 的结构式为
的结构式为______ ;
(3)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域 键”
键” 或大
或大 键
键 。大
。大 键可用
键可用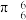 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的电子数和原子个数,如苯分子中大
键的电子数和原子个数,如苯分子中大 键表示为
键表示为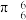
①下列微粒中存在“离域 键”的是
键”的是______ ;
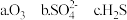
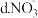
②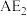 分子中大
分子中大 键可以表示为
键可以表示为______ ;
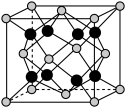
(4) 和D能够形成化合物X,其晶胞结构如图所示,晶胞参数
和D能够形成化合物X,其晶胞结构如图所示,晶胞参数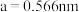 ,晶胞中C原子的配位数为
,晶胞中C原子的配位数为______ ;列式计算晶体X的密度______  。
。
(1)
 原子基态时外围电子轨道表示式为
原子基态时外围电子轨道表示式为(2)由A、B、C形成的离子
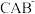 与
与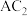 互为等电子体,则
互为等电子体,则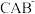 的结构式为
的结构式为(3)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域
 键”
键” 或大
或大 键
键 。大
。大 键可用
键可用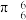 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的电子数和原子个数,如苯分子中大
键的电子数和原子个数,如苯分子中大 键表示为
键表示为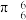
①下列微粒中存在“离域
 键”的是
键”的是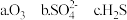
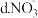
②
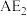 分子中大
分子中大 键可以表示为
键可以表示为(4)
 和D能够形成化合物X,其晶胞结构如图所示,晶胞参数
和D能够形成化合物X,其晶胞结构如图所示,晶胞参数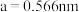 ,晶胞中C原子的配位数为
,晶胞中C原子的配位数为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】按要求填空:
(1)基态Ge原子的核外电子排布式为[Ar]___________ 。
(2) D元素的正三价离子的3d能级为半充满,D的元素符号为___________ ,该原子的原子结构示意图为___________ 。
(3)钒在元素周期表中的位置为___________ ,其价层电子排布图为___________ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为_______ ,其价电子排布图为___________ 。
(5)基态Cr原子有___________ 个未成对电子,Cr 的M层电子排布式为 ___________ 。
(6)铝原子核外电子云有___________ 种不同的伸展方向,有___________ 种不同运动状态的电子。
(7) 在BF3分子中,F—B—F的键角是___________ ,硼原子的杂化轨道类型为___________ ,BF3和过量NaF作用可生成NaBF4,BF 的立体构型为
的立体构型为___________ 。
(1)基态Ge原子的核外电子排布式为[Ar]
(2) D元素的正三价离子的3d能级为半充满,D的元素符号为
(3)钒在元素周期表中的位置为
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为
(5)基态Cr原子有
(6)铝原子核外电子云有
(7) 在BF3分子中,F—B—F的键角是
 的立体构型为
的立体构型为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】镍(Ni)及其化合物广泛应用于电池、电镀和催化剂等领域,一种以电镀废渣(除含镍外,还含有Cu2+、Zn2+、Fe2+等)为原料获得NiSO4·6H2O的流程如图:
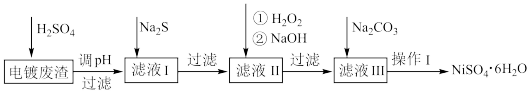
(1)SO 的VSEPR模型为
的VSEPR模型为______ 。
(2)加入Na2S的目的是______ [已知:Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36,Ksp(ZnS)=1.3×10-21,Ksp(NiS)=1.1×10-21]
(3)H2O2为______ (填“极性”或“非极性”)分子,可用氯酸钠代替H2O2,写出氯酸钠与“滤液II”反应的离子方程式:______ 。
(4)向“滤液II”中加入NaOH调节pH在一定范围内可生成氢氧化铁沉淀。已知常温下Fe(OH)3的Ksp=1.0×10-39,若要使溶液中c(Fe3+)≤1.0×10-6mol•L-1,则应该控制溶液pH不小于_____ 。
(5)硫酸镍与硫酸铜类似,向硫酸镍中加入足量氨水可以形成[Ni(NH3)6]SO4蓝色溶液。
①在[Ni(NH3)6]SO4中,Ni2+与NH3之间形成的化学键是_____ ,该物质中配位数是_____ 。
②NH3分子的空间结构为_____ 。

(1)SO
 的VSEPR模型为
的VSEPR模型为(2)加入Na2S的目的是
(3)H2O2为
(4)向“滤液II”中加入NaOH调节pH在一定范围内可生成氢氧化铁沉淀。已知常温下Fe(OH)3的Ksp=1.0×10-39,若要使溶液中c(Fe3+)≤1.0×10-6mol•L-1,则应该控制溶液pH不小于
(5)硫酸镍与硫酸铜类似,向硫酸镍中加入足量氨水可以形成[Ni(NH3)6]SO4蓝色溶液。
①在[Ni(NH3)6]SO4中,Ni2+与NH3之间形成的化学键是
②NH3分子的空间结构为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】据报道,我国化学研究人员用Ni(NO3)2和Tb(CH3COO)3等合成了一个镍的一维链状配位聚合物(如图),对镍配合物在磁性、电化学性质等方面的研究提出了理论指导。
请回答下列问题:
(1)基态Ni原子的价电子轨道表达式为____________ ,Ni在元素周期表中处于第____________ 纵行。
(2)C、N、O三种元素中电负性最大的是____ (填元素符号),C在形成化合物时,其键型以共价键为主,原因是_____________ 。
(3)Ni(NO3)2中阴离子的空间构型是______ ,写出与该阴离子互为等电子体的一种分子的化学式:________ 。
(4)一维链状配位聚合物中,碳原子的杂化形式为________________________ 。
(5)已知: CH3COOH的沸点为117.9℃, HCOOCH3的沸点为32℃,CH3COOH的沸点高于 HCOOCH3的主要原因是______ 。
(6)已知:氧化镍的晶胞结构如图所示。
①若NA为阿伏加 德罗常数的值,晶体密度为ρg·cm-3,则该晶胞中最近的O2-之间的距离为____ pm(用含ρ、NA的代数式表示)。
②某缺陷氧化镍的组成为 Ni0.97O,其中Ni元素只有+2和+3两种价态,两种价态的镍离子数目之比为___ 。
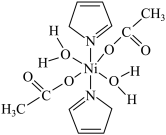
请回答下列问题:
(1)基态Ni原子的价电子轨道表达式为
(2)C、N、O三种元素中电负性最大的是
(3)Ni(NO3)2中阴离子的空间构型是
(4)一维链状配位聚合物中,碳原子的杂化形式为
(5)已知: CH3COOH的沸点为117.9℃, HCOOCH3的沸点为32℃,CH3COOH的沸点高于 HCOOCH3的主要原因是
(6)已知:氧化镍的晶胞结构如图所示。
①若NA为阿伏加 德罗常数的值,晶体密度为ρg·cm-3,则该晶胞中最近的O2-之间的距离为
②某缺陷氧化镍的组成为 Ni0.97O,其中Ni元素只有+2和+3两种价态,两种价态的镍离子数目之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钴元素的用途广泛,据古文献记载:宜德时期青花瓷使用的颜料“苏勃泥青"是从一种进口钴毒矿[主要成分:(FeCo)xAsS]中提取出来的。
(1)Co的价电子排布式为_______
(2)无水CoCl2的熔点是735°C ,沸点1049°C ,CoCl2属于_______ 晶体;砷酸(H3AsO4)分子中As原子的杂化方式为_______ 杂化;砷酸根离子的空间构型为_______ ;第一电离能I1(As)_______ I1(Se)(填“大于”或“小于")。
(3)[Co(NH3)4(H2O)2]Cl3是一种特殊的配合物,其中心离子的配位数是_______ ,每个[Co(NH3)4(H2O)2]3+所含共价键的数目是_______ ,配体NH3的熔沸点大于同族元素氢化物AsH3的原因是_______ 。
(4)钴氰化钾K3[Co(CN)6]是一种浅黄色单斜棱晶体,与配体CN-原子总数相等的等电子体是_______ 。
(5)金属钴晶体的晶胞结构如图所示,其中正六边形的面积为apm2,棱长为bpm;每个Co距离最近且相等的Co原子数目为_______ ; 设阿伏加德罗常数的值为NA,则该晶体的密度为_______ (用含a、b、NA的代数式表示) g·cm-3。

(1)Co的价电子排布式为
(2)无水CoCl2的熔点是735°C ,沸点1049°C ,CoCl2属于
(3)[Co(NH3)4(H2O)2]Cl3是一种特殊的配合物,其中心离子的配位数是
(4)钴氰化钾K3[Co(CN)6]是一种浅黄色单斜棱晶体,与配体CN-原子总数相等的等电子体是
(5)金属钴晶体的晶胞结构如图所示,其中正六边形的面积为apm2,棱长为bpm;每个Co距离最近且相等的Co原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】研究表明TiO2-aNb、Cu(In1-xGaxSe2)是光学活性物质,请回答下列问题:
(1)基态Ti原子核外电子占据的最高能级符号为____ ,Ga、In、Se,第一电离能从大到小顺序为____ 。
(2)SeO 的立体构型为
的立体构型为____ ;SeO2中硒原子采取的杂化类型是____ 。
(3)31Ga可以形成GaCl3•xNH3(x=3,4,5,6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,生成沉淀;过滤后,充分加热滤液有氨气逸出,又有沉淀生成,两次沉淀的物质的量之比为1:2。则该溶质的化学式为____ 。
(4)Cu2+与NH3形成的配离子为[Cu(NH3)4]2+,在该配离子中,氮氢键的键角比独立的氨气分子中键角略大,其原因是____ 。
(5)TiO2通过氮掺杂反应生成TiO2-aNb,可表示如图,则TiO2-aNb晶体中a=____ ,b=____ 。

(1)基态Ti原子核外电子占据的最高能级符号为
(2)SeO
 的立体构型为
的立体构型为(3)31Ga可以形成GaCl3•xNH3(x=3,4,5,6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,生成沉淀;过滤后,充分加热滤液有氨气逸出,又有沉淀生成,两次沉淀的物质的量之比为1:2。则该溶质的化学式为
(4)Cu2+与NH3形成的配离子为[Cu(NH3)4]2+,在该配离子中,氮氢键的键角比独立的氨气分子中键角略大,其原因是
(5)TiO2通过氮掺杂反应生成TiO2-aNb,可表示如图,则TiO2-aNb晶体中a=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】重金属元素具有毒性,常用含巯基(-SH)的有机化合物作为解毒剂。例如,解毒剂化合物I与氧化汞生成化合物II。
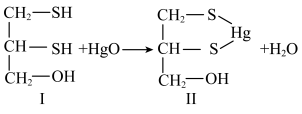
(1)汞的原子序数为80,位于元素周期表第___________ 周期第IIB族。
(2)基态硫原子价电子排布式为___________ 。
(3)H2S、CH4、H2O的沸点由高到低顺序为___________ 。
(4)化合物III也是一种汞解毒剂。下列说法正确的是___________。

(5)理论预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
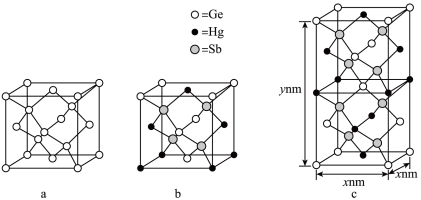
①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是___________ 。
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_______ ;该晶胞中粒子个数比Hg:Ge:Sb = _______ 。
③设X的最简式的式量为M,阿伏加德罗常数为NA.则X晶体的密度为______ g/cm3(列出算式)。

(1)汞的原子序数为80,位于元素周期表第
(2)基态硫原子价电子排布式为
(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)化合物III也是一种汞解毒剂。下列说法正确的是___________。

| A.在I中,O和S原子都采取sp3杂化 |
| B.在II中S元素的电负性最大,更易与Hg结合成键 |
| C.在III中,C-C-C键角是180° |
| D.与化合物I相比,III的水溶性更好 |

①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为
③设X的最简式的式量为M,阿伏加德罗常数为NA.则X晶体的密度为
您最近一年使用:0次



