重金属元素具有毒性,常用含巯基(-SH)的有机化合物作为解毒剂。例如,解毒剂化合物I与氧化汞生成化合物II。
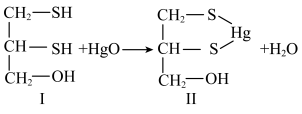
(1)汞的原子序数为80,位于元素周期表第___________ 周期第IIB族。
(2)基态硫原子价电子排布式为___________ 。
(3)H2S、CH4、H2O的沸点由高到低顺序为___________ 。
(4)化合物III也是一种汞解毒剂。下列说法正确的是___________。

(5)理论预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
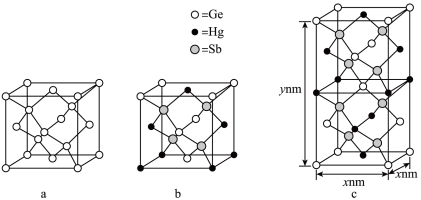
①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是___________ 。
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_______ ;该晶胞中粒子个数比Hg:Ge:Sb = _______ 。
③设X的最简式的式量为M,阿伏加德罗常数为NA.则X晶体的密度为______ g/cm3(列出算式)。

(1)汞的原子序数为80,位于元素周期表第
(2)基态硫原子价电子排布式为
(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)化合物III也是一种汞解毒剂。下列说法正确的是___________。

| A.在I中,O和S原子都采取sp3杂化 |
| B.在II中S元素的电负性最大,更易与Hg结合成键 |
| C.在III中,C-C-C键角是180° |
| D.与化合物I相比,III的水溶性更好 |

①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为
③设X的最简式的式量为M,阿伏加德罗常数为NA.则X晶体的密度为
2023·北京东城·模拟预测 查看更多[3]
更新时间:2023-06-02 09:47:08
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】一种新型硫酸盐功能电解液由2mol·L-1Na2SO4和0.3mol·L-1MgSO4混合组成,电化学测试表明该电解液构建的Na2Ni[Fe(CN)6]、NaTi2(PO4)3/C电池可以稳定循环500次以上。
请回答下列问题:
(1)MgSO4三种原子中电负性最大的元素是_______ (填名称)。
(2)Na2Ni[Fe(CN)6]中,基态Fe2+核外电子的价电子排布式_______ ,[Fe(CN)6]4-中σ键和π键的数目之比为_______ 。
(3)NaTi2(PO4)3中, 中磷原子的杂化类型是
中磷原子的杂化类型是_______ 。
(4)①氨气溶于水时,大部分NH3与H2O用氢键(用“···”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为_______ (填标号)。
A.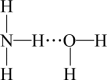 B.
B.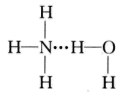
C. D.
D.
②将NH3与CO2以 =2溶于水,充分反应后所得的产物中,阴离子的空间结构为
=2溶于水,充分反应后所得的产物中,阴离子的空间结构为_______ 。
(5)NiaMgbFec的立方晶胞结构如图所示。已知晶胞的边长为npm,设NA为阿伏加德罗常数的值。
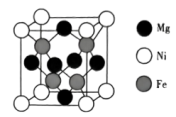
①a:b:c=_______ 。
②该晶体密度是_______ g·cm-3(用含n、NA的代数式表示)。
请回答下列问题:
(1)MgSO4三种原子中电负性最大的元素是
(2)Na2Ni[Fe(CN)6]中,基态Fe2+核外电子的价电子排布式
(3)NaTi2(PO4)3中,
 中磷原子的杂化类型是
中磷原子的杂化类型是(4)①氨气溶于水时,大部分NH3与H2O用氢键(用“···”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为
A.
 B.
B.
C.
 D.
D.
②将NH3与CO2以
 =2溶于水,充分反应后所得的产物中,阴离子的空间结构为
=2溶于水,充分反应后所得的产物中,阴离子的空间结构为(5)NiaMgbFec的立方晶胞结构如图所示。已知晶胞的边长为npm,设NA为阿伏加德罗常数的值。

①a:b:c=
②该晶体密度是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】现有A、B、C、D、E、F六种元素,为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)D的基态原子有___________ 种运动状态的电子,某同学推断D元素基态原子的核外电子轨道表示式为 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了___________ 。
(2)AEC可以做漂白剂,它的电子式为___________ (用元素符号表示);B2A4结构式___________ (用元素符号表示)
(3)C、D、E三种元素的简单离子半径由大到小的顺序是___________ 。(用离子符号表示)
(4)BC 离子的立体构型是
离子的立体构型是___________ ,除σ键外还有___________ 键
(5)下列关于A2C2分子和乙炔分子的说法正确的是___________ 。
a.分子中都含σ键和π键
b.乙炔分子的沸点明显低于A2C2分子
c.都是含极性键和非极性键的非极性分子
d.A2C2分子中C原子杂化方式与乙炔中碳原子杂化方式相同
(6)F元素在周期表中位置为___________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素基态原子未成对电子数在同周期元素中最多 |
| C元素基态原子的核外p能级电子数和s能级电子数相等 |
| D元素基态原子的核外p能级电子数和s能级电子数也相等 |
| E元素的主族序数与周期数的差为4 |
| F元素有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)D的基态原子有
 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了(2)AEC可以做漂白剂,它的电子式为
(3)C、D、E三种元素的简单离子半径由大到小的顺序是
(4)BC
 离子的立体构型是
离子的立体构型是(5)下列关于A2C2分子和乙炔分子的说法正确的是
a.分子中都含σ键和π键
b.乙炔分子的沸点明显低于A2C2分子
c.都是含极性键和非极性键的非极性分子
d.A2C2分子中C原子杂化方式与乙炔中碳原子杂化方式相同
(6)F元素在周期表中位置为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F六种元素均位于元素周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子占据四个原子轨道;D元素原子的成对电子总数是未成对电子总数的3倍;E与D位于同一主族;F位于ds区,且原子的最外层只有1个电子。
(1)基态F核外电子排布式是____ ,最高能级电子的电子云轮廓形状为____ 。
(2)B、C元素的某些氢化物的分子中均含有18个电子,则B元素的这种氢化物的化学式是____ ;B、C元素的这些氢化物的熔、沸点相差较大的主要原因是____ 。
(3)A、B、D可形成分子式为BA2D的某化合物,则该化合物分子中B原子的杂化轨道类型是___ ;A和D还可以形成1:1的化合物,它的电子式为____ 。
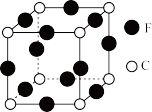
(4)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是____ ,C原子的配位数是____ 。
(1)基态F核外电子排布式是
(2)B、C元素的某些氢化物的分子中均含有18个电子,则B元素的这种氢化物的化学式是
(3)A、B、D可形成分子式为BA2D的某化合物,则该化合物分子中B原子的杂化轨道类型是
(4)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有五种元素A、D、E、M、R,它们的原子序数依次增大,其中A、D、E为短周期主族元素,M、R为第四周期元素.请根据相关信息回答问题.
(1)A元素基态原子具有___________ 种运动状态不同的电子
(2)M在元素周期表中属于___________ 区元素,其基态原子核外共有__________ 个未成对电子
(3) A、D两元素第一电离能大小关系是___________ (用元素符号表示)
(4)E的元素符号为___________
(5)R元素第五电离能与第六电离能相差较大的原因是________________
元素 | 相关信息 |
A | 元素原子的价层电子排布式为 |
D | 原子核外电子占据三个能级,最高能级有两个未成对电子 |
E | 电负性是短周期中最小的 |
M | 在元素周期表的第6列 |
R | 价电子数与A相同.元素第一到第六电离能分别为 , , , , , , , , , , |
(2)M在元素周期表中属于
(3) A、D两元素第一电离能大小关系是
(4)E的元素符号为
(5)R元素第五电离能与第六电离能相差较大的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】I.双氰胺结构简式如图。

(1)双氰胺的晶体类型为_____ 。
(2)双氰胺所含元素中,_____ (填元素名称)元素基态原子核外未成对电子数最多。
(3)双氰胺分子中σ键和π键数目之比为_____
II.硼的最简单氢化物——乙硼烷球棍模型如图,由它制取硼氢化锂的反应为:2LiH + B2H6 =2LiBH4

(4)乙硼烷分子中硼原子的杂化轨道类型为______ 。
(5)BH4-为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为____ (填序号)。
A 离子键 B 金属键 C 氢键 D 配位键 E 极性键 F 非极性键
(6)根据以上反应判断,其中涉及元素的电负性从小到大的顺序为____ (填元素符号)。
Ⅲ.金属铝的晶胞结构如图1所示,原子之间相对位置关系的平面图如图2所示。

(7)晶体铝中原子的堆积方式为_____ 。
(8)已知铝原子半径为a cm,摩尔质量为Mg·mol-1,阿伏伽德罗常数的值为NA,则晶体铝的密度ρ=___ g·cm-3(用含a、M、NA的代数式来表示)。

(1)双氰胺的晶体类型为
(2)双氰胺所含元素中,
(3)双氰胺分子中σ键和π键数目之比为
II.硼的最简单氢化物——乙硼烷球棍模型如图,由它制取硼氢化锂的反应为:2LiH + B2H6 =2LiBH4

(4)乙硼烷分子中硼原子的杂化轨道类型为
(5)BH4-为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为
A 离子键 B 金属键 C 氢键 D 配位键 E 极性键 F 非极性键
(6)根据以上反应判断,其中涉及元素的电负性从小到大的顺序为
Ⅲ.金属铝的晶胞结构如图1所示,原子之间相对位置关系的平面图如图2所示。

(7)晶体铝中原子的堆积方式为
(8)已知铝原子半径为a cm,摩尔质量为Mg·mol-1,阿伏伽德罗常数的值为NA,则晶体铝的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】Mg、Zn、S、B等元素在医药、国防、材料领域应用广泛。请回答下列问题:
(1)Zn元素在周期表中的位置为____ ;基态硫原子核外电子的空间运动状态有____ 种。
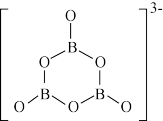
(2)氨硼烷(H3BNH3)是一种安全、高效的储氢材料,H3BNH3分子的结构与乙烷相似,与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从小到大的顺序为____ 。NH3BH3分子中,N—B化学键称为____ 键,其电子对由____ 提供。氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH3+B3O +9H2,B3O
+9H2,B3O 的结构如图所示,在该反应中,B原子的杂化轨道类型由
的结构如图所示,在该反应中,B原子的杂化轨道类型由____ 变为____ 。
(3)三氯化硼是一种重要的化工原料。制备BCl3的原理为B2O3+3C+3Cl2=2BCl3+3CO,BCl3分子的空间构型为____ ,形成BCl3分子时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式为____ (填序号)。
A.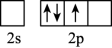 B.
B.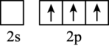 C.
C. D.
D.
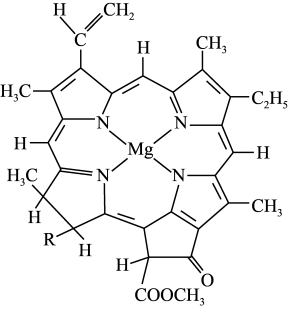
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。卟啉配合物叶绿素是一种,其结构如图所示,其中C原子的杂化方式为____ 。叶绿素的中心离子无论是Mg2+还是Cu2+,都能形成稳定结构,其中稳定性相对较高的是____ (填“Mg2+”或“Cu2+”)。
(1)Zn元素在周期表中的位置为
(2)氨硼烷(H3BNH3)是一种安全、高效的储氢材料,H3BNH3分子的结构与乙烷相似,与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从小到大的顺序为
 +9H2,B3O
+9H2,B3O 的结构如图所示,在该反应中,B原子的杂化轨道类型由
的结构如图所示,在该反应中,B原子的杂化轨道类型由
(3)三氯化硼是一种重要的化工原料。制备BCl3的原理为B2O3+3C+3Cl2=2BCl3+3CO,BCl3分子的空间构型为
A.
 B.
B. C.
C. D.
D.
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。卟啉配合物叶绿素是一种,其结构如图所示,其中C原子的杂化方式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大。元素A、B、C、D、E的原子结构等信息如下:
请回答下列问题:(用A、B、C、D、E,所对应的元素符号作答)
(1)D位于周期表中_______ 区; 的核外电子排布式简写为
的核外电子排布式简写为_______ 。
(2)B、C、D第一电离能由大到小为_______  用元素符号表示
用元素符号表示
(3)A和C形成的四原子分子中,中心原子的杂化方式为_______ 杂化。
(4) 分子中含有
分子中含有 键数目为
键数目为_______ 。
(5)E的单质与C的最高价氧化物水化物的稀溶液反应的离子方程式为_______ 。
| 元素 | 元素性质或原子结构 |
| A | 周期表中原子半径最小的元素 |
| B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
| C | 最外层p轨道半充满 |
| D | 位于短周期,其原子的核外成对电子数是未成对电子数的 倍 倍 |
| E | 位于 区且原子的最外层电子数与A的相同 区且原子的最外层电子数与A的相同 |
(1)D位于周期表中
 的核外电子排布式简写为
的核外电子排布式简写为(2)B、C、D第一电离能由大到小为
 用元素符号表示
用元素符号表示
(3)A和C形成的四原子分子中,中心原子的杂化方式为
(4)
 分子中含有
分子中含有 键数目为
键数目为(5)E的单质与C的最高价氧化物水化物的稀溶液反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】【物质结构与性质】硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式____________ 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),结构如图
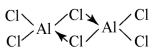
缔合双分子Al2Cl6中Al原子的轨道杂化类型是_______ 。
(3)B原子的电子有_____ 个不同的能级;晶体硼熔点为2300℃,则其为_____ 晶体。
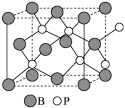
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,它是通过在高温氢气氛围下(>750℃)三溴化硼和三溴化磷反应制得。BP晶胞如图所示。
①画出三溴化硼和三溴化磷的空间结构式。
三溴化硼___________________ 三溴化磷____________________
②在BP晶胞中B的堆积方式为__________________ 。
③计算当晶胞晶格参数为a pm(即图中立方体的每条边长为 a pm)时,磷化硼中硼原子和磷原子之间的最近距离____________ 。
(1)写出基态镓原子的电子排布式
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),结构如图

缔合双分子Al2Cl6中Al原子的轨道杂化类型是
(3)B原子的电子有
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,它是通过在高温氢气氛围下(>750℃)三溴化硼和三溴化磷反应制得。BP晶胞如图所示。

①画出三溴化硼和三溴化磷的空间结构式。
三溴化硼
②在BP晶胞中B的堆积方式为
③计算当晶胞晶格参数为a pm(即图中立方体的每条边长为 a pm)时,磷化硼中硼原子和磷原子之间的最近距离
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】向蓝色的CuSO4溶液中加入过量浓氨水,溶液中产生深蓝色的[Cu(NH3)4]2+。继续向该溶液中加入95%的乙醇,析出[Cu(NH3)4]SO4•H2O晶体。请结合实验情境与所学知识回答下列问题:
(1)在高温下,Cu2O比CuO稳定,从离子的电子层结构角度分析原因_______________________
(2)CuSO4溶液显蓝色是由于Cu2+与H2O结合形成[Cu(H2O)4]2+,画出该离子的结构_________ ,1mol该离子中含有σ键的数量为_____
(3)SO 的空间结构为
的空间结构为_______ ,其中S原子的杂化类型为________
(4)[Cu(NH3)4]2+其实为[Cu(NH3)4(H2O)2]2+的简略写法。该配离子的空间结构为狭长八面体(如图所示)。
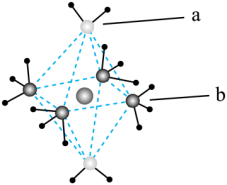
下列关于a、b两种配体的说法不正确 的是_________ (填数字)。
①中心原子的杂化方式相同 ②价电子对的空间结构相同
③分子的热稳定性a弱于b ④配体结合中心离子的能力a强于b
(5)[Cu(NH3)4]SO4•H2O中存在的化学键有_________ (填字母)。
a.离子键 b.配位键 c.非极性键 d.极性键 e.金属键
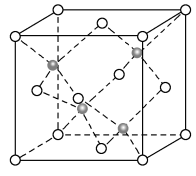
(6)Cu与F形成的化合物的晶胞结构如图所示,则该物质化学式为____________ ;若晶体密度为a g·cm-3,则Cu与F最近距离为______________ pm。(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;图中○为Cu, 为F)
为F)
(1)在高温下,Cu2O比CuO稳定,从离子的电子层结构角度分析原因
(2)CuSO4溶液显蓝色是由于Cu2+与H2O结合形成[Cu(H2O)4]2+,画出该离子的结构
(3)SO
 的空间结构为
的空间结构为(4)[Cu(NH3)4]2+其实为[Cu(NH3)4(H2O)2]2+的简略写法。该配离子的空间结构为狭长八面体(如图所示)。

下列关于a、b两种配体的说法
①中心原子的杂化方式相同 ②价电子对的空间结构相同
③分子的热稳定性a弱于b ④配体结合中心离子的能力a强于b
(5)[Cu(NH3)4]SO4•H2O中存在的化学键有
a.离子键 b.配位键 c.非极性键 d.极性键 e.金属键
(6)Cu与F形成的化合物的晶胞结构如图所示,则该物质化学式为
 为F)
为F)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】K、Al、Si、Cu、N i均为重要的合金材料,在工业生产、科技、国防领域有着广泛的用途,请回答下列问题:
(1)K元素处于元素周期表的_____ 区。
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是______ (填标号)。
A. [Ne] B. [Ne]
B. [Ne]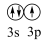 C. [Ne]
C. [Ne] 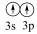 D. [Ne]
D. [Ne]
(3)从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因是_____________ 。
(4)一些化合物的熔点如下表所示:
解释表中化合物之间熔点差异的原因________________________________ 。
(5)NiSO4溶于氨水形成[Ni (NH3)6]SO4。
①N、O、S三种元素中电负性最大的是_______ 。
②写出一种与[Ni (NH3)6]SO4中的阴离子互为等电子体的分子的分子式_________ 。
③1mol[Ni (NH3)6]SO4中含有δ键的数目为___________ 。
④NH3的VSEPR模型为____ ;NH3、SO42-的中心原子的杂化类型分别为___ 、___ 。
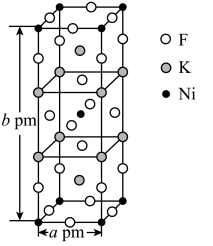
(6)K、Ni、F三种元素组成的一种晶体的长方体晶胞结构如图所示。若NA为阿伏加 德罗常数的值,该晶体的密度ρ=______ g·cm-3(用代数式表示)。
(1)K元素处于元素周期表的
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是
A. [Ne]
 B. [Ne]
B. [Ne] C. [Ne]
C. [Ne]  D. [Ne]
D. [Ne]
(3)从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因是
(4)一些化合物的熔点如下表所示:
| 化合物 | NaCl | KCl | SiO2 |
| 熔点/°C | 801 | 770 | 1723 |
解释表中化合物之间熔点差异的原因
(5)NiSO4溶于氨水形成[Ni (NH3)6]SO4。
①N、O、S三种元素中电负性最大的是
②写出一种与[Ni (NH3)6]SO4中的阴离子互为等电子体的分子的分子式
③1mol[Ni (NH3)6]SO4中含有δ键的数目为
④NH3的VSEPR模型为

(6)K、Ni、F三种元素组成的一种晶体的长方体晶胞结构如图所示。若NA为阿伏加 德罗常数的值,该晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】某课题组在光子晶体领域取得新进展,成功制备出高质量硫化锌光子晶体。回答下列问题:
(1)基态硫原子的价电子排布图为___________ 。第一电离能介于 、P之间的第三周期元素为
、P之间的第三周期元素为__________ 。
(2) 中S的价层电子对数为
中S的价层电子对数为_______ , 中S的杂化类型为
中S的杂化类型为________ , 的立体构型为
的立体构型为_______ 。
(3)硫酸锌溶于氨水可生成 溶液,
溶液, 中含有
中含有 键的数目为
键的数目为____ ( 为阿伏加 德罗常数的值)。与
为阿伏加 德罗常数的值)。与 互为等电子体的分子有
互为等电子体的分子有__________ (任写一种)
(4)硫化锌的晶胞结构如图所示,该晶胞中与硫原子距离最近且相等的硫原子有_____ 个,若该晶胞的密度为 ,用
,用 代表阿伏加 德罗常数的值,则晶胞边长为
代表阿伏加 德罗常数的值,则晶胞边长为_______  。
。

(1)基态硫原子的价电子排布图为
 、P之间的第三周期元素为
、P之间的第三周期元素为(2)
 中S的价层电子对数为
中S的价层电子对数为 中S的杂化类型为
中S的杂化类型为 的立体构型为
的立体构型为(3)硫酸锌溶于氨水可生成
 溶液,
溶液, 中含有
中含有 键的数目为
键的数目为 为阿伏加 德罗常数的值)。与
为阿伏加 德罗常数的值)。与 互为等电子体的分子有
互为等电子体的分子有(4)硫化锌的晶胞结构如图所示,该晶胞中与硫原子距离最近且相等的硫原子有
 ,用
,用 代表阿伏加 德罗常数的值,则晶胞边长为
代表阿伏加 德罗常数的值,则晶胞边长为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】学习物质结构和性质的知识,能使你想象的翅膀变得更加有力。
(1) 的空间结构为
的空间结构为_______ ,属于_______ 分子(填“极性”或“非极性”)。
(2)我国空间站日常运行所需电源主要由太阳能电池提供,太阳能电池主要材料是砷化镓(GaAs)、碲化镉(CdTe),它们可以直接把光能转化成电能给空间站供电。
①Cd与Zn是相邻周期同族元素,基态Cd的价电子排布为_______ 。
②砷化镓(GaAs)能够承受太空高温环境,原因是_______ 。
(3)二个甲酸分子通过氢键形成二聚体(含八元环),画出该二聚体的结构:_______ 。
(4)具有高稳定性、超导电性的二维硼烯氧化物( )的部分结构如图所示,则该氧化物的化学式为
)的部分结构如图所示,则该氧化物的化学式为_______ ,其中B-B键的键长_______ B-O键的键长(填“>”“<”或“=”)。

(1)
 的空间结构为
的空间结构为(2)我国空间站日常运行所需电源主要由太阳能电池提供,太阳能电池主要材料是砷化镓(GaAs)、碲化镉(CdTe),它们可以直接把光能转化成电能给空间站供电。
①Cd与Zn是相邻周期同族元素,基态Cd的价电子排布为
②砷化镓(GaAs)能够承受太空高温环境,原因是
(3)二个甲酸分子通过氢键形成二聚体(含八元环),画出该二聚体的结构:
(4)具有高稳定性、超导电性的二维硼烯氧化物(
 )的部分结构如图所示,则该氧化物的化学式为
)的部分结构如图所示,则该氧化物的化学式为
您最近一年使用:0次



