过渡金属元素在工业生产中发挥着重要作用。技术人员晒制蓝图时,用K3[Fe(C2O4)3]●3H2O(三草酸合铁酸钾晶体)作感光剂,再以K3[Fe(CN)6](六氰合铁酸钾)溶液作显影剂。
请回答以下问题:
(1)铁元素位于元素周期表的___________ 区,Fe3+的基态价电子排布图为___________ ;在上述两种钾盐中第一电离能最大的元素为___________ 。
(2)C与Si为同主族元素,高纯硅制备过程中会生成SiHCl3、SiCl4等中间产物。 已知电负性:H>Si,则SiHCl3中H的化合价为___________ ;SiCl4中硅原子的杂化类型是___________ ; 沸点:SiHCl3<SiC14原因是___________ 。
(3)复兴号亚运智能动车组列车材质用到Mn、Co等元素。Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],CH3CN中σ 键与π 键数目之比为___________ ;CH3CN与Mn形成___________ 键。
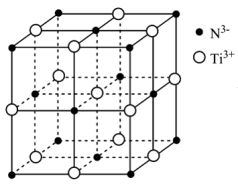
(4)时速600千米的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图),晶胞参数(晶胞棱长)为a D(1D= 10-10m),其中阴离子(N3-)采用面心立方最密堆积方式,则1个晶胞中含有___________ 个TiN;该氮化钛的密度为___________ g/cm3(列出计算式,阿伏加德罗常数的值为NA)。
请回答以下问题:
(1)铁元素位于元素周期表的
(2)C与Si为同主族元素,高纯硅制备过程中会生成SiHCl3、SiCl4等中间产物。 已知电负性:H>Si,则SiHCl3中H的化合价为
(3)复兴号亚运智能动车组列车材质用到Mn、Co等元素。Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],CH3CN中σ 键与π 键数目之比为
(4)时速600千米的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图),晶胞参数(晶胞棱长)为a D(1D= 10-10m),其中阴离子(N3-)采用面心立方最密堆积方式,则1个晶胞中含有

更新时间:2024-01-07 17:28:22
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
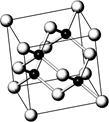
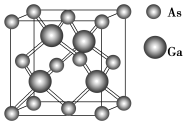
【推荐1】砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措,已知砷化镓的晶胞结构如右图。试回答下列问题
(1)下列说法正确的是_______ (选填序号)。
A.砷化镓晶胞结构与NaCl相同
B.第一电离能:As>Ga
C.电负性:As>Ga
D.砷和镓都属于p区元素
E.半导体GaP、SiC与砷化镓为等电子体
(2)砷化镓是将(CH3)3Ga和AsH3用MOCVD方法制备得到,该反应在700℃进行,反应的方程式为:_______ 。AsH3空间形状为:_______ (CH3)3Ga中镓原子杂化方式为:_______ 。
(3)Ga的核外电子排布式为:_______ 。
(4)AsH3沸点比NH3低,其原因是:_______ 。

(1)下列说法正确的是
A.砷化镓晶胞结构与NaCl相同
B.第一电离能:As>Ga
C.电负性:As>Ga
D.砷和镓都属于p区元素
E.半导体GaP、SiC与砷化镓为等电子体
(2)砷化镓是将(CH3)3Ga和AsH3用MOCVD方法制备得到,该反应在700℃进行,反应的方程式为:
(3)Ga的核外电子排布式为:
(4)AsH3沸点比NH3低,其原因是:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】VA族元素及其化合物在生产、生活中用途广泛。
(1)① 常用于制造火柴,P和S的第一电离能较大的是
常用于制造火柴,P和S的第一电离能较大的是______ 。
② 俗称雄黄,其中基态
俗称雄黄,其中基态 原子的核外电子排布式为
原子的核外电子排布式为______ ,有______ 个未成对电子。
③P、S、 电负性由大到小的顺序是
电负性由大到小的顺序是______ 。
(2) 、
、 、
、 中沸点最高的是
中沸点最高的是______ ,其主要原因是______ 。
(3)白磷在氯气中燃烧可以得到 和
和 ,其中气态
,其中气态 分子的立体构型为
分子的立体构型为______ 。
(1)①
 常用于制造火柴,P和S的第一电离能较大的是
常用于制造火柴,P和S的第一电离能较大的是②
 俗称雄黄,其中基态
俗称雄黄,其中基态 原子的核外电子排布式为
原子的核外电子排布式为③P、S、
 电负性由大到小的顺序是
电负性由大到小的顺序是(2)
 、
、 、
、 中沸点最高的是
中沸点最高的是(3)白磷在氯气中燃烧可以得到
 和
和 ,其中气态
,其中气态 分子的立体构型为
分子的立体构型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有a、b、c、d、e五种前四周期的元素,它们的原子序数依次增大,请根据下列相关信息,回答有关问题:
(1)元素a的名称是_______ ,b元素的基态电子排布式_______ ,c元素在元素周期表中的位置_______ 。
(2)d元素基态原子中最高能层符号是_______ ,核外电子的空间运动状态有_______ 种。
(3)e元素处于周期表的_______ 区,价层电子排布图为_______ 。
(4)元素a、b、d的电负性由大到小的顺序是_______ (用元素符号表示);元素c的第一电离能比元素d的要小,原因是_______ 。
(5)元素b、c、d的最高价氧化物的水化物酸性由强到弱的顺序是_______ (用化学式表示)。
| a元素的核外电子数等于电子层数 |
| b元素基态原子的核外s电子是p电子的2倍 |
| c元素最高正价与最低负价的代数和为4 |
d元素的价层电子排布式为: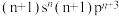 |
| e元素基态原子中单电子数是本周期中最多的元素 |
(2)d元素基态原子中最高能层符号是
(3)e元素处于周期表的
(4)元素a、b、d的电负性由大到小的顺序是
(5)元素b、c、d的最高价氧化物的水化物酸性由强到弱的顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】青蒿素是从黄花蒿中提取的一种无色针状晶体,双氢青蒿素是青蒿素的重要衍生物,抗疟疾疗效优于青蒿素,请回答下列问题:

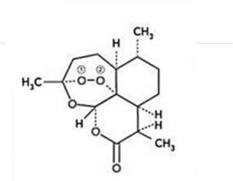
(1)组成青蒿素的三种元素电负性由大到小排序是__________ ,画出基态O原子的价电子排布图__________ 。
(2)一个青蒿素分子中含有_______ 个手性碳原子。
(3)双氢青蒿素的合成一般是用硼氢化钠(NaBH4)还原青蒿素.硼氢化物的合成方法有: 2LiH+B2H6=2LiBH4; 4NaH+BF3═NaBH4+3NaF
①写出BH4﹣的等电子体_________ (分子、离子各写一种);
②B2H6分子结构如图,2个B原子和一个H原子共用2个电子形成3中心二电子键,中间的2个氢原子被称为“桥氢原子”,它们连接了2个B原子.则B2H6分子中有______ 种共价键;
③NaBH4的阴离子中一个B原子能形成4个共价键,而冰晶石(Na3AlF6)的阴离子中一个Al原子可以形成6个共价键,原因是______________ ;
④NaH的晶胞如图,则NaH晶体中阳离子的配位数是_________ ;设晶胞中阴、阳离子为刚性球体且恰好相切,求阴、阳离子的半径比 =
=__________ 由此可知正负离子的半径比是决定离子晶体结构的重要因素,简称几何因素,除此之外影响离子晶体结构的因素还有_________ 、_________ 。


(1)组成青蒿素的三种元素电负性由大到小排序是
(2)一个青蒿素分子中含有
(3)双氢青蒿素的合成一般是用硼氢化钠(NaBH4)还原青蒿素.硼氢化物的合成方法有: 2LiH+B2H6=2LiBH4; 4NaH+BF3═NaBH4+3NaF
①写出BH4﹣的等电子体
②B2H6分子结构如图,2个B原子和一个H原子共用2个电子形成3中心二电子键,中间的2个氢原子被称为“桥氢原子”,它们连接了2个B原子.则B2H6分子中有
③NaBH4的阴离子中一个B原子能形成4个共价键,而冰晶石(Na3AlF6)的阴离子中一个Al原子可以形成6个共价键,原因是
④NaH的晶胞如图,则NaH晶体中阳离子的配位数是
 =
=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】最近我国科研人员成功攻克了5G通信芯片制造中关键材料氮化镓(GaN)的研制难题。已知元素镓(Ga)与Al、N与As分别是同主族的元素,请回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]______ 。
(2)根据元素周期律,元素的电负性Ga______ (填“大于”或“小于”,下同)As;
(3)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与______ 个氮原子相连,氮化铝晶体属于______ 晶体。
(4)NH3是氮的氢化物,中心原子的杂化方式是______ ,NH3的沸点比AsH3高的原因是______ 。
(5)共价晶体GaAs的晶胞参数y=xpm,它的晶胞结构如下图所示,该晶胞内部存在的共价键数为______ ;紧邻的As原子之间的距离为a,紧邻的As、Ga原子之间的距离为b,则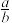 =
=______ 。该晶胞的密度为______ g·cm-3(阿伏伽德罗常数用NA表示)。
(1)基态Ga原子的核外电子排布式为[Ar]
(2)根据元素周期律,元素的电负性Ga
(3)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与
(4)NH3是氮的氢化物,中心原子的杂化方式是
(5)共价晶体GaAs的晶胞参数y=xpm,它的晶胞结构如下图所示,该晶胞内部存在的共价键数为
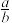 =
=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A、B、C是同一周期的非金属元素。A的最外层电子数是次外层的2倍,C为地壳中含量最高的元素,D的二价阳离子与C的阴离子具有相同的电子层结构。E的原子序数为24,请用化学用语回答下列问题:
(1) A、B、C的第一电离能由小到大的顺序为______ ,电负性由大到小的顺序为______ 。
(2)C的核外电子的轨道排布式为______ ,E的核外价层电子排布式是______ 。
(3)写出化合物 的电子式
的电子式______ ,单质 的结构式
的结构式______ 。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到零价,该反应的化学方程式是______ 。
(1) A、B、C的第一电离能由小到大的顺序为
(2)C的核外电子的轨道排布式为
(3)写出化合物
 的电子式
的电子式 的结构式
的结构式(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到零价,该反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】黑火药是我国古代的四大发明之一,距今已有1000多年的历史。黑火药在发生爆炸时发生的反应为: (已配平)。回答下列问题:
(已配平)。回答下列问题:
(1)K原子激发态的电子排布式有_______ ,其中能量较高的是_______ 。(填标号)
a.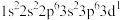 b.
b.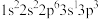
c.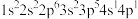 d.
d.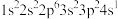
(2)在生成物中,A的电子式为_______ 。
(3)已知 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为_______ 。
(4)第VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含第VIA族元素的化合物在研究和生产中有许多重要用途。
①O、S、Se原子的第一电离能由大到小的顺序为_______ 。
② 的酸性比
的酸性比 的酸性
的酸性_______ (填“强”或“弱”)。气态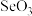 分子中Se的杂化方式为
分子中Se的杂化方式为_______ , 离子的VSEPR模型名称为
离子的VSEPR模型名称为_______ 。
 (已配平)。回答下列问题:
(已配平)。回答下列问题:(1)K原子激发态的电子排布式有
a.
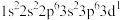 b.
b.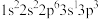
c.
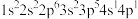 d.
d.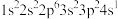
(2)在生成物中,A的电子式为
(3)已知
 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为(4)第VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含第VIA族元素的化合物在研究和生产中有许多重要用途。
①O、S、Se原子的第一电离能由大到小的顺序为
②
 的酸性比
的酸性比 的酸性
的酸性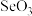 分子中Se的杂化方式为
分子中Se的杂化方式为 离子的VSEPR模型名称为
离子的VSEPR模型名称为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】Ⅰ.元素Fe、C、卤素元素等形成的材料在工业、生活、国防中有很大的作用。请回答下列问题:
(1)基态Fe原子核外电子的空间运动状态有_______ 种,实验室常用邻二氮菲(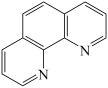 )检验Fe2+ ,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为
)检验Fe2+ ,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为_______ 。
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(2)拟卤素( CN)2、( SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足8电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H- S- C≡N )的沸点低于异硫氰酸(H -N=C=S),其原因是_______ 。
(3)卤化物RbICl2在加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为_______ ; 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为_______ 。
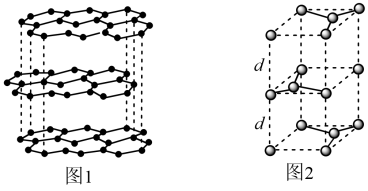
(4)碳的一种同素异形体---石墨,其晶体结构及晶胞如图1、图2所示。则石墨晶胞含碳原子个数为_______ 个。已知石墨的密度为ρg· cm-3 ,C-C键键长为r cm ,阿伏加德罗常数的值为NA,计算石墨晶体的层间距d为_______ cm。
(1)基态Fe原子核外电子的空间运动状态有
 )检验Fe2+ ,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为
)检验Fe2+ ,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(2)拟卤素( CN)2、( SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足8电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H- S- C≡N )的沸点低于异硫氰酸(H -N=C=S),其原因是
(3)卤化物RbICl2在加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为
 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为(4)碳的一种同素异形体---石墨,其晶体结构及晶胞如图1、图2所示。则石墨晶胞含碳原子个数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】2021年7月4日,“神舟十二号”航天员圆满完成出舱任务。“神舟十二号”制作材料中包含了 、
、 、
、 、
、 等多种元素。回答下列问题:
等多种元素。回答下列问题:
(1) 元素基态原子的外围电子排布式为
元素基态原子的外围电子排布式为___________ , 、
、 、
、 三种元素的第一电离能由大到小的顺序为
三种元素的第一电离能由大到小的顺序为___________ 。
(2) 位于元素周期表的
位于元素周期表的___________ (填“s”、“p”、“d”或“ds”)区, 催化烯烃硝化反应过程中会产生
催化烯烃硝化反应过程中会产生 。键角:
。键角:
___________  (填“<”或“>”),判断依据是
(填“<”或“>”),判断依据是___________ 。
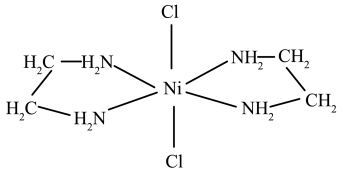
(3)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物。 的一种螯合物结构如图所示,
的一种螯合物结构如图所示,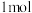 该配合物中通过鳌合作用形成的配位键有
该配合物中通过鳌合作用形成的配位键有___________ 个,该整合物中C的杂化方式为___________ 。
 、
、 、
、 、
、 等多种元素。回答下列问题:
等多种元素。回答下列问题:
(1)
 元素基态原子的外围电子排布式为
元素基态原子的外围电子排布式为 、
、 、
、 三种元素的第一电离能由大到小的顺序为
三种元素的第一电离能由大到小的顺序为(2)
 位于元素周期表的
位于元素周期表的 催化烯烃硝化反应过程中会产生
催化烯烃硝化反应过程中会产生 。键角:
。键角:
 (填“<”或“>”),判断依据是
(填“<”或“>”),判断依据是(3)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物。
 的一种螯合物结构如图所示,
的一种螯合物结构如图所示,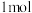 该配合物中通过鳌合作用形成的配位键有
该配合物中通过鳌合作用形成的配位键有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E是元素周期表中前四周期的五种常见元素,其原子序数依次增大。详细信息见表,请回答下列问题:
(1)D的价电子排布式可表示为_______ 。
(2)BC3-的空间构型为____ (用文字描述)。
(3)根据等电子原理,AC分子的结构式为_____ 。
(4)1 mol AC2中σ键、π键数目之比为____ 。
(5)将白色的ESO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配合离子。请写出生成此配合离子的离子方程式:____ 。
(6)E2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[E(NH3)4]2+中存在的化学键类型有____ (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②[E(NH3)4]2+具有对称的空间构型,[E(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[E(NH3)4]2+的空间构型为_____ 。其中,配体的杂化类型是_____ 。
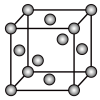
(7)E的晶胞如下图所示,E为______ 堆积,空间利用率为_____ ,E晶体中每个E原子周围距离最近的E原子数目为____ ;已知E原子的半径为a nm,阿伏加 德罗常数的值为NA,则E晶体的密度是_____ g·cm-3。(列出算式即可)。
| ① | A的一种核素在考古时常用来鉴定一些文物的年代 |
| ② | B的氧化物是导致光化学烟雾的主要物质之一 |
| ③ | C的某一种单质是空气的主要成分之一 |
| ④ | D的基态原子核外有6个原子轨道处于半充满状态 |
| ⑤ | E能形成红色的E2O和黑色的EO两种氧化物 |
(2)BC3-的空间构型为
(3)根据等电子原理,AC分子的结构式为
(4)1 mol AC2中σ键、π键数目之比为
(5)将白色的ESO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配合离子。请写出生成此配合离子的离子方程式:
(6)E2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[E(NH3)4]2+中存在的化学键类型有
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②[E(NH3)4]2+具有对称的空间构型,[E(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[E(NH3)4]2+的空间构型为
(7)E的晶胞如下图所示,E为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】I.氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。

(1)基态硼原子的电子排布式为____ 。
(2)关于这两种晶体的说法,正确的是____ (填序号)。
a.六方相氮化硼与石墨一样可以导电
b.立方相氮化硼只含有σ键
c.两种晶体均为分子晶体
d.六方相氮化硼晶体层内一个硼原子与相邻氮原子构成平面三角形
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为___ ,其结构与石墨相似却不导电,原因是___ 。
II.有一种氮化硼晶体的结构与金刚石相似,其晶胞如图所示。

(1)在一个晶胞中,含有硼原子___ 个,氮原子___ 个。
(2)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。已知三个原子分数坐标参数:A为(0,0,0)、B为(0,1,1)、C为(1,1,0);则E原子为___ 。
(3)氮化硼晶胞的俯视投影图是___ 。

(4)已知氮化硼晶胞为ρg•cm-3,设NA为阿伏加德罗常数的值,则氮化硼晶胞的棱长为___ cm(用代数式表示)。

(1)基态硼原子的电子排布式为
(2)关于这两种晶体的说法,正确的是
a.六方相氮化硼与石墨一样可以导电
b.立方相氮化硼只含有σ键
c.两种晶体均为分子晶体
d.六方相氮化硼晶体层内一个硼原子与相邻氮原子构成平面三角形
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为
II.有一种氮化硼晶体的结构与金刚石相似,其晶胞如图所示。

(1)在一个晶胞中,含有硼原子
(2)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。已知三个原子分数坐标参数:A为(0,0,0)、B为(0,1,1)、C为(1,1,0);则E原子为
(3)氮化硼晶胞的俯视投影图是

(4)已知氮化硼晶胞为ρg•cm-3,设NA为阿伏加德罗常数的值,则氮化硼晶胞的棱长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】氮元素在农药生产及工业、制造业等领域用途非常广泛。请根据提示回答下列问题∶
(1)N原子的最外层电子排布式为___ ,在第二周期元素中,第一电离能大于N的元素有___ 种。
(2)NH3是重要的配体,如[Cu(NH3)4]2+,NH3分子的VSEPR模型为____ ,其中H—N—H的键角为107.3°,则[Cu(NH3)4]2+中H—N—H的键角___ 107.3°(填“大于”“小于”“等于”)。
(3)甲基胺离子(CH3NH )的电子式为
)的电子式为_____ ,其中存在的共价键类型为____ (填极性键、非极性键、配位键)。已知(CH3)2NH比NH3接收质子的能力强,可能的原因是____ 。
(4)2-甲基吡啶(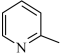 )是类似于苯的芳香化合物,分子中N原子的杂化类型为
)是类似于苯的芳香化合物,分子中N原子的杂化类型为___ 。1mol该物质中含有的σ键数目为____ 。
(5)已知氨在一定条件下可形成一种立方晶系,其立方晶胞沿x、y或z轴投影图均如图所示

①晶胞的棱长为apm,则该晶体的密度为___ g/cm3(写出数学表达式,设NA为阿伏加德罗常数的值)。
②请画出该立方晶胞沿体对角线方向的投影图___ 。
(1)N原子的最外层电子排布式为
(2)NH3是重要的配体,如[Cu(NH3)4]2+,NH3分子的VSEPR模型为
(3)甲基胺离子(CH3NH
 )的电子式为
)的电子式为(4)2-甲基吡啶(
 )是类似于苯的芳香化合物,分子中N原子的杂化类型为
)是类似于苯的芳香化合物,分子中N原子的杂化类型为(5)已知氨在一定条件下可形成一种立方晶系,其立方晶胞沿x、y或z轴投影图均如图所示

①晶胞的棱长为apm,则该晶体的密度为
②请画出该立方晶胞沿体对角线方向的投影图
您最近一年使用:0次



