工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
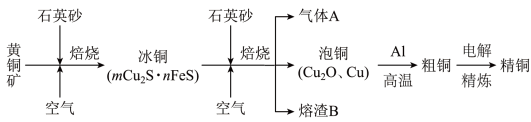
(1)气体A中的大气污染物可选用下列试剂中的_______ 吸收.
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在__________ (填离子符号),检验溶液中还存在Fe2+的方法是_____________________________ (注明试剂、现象).
(3)由泡铜冶炼粗铜的化学反应方程式为________________________ .
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是_________ .
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为______________________ .

(1)气体A中的大气污染物可选用下列试剂中的
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
(3)由泡铜冶炼粗铜的化学反应方程式为
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
2014·北京东城·一模 查看更多[7]
(已下线)第5讲 金属材料与金属的冶炼(已下线)第10讲 金属材料及金属矿物的开发利用(精练)-2022年高考化学一轮复习讲练测新疆乌鲁木齐县柴窝堡林场中学2019届高三四月调研考试理综化学试题2017届山东省德州市陵城一中高三12月月考化学试卷2012年普通高等学校招生全国统一考试化学(山东卷)(已下线)2014高考名师推荐化学实验专题(已下线)2014届北京市东城区高三第二学期质量调研理综化学试卷
更新时间:2016-12-09 06:02:35
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】碘化亚铜(CuI)是阳极射线管覆盖物,不溶于水和乙醇。下图是工业上由冰铜制取无水碘化亚铜的流程。

(1)步骤a中Cu2S被转化为Cu,同时有大气污染物A生成,相关反应的化学方程式为___________ ,熔渣B主要成分为黑色磁性物质,其化学式为___________ 。
(2)步骤b中H2O2的作用是___________ ;步骤c中加入过量NaI涉及的主要反应的离子方程式为___________ 。
(3)步骤d用乙醇洗涤的优点是______ ;检验沉淀是否洗涤干净的方法是_________ 。

(1)步骤a中Cu2S被转化为Cu,同时有大气污染物A生成,相关反应的化学方程式为
(2)步骤b中H2O2的作用是
(3)步骤d用乙醇洗涤的优点是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】人类的生产、生活离不开化学。
(1)铝粉与某些金属氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应,如:2Al+Fe2O3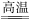 2Fe+Al2O3,反应发生时放出大量的热。
2Fe+Al2O3,反应发生时放出大量的热。
①“铝热反应”属于四种基本反应类型中的___ 反应。
②信息中的“某些”指___ (填“比铝活泼”“比铝不活泼”或“任意”)。
③试写出铝粉与MnO2发生的铝热反应方程式:___ 。
(2)从海水中提取溴的工业流程如图:
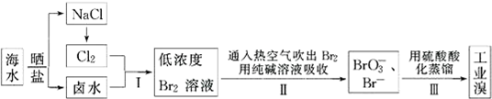
①步骤I中发生反应的离子方程式为___ 。
②步骤II用热空气吹出的Br2被纯碱溶液吸收时,则被氧化和被还原的Br2的物质的量之比为___ 。
(3)海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①若操作I用H2O2溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程为___ 。
②操作II的名称为___ 、___ ,此过程中可以选用的有机溶剂是___ (填一种)。
(1)铝粉与某些金属氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应,如:2Al+Fe2O3
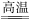 2Fe+Al2O3,反应发生时放出大量的热。
2Fe+Al2O3,反应发生时放出大量的热。①“铝热反应”属于四种基本反应类型中的
②信息中的“某些”指
③试写出铝粉与MnO2发生的铝热反应方程式:
(2)从海水中提取溴的工业流程如图:

①步骤I中发生反应的离子方程式为
②步骤II用热空气吹出的Br2被纯碱溶液吸收时,则被氧化和被还原的Br2的物质的量之比为
(3)海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①若操作I用H2O2溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程为
②操作II的名称为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】H2SiF6(氟硅酸)是一种基本化工原料,广泛用于制取氟硅酸盐及氟化物等。以氟硅酸和碳酸锂等为原料生产电池级LiF的工艺流程如图:
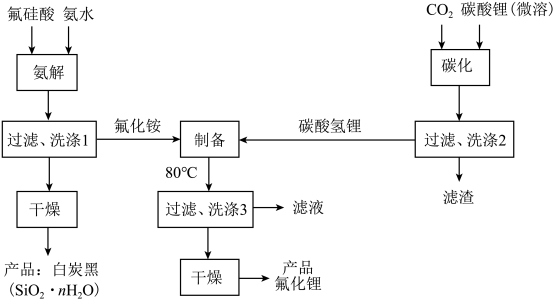
回答下列问题:
(1)生产中采用内衬为聚四氟乙烯或石墨的反应器。聚四氟乙烯的结构简式为____ ;不用陶瓷设备的原因是____ 。
(2)“氨解”时发生反应的化学方程式为____ ,氟化铵的电子式为____ 。
(3)“碳化”时发生反应的离子方程式为____ 。
(4)“制备”时产生的气体经分别吸收后返回____ 和___ 工序循环使用。
(5)H2SiF6水溶液中存在平衡:SiF62-(aq)+4H2O(1)═Si(OH)4(aq)+4H+(aq)+6F-(aq),该反应的平衡常数表达式为___ 。
(6)某工厂用纯度为85%的氟硅酸14.4吨和纯度为90%的碳酸锂7.4吨来制备氟化锂,已知流程中氟元素的损耗率为10%,锂元素的损耗率为8%,则最终产品氟化锂为____ 吨(精确到0.1)。

回答下列问题:
(1)生产中采用内衬为聚四氟乙烯或石墨的反应器。聚四氟乙烯的结构简式为
(2)“氨解”时发生反应的化学方程式为
(3)“碳化”时发生反应的离子方程式为
(4)“制备”时产生的气体经分别吸收后返回
(5)H2SiF6水溶液中存在平衡:SiF62-(aq)+4H2O(1)═Si(OH)4(aq)+4H+(aq)+6F-(aq),该反应的平衡常数表达式为
(6)某工厂用纯度为85%的氟硅酸14.4吨和纯度为90%的碳酸锂7.4吨来制备氟化锂,已知流程中氟元素的损耗率为10%,锂元素的损耗率为8%,则最终产品氟化锂为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应中常常伴随着能量的变化。
(1)下列变化中属于吸热过程的化学变化的是___________ (填字母)
①液态水汽化
②盐酸与碳酸氢钠的反应
③氢氧化钡与氯化铵的反应
④氯酸钾分解制氧气
⑤生石灰与水反应生成熟石灰
⑥干冰升华
(2)断开 键、
键、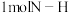 键、
键、 键分别需要吸收的能量为
键分别需要吸收的能量为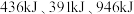 ,合成氨工业中生成
,合成氨工业中生成 时理论上能
时理论上能___________ (填“吸收”或“放出”)能量___________  。
。
(3)以 为燃料可设计成结构简单、能量转化率高、对环境无污染的酸性燃料电池,其工作原理如图甲所示,电池的总反应为:CH4+2O2=CO2+2H2O。则通入b气体的电极为
为燃料可设计成结构简单、能量转化率高、对环境无污染的酸性燃料电池,其工作原理如图甲所示,电池的总反应为:CH4+2O2=CO2+2H2O。则通入b气体的电极为___________ (填“正极”或“负极”),通入a气体的电极反应式为___________ 。(质子交换膜只允许 通过)
通过)
(1)下列变化中属于吸热过程的化学变化的是
①液态水汽化
②盐酸与碳酸氢钠的反应
③氢氧化钡与氯化铵的反应
④氯酸钾分解制氧气
⑤生石灰与水反应生成熟石灰
⑥干冰升华
(2)断开
 键、
键、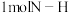 键、
键、 键分别需要吸收的能量为
键分别需要吸收的能量为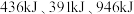 ,合成氨工业中生成
,合成氨工业中生成 时理论上能
时理论上能 。
。(3)以
 为燃料可设计成结构简单、能量转化率高、对环境无污染的酸性燃料电池,其工作原理如图甲所示,电池的总反应为:CH4+2O2=CO2+2H2O。则通入b气体的电极为
为燃料可设计成结构简单、能量转化率高、对环境无污染的酸性燃料电池,其工作原理如图甲所示,电池的总反应为:CH4+2O2=CO2+2H2O。则通入b气体的电极为 通过)
通过)
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素。已知A、C及B、E分别是同主族元素,且B、E两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍。处于同周期的C、D、E元素中,D是该周期金属元素中金属性最弱的元素。
(1)试比较C、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)______ >_______ ;
(2) A、B、C形成的化合物的晶体类型为__________ ;电子式为__________ ;
(3)写出D单质与C元素最高价氧化物对应水化物反应的离子方程式___________ ;
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式_________________________ ;
(5)A单质和B单质能构成电池,该电池用多孔惰性电极浸入浓KOH溶液,两极分别通入A单质和B单质,写出该电池负极电极反应方程式_______________ ;
(6)通常条件下,C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6kJ,试写出表示该热量变化的离子方程式__________ 。
(1)试比较C、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)
(2) A、B、C形成的化合物的晶体类型为
(3)写出D单质与C元素最高价氧化物对应水化物反应的离子方程式
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式
(5)A单质和B单质能构成电池,该电池用多孔惰性电极浸入浓KOH溶液,两极分别通入A单质和B单质,写出该电池负极电极反应方程式
(6)通常条件下,C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6kJ,试写出表示该热量变化的离子方程式
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】I.二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g)⇌CH3OH(g) ∆H1=-90.7 kJ·mol-1
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H2=-23.5 kJ·mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g) ∆H3=-41.2kJ·mol-1
回答下列问题:
(1)则反应3H2(g)+3CO(g)⇌CH3OCH3(g)+CO2(g)的∆H=_______ kJ·mol-1。
(2)二甲醚燃料电池的工作原理如图所示:
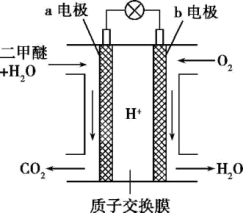
该电池负极的电极反应式为_______ 。
II .某研究小组用NaOH溶液吸收二氧化硫后,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。
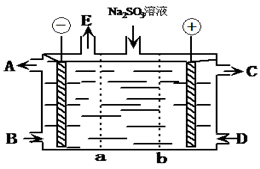
①a表示_______ (填“阴”或“阳”)膜。A-E分别代表原料或产品,其中C为稀硫酸,E为氢气,则A为_______ 溶液(填写化学式)。
②阳极电极反应式为_______ 。
III. 次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍-磷合金。化学镀镍的溶液中含有Ni2+和H2PO ,在酸性条件下发生以下镀镍反应:
,在酸性条件下发生以下镀镍反应:
Ni2++_______H2PO +_______=_______Ni+_______H2PO
+_______=_______Ni+_______H2PO +_______
+_______
①请配平上述方程式________ 。
②反应中,若生成1mol H2PO ,反应中转移电子的数目为
,反应中转移电子的数目为_______ 。
①CO(g)+2H2(g)⇌CH3OH(g) ∆H1=-90.7 kJ·mol-1
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H2=-23.5 kJ·mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g) ∆H3=-41.2kJ·mol-1
回答下列问题:
(1)则反应3H2(g)+3CO(g)⇌CH3OCH3(g)+CO2(g)的∆H=
(2)二甲醚燃料电池的工作原理如图所示:

该电池负极的电极反应式为
II .某研究小组用NaOH溶液吸收二氧化硫后,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。

①a表示
②阳极电极反应式为
III. 次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍-磷合金。化学镀镍的溶液中含有Ni2+和H2PO
 ,在酸性条件下发生以下镀镍反应:
,在酸性条件下发生以下镀镍反应:Ni2++_______H2PO
 +_______=_______Ni+_______H2PO
+_______=_______Ni+_______H2PO +_______
+_______①请配平上述方程式
②反应中,若生成1mol H2PO
 ,反应中转移电子的数目为
,反应中转移电子的数目为
您最近半年使用:0次
【推荐1】铜在自然界存在于多种矿石中.
(Ⅰ)以硅孔雀石(主要成分为CuSiO3•2H2O,含少量SiO2、FeCO3、Fe2O3等杂质)为原料制取硫酸铜的工艺流程如下:

已知:Fe3+、Cu2+和Fe2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、6.7和9.7.
(1)“溶浸”中CuSiO3•2H2O和H2SO4发生反应的化学方程式___________ .
(2)“溶浸”中,选取浓度为20% H2SO4为浸出剂,铜的浸出率与浸出时间的关系见图1.由图1可得,随着浸出时间的增长,_____________ (至少写一条变化规律).
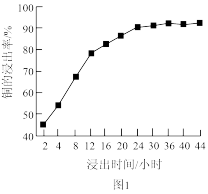
(3)“除杂”中,加入MnO2的作用是___________ (用离子方程式表示).“除杂”中需在搅拌下加入石灰乳以调节溶液的pH到3~4,沉淀部分杂质离子,分离得滤液.滤渣的主要成分为________ .
(Ⅱ)以黄铜矿(主要成分为CuFeS2)为原料炼制精铜的工艺流程如下:
黄铜矿 精铜冰铜(Cu2S和FeS)
精铜冰铜(Cu2S和FeS) 粗铜
粗铜 精铜
精铜
(4)“还原”工艺中其中一个反应为:Cu2S+2Cu2O 6Cu+SO2↑,该反应的氧化剂是
6Cu+SO2↑,该反应的氧化剂是___ .
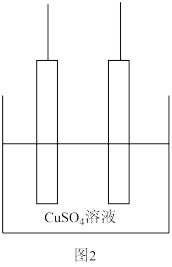
(5)粗铜含少量Fe、Ag、Au等金属杂质,电解精炼铜时,阴极反应式为________ .完成图2中由粗铜电解得到精铜的示意图,并作相应标注._______
(Ⅰ)以硅孔雀石(主要成分为CuSiO3•2H2O,含少量SiO2、FeCO3、Fe2O3等杂质)为原料制取硫酸铜的工艺流程如下:

已知:Fe3+、Cu2+和Fe2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、6.7和9.7.
(1)“溶浸”中CuSiO3•2H2O和H2SO4发生反应的化学方程式
(2)“溶浸”中,选取浓度为20% H2SO4为浸出剂,铜的浸出率与浸出时间的关系见图1.由图1可得,随着浸出时间的增长,

(3)“除杂”中,加入MnO2的作用是
(Ⅱ)以黄铜矿(主要成分为CuFeS2)为原料炼制精铜的工艺流程如下:
黄铜矿
 精铜冰铜(Cu2S和FeS)
精铜冰铜(Cu2S和FeS) 粗铜
粗铜 精铜
精铜(4)“还原”工艺中其中一个反应为:Cu2S+2Cu2O
 6Cu+SO2↑,该反应的氧化剂是
6Cu+SO2↑,该反应的氧化剂是(5)粗铜含少量Fe、Ag、Au等金属杂质,电解精炼铜时,阴极反应式为

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】电解精炼铜,可以降低铜中杂质含量,提高铜的性能,同时也可以回收其中的贵金属。
(1)电解时,阴极反应方程式为____ 。
(2)工业上从电解铜的阳极泥中提取贵金属的流程的工艺流程如图:

已知:温度和硫酸浓度对阳极泥中各组分浸出率的影响,如表所示:
①步骤I的主要目的为浸出铜,分析表格数据,可知步骤I最适合的条件为____ 。
②步骤II中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为____ 。
③步骤III的操作方法为_____ 、过滤。
④步骤IV中,反应温度为75℃,此过程中H2O2溶液的添加量高于理论值,原因为___ 。
⑤步骤VII中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为____ 。
⑥步骤VIII中得到的Au和Ag混合物最好用____ 进行分离(填选项字母)。
A.稀硝酸 B.浓盐酸 C.稀盐酸 D.浓氢氧化钠溶液 E.王水
(1)电解时,阴极反应方程式为
(2)工业上从电解铜的阳极泥中提取贵金属的流程的工艺流程如图:

已知:温度和硫酸浓度对阳极泥中各组分浸出率的影响,如表所示:
| 固定浸出温度 | 固定H2SO4浓度 | |||||||||||
| H2SO4浓度/mol·L-1 | 浸出率1% | 浸出温度/℃ | 浸出率/% | |||||||||
| Cu | Ag | Au | Se | Te | Cu | Ag | Au | Se | Te | |||
| 4 | 95.1 | 4.67 | <0.2 | 0.83 | 8.93 | 30 | 87.1 | 4.58 | <0.2 | 0.18 | 6.83 | |
| 3 | 94.5 | 4.65 | <0.2 | 0.28 | 3.90 | 40 | 94.5 | 4.65 | <0.2 | 0.28 | 6.90 | |
| 2 | 78.1 | 2.65 | <0.2 | 0.05 | 2.85 | 50 | 96.1 | 4.90 | <0.2 | 0.64 | 8.73 | |
②步骤II中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为
③步骤III的操作方法为
④步骤IV中,反应温度为75℃,此过程中H2O2溶液的添加量高于理论值,原因为
⑤步骤VII中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为
⑥步骤VIII中得到的Au和Ag混合物最好用
A.稀硝酸 B.浓盐酸 C.稀盐酸 D.浓氢氧化钠溶液 E.王水
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】如图所示,U形管内盛有100mL的溶液,按要求回答问题。
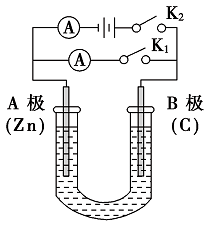
(1)打开K2,合并K1,若所盛溶液为CuSO4溶液:则A为_______ 极,A极的电极反应式为_______ 。若所盛溶液为KCl溶液:则B极的电极反应式为_______ ,K+移向_______ 极(填A、B)
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可观察到的现象是_______ 。
②B电极的电极反应式为_______ ,
③U形管内总反应化学方程式是_______ ;
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则:
A电极的材料应换成是_______ ,电极反应式是_______ 。B电极的材料应换成是_______ ,反应一段时间后电解质溶液中Cu2+浓度_______ (填“增大”、“减小”、“不变”)。

(1)打开K2,合并K1,若所盛溶液为CuSO4溶液:则A为
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可观察到的现象是
②B电极的电极反应式为
③U形管内总反应化学方程式是
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则:
A电极的材料应换成是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
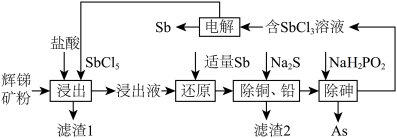
【推荐1】锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为Sb2S3,还含有PbS、As2S3、CuO、SiO2等)为原料制备金属锑的工艺流程如图所示:
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有___________ (填化学式)。
(2)“浸出”时,Sb2S3发生反应的化学方程式为_________________ 。
(3)“还原”时,被Sb还原的物质为_____________ (填化学式)。
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于______ ;所加Na2S也不宜过多,其原因为_____________ 。
(5)“除砷”时有H3PO3生成,该反应的离子方程式为________________ 。
(6)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为_______ 。
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有
(2)“浸出”时,Sb2S3发生反应的化学方程式为
(3)“还原”时,被Sb还原的物质为
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于
(5)“除砷”时有H3PO3生成,该反应的离子方程式为
(6)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
【推荐2】Ⅰ.化学实验室制取氯化氢气体的方法之一是将浓硫酸滴入浓盐酸中。请从下图中挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体的装置简图,并在图中标明所用试剂。(仪器可重复使用,固定装置不必画出)。
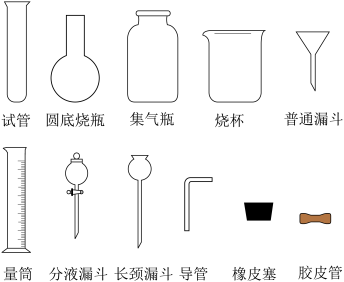

________________________________________________
Ⅱ.实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%-30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡。将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置、冷却一段时间后收集产品。
(1)写出该实验制备硫酸亚铁的化学方程式:________________________ 。
(2)硫酸溶液过稀会导致___________________________ 。
(3)采用水浴加热的原因是________________________ 。
(4)反应时铁屑过量的目的是(用离子方程式表示)___________________ 。
(5)溶液趁热过滤的原因是_______________________________ 。塞紧试管口的目的是_________________________________________ 。
(6)静置冷却一段时间后,在试管中观察到的现象是____________________ 。


Ⅱ.实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%-30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡。将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置、冷却一段时间后收集产品。
(1)写出该实验制备硫酸亚铁的化学方程式:
(2)硫酸溶液过稀会导致
(3)采用水浴加热的原因是
(4)反应时铁屑过量的目的是(用离子方程式表示)
(5)溶液趁热过滤的原因是
(6)静置冷却一段时间后,在试管中观察到的现象是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】亚硝酸钠(NaNO2)可用作建筑钢材的缓蚀剂;也可用作食品添加剂,抑制微生物,保持肉制品的结构和营养价值,但是过量摄入会导致中毒。
I.某工厂以浓HNO3、SO2、Na2CO3溶液等为原料生产NaNO2,其流程如图:

(1)在“分解塔”中,按一定比通入SO2和喷入浓HNO3,产生NO和NO2。操作时将SO2从塔底通入,浓HNO3从塔顶向下喷淋,这种加料操作的目的是___ 。
(2)“分解塔”中的温度不宜过高,其主要原因是___ 。
(3)“吸收塔”中主要发生NO、NO2与Na2CO3溶液反应生成NaNO2。写出NO、NO2按物质的量之比1:1与Na2CO3反应生成NaNO2的化学方程式:___ 。
II.某化学研究小组在实验室用稀HNO3、Cu、Na2O2为原料制备NaNO2,实验装置如图(夹持装置已省略)。
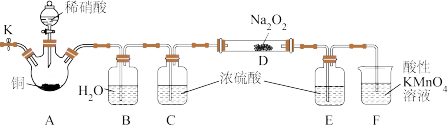
已知:①2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3
②酸性条件下,NO、NO2或NO 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+
和Mn2+
(4)实验开始加入稀HNO3前,需要先打开止水夹K,向装置中通入一段时间N2,目的是___ 。
(5)装置A中发生反应的离子方程式为___ 。
(6)装置C、E不可省去,否则会导致产品中混有___ 杂质(填化学式)。
III.NaNO2含量测定
工业亚硝酸钠产品中往往混有少量NaNO3等杂质,可以采用KMnO4测定含量。称取5.000g该亚硝酸钠产品溶于水配制成250mL的样品溶液。取25.00mL该样品溶液于锥形瓶中,用稀H2SO4酸化后,再向锥形瓶中滴加0.1000mol·L-1KMnO4溶液,至恰好完全反应时,消耗28.00mLKMnO4溶液。
(7)请写出该反应的离子方程式___ 。
(8)计算该产品中NaNO2的质量分数___ 。(写出计算过程)
I.某工厂以浓HNO3、SO2、Na2CO3溶液等为原料生产NaNO2,其流程如图:

(1)在“分解塔”中,按一定比通入SO2和喷入浓HNO3,产生NO和NO2。操作时将SO2从塔底通入,浓HNO3从塔顶向下喷淋,这种加料操作的目的是
(2)“分解塔”中的温度不宜过高,其主要原因是
(3)“吸收塔”中主要发生NO、NO2与Na2CO3溶液反应生成NaNO2。写出NO、NO2按物质的量之比1:1与Na2CO3反应生成NaNO2的化学方程式:
II.某化学研究小组在实验室用稀HNO3、Cu、Na2O2为原料制备NaNO2,实验装置如图(夹持装置已省略)。

已知:①2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3
②酸性条件下,NO、NO2或NO
 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+
和Mn2+(4)实验开始加入稀HNO3前,需要先打开止水夹K,向装置中通入一段时间N2,目的是
(5)装置A中发生反应的离子方程式为
(6)装置C、E不可省去,否则会导致产品中混有
III.NaNO2含量测定
工业亚硝酸钠产品中往往混有少量NaNO3等杂质,可以采用KMnO4测定含量。称取5.000g该亚硝酸钠产品溶于水配制成250mL的样品溶液。取25.00mL该样品溶液于锥形瓶中,用稀H2SO4酸化后,再向锥形瓶中滴加0.1000mol·L-1KMnO4溶液,至恰好完全反应时,消耗28.00mLKMnO4溶液。
(7)请写出该反应的离子方程式
(8)计算该产品中NaNO2的质量分数
您最近半年使用:0次



