天然气开采过程中产生大量的含硫废水(硫元素的主要存在形式为 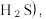 需要回收处理并加以利用,有关反应如下:
需要回收处理并加以利用,有关反应如下:
ⅰ.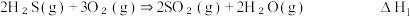
ⅱ.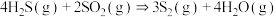 △H₂
△H₂
ⅲ.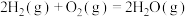
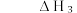
回答下列问题:
(1)H₂S热分解反应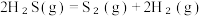 的
的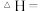
___________ (用含 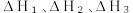 的式子表示);若起始加1molH₂气体在刚性容器中发生该分解反应,下列说法
的式子表示);若起始加1molH₂气体在刚性容器中发生该分解反应,下列说法不能 说明该反应已达平衡的是___________ (填序号)
A.H₂S 与S₂ 的物质的量之比保持2:1不变
B.容器中混合气体平均摩尔质量保持不变
C.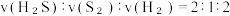 保持不变
保持不变
D.容器中混合气体的颜色保持不变
(2)总压恒定为 100kPa,向密闭容器中充入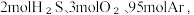 发生反应i和反应ii,反应过程中
发生反应i和反应ii,反应过程中 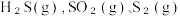 )等含硫物质的分布分数δ随时间变化如图所示。
)等含硫物质的分布分数δ随时间变化如图所示。
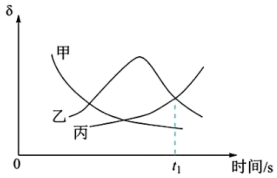
①表示 分布分数的曲线为
分布分数的曲线为___________ (填“甲”“乙”或“丙”)。
②t₁时测得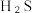 转化率为α,此时体系中
转化率为α,此时体系中 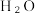 的物质的量为
的物质的量为___________ mol;用 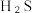 分压表示的平均反应速率为
分压表示的平均反应速率为___________ (用含α、t₁的式子表示,列出计算式即可) 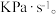
(3)也可采用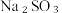 氧化法对
氧化法对 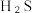 进行处理,过程中发生反应的方程式(均未配平)为:
进行处理,过程中发生反应的方程式(均未配平)为:
ⅰ.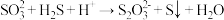
ⅱ.
ⅲ.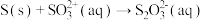
实验测得,在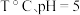 时,
时, 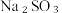 的投加量对平衡体系中部分微粒浓度的影响如图所示。
的投加量对平衡体系中部分微粒浓度的影响如图所示。
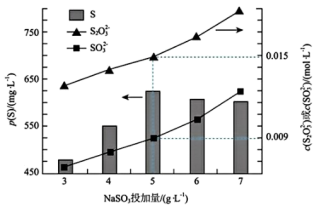
①T℃时,反应iii的平衡常数 K=___________ 。
②结合三个反应分析,当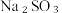 投加量高于
投加量高于 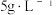 时,单位体积内 S 的质量减小的原因为:
时,单位体积内 S 的质量减小的原因为:___________ 。
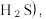 需要回收处理并加以利用,有关反应如下:
需要回收处理并加以利用,有关反应如下:ⅰ.
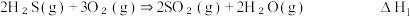
ⅱ.
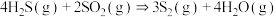 △H₂
△H₂ⅲ.
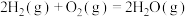
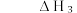
回答下列问题:
(1)H₂S热分解反应
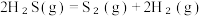 的
的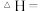
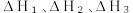 的式子表示);若起始加1molH₂气体在刚性容器中发生该分解反应,下列说法
的式子表示);若起始加1molH₂气体在刚性容器中发生该分解反应,下列说法A.H₂S 与S₂ 的物质的量之比保持2:1不变
B.容器中混合气体平均摩尔质量保持不变
C.
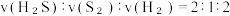 保持不变
保持不变 D.容器中混合气体的颜色保持不变
(2)总压恒定为 100kPa,向密闭容器中充入
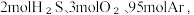 发生反应i和反应ii,反应过程中
发生反应i和反应ii,反应过程中 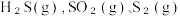 )等含硫物质的分布分数δ随时间变化如图所示。
)等含硫物质的分布分数δ随时间变化如图所示。
①表示
 分布分数的曲线为
分布分数的曲线为②t₁时测得
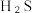 转化率为α,此时体系中
转化率为α,此时体系中 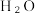 的物质的量为
的物质的量为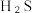 分压表示的平均反应速率为
分压表示的平均反应速率为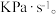
(3)也可采用
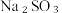 氧化法对
氧化法对 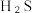 进行处理,过程中发生反应的方程式(均未配平)为:
进行处理,过程中发生反应的方程式(均未配平)为:ⅰ.
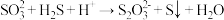
ⅱ.

ⅲ.
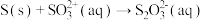
实验测得,在
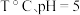 时,
时, 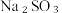 的投加量对平衡体系中部分微粒浓度的影响如图所示。
的投加量对平衡体系中部分微粒浓度的影响如图所示。
①T℃时,反应iii的平衡常数 K=
②结合三个反应分析,当
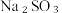 投加量高于
投加量高于 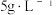 时,单位体积内 S 的质量减小的原因为:
时,单位体积内 S 的质量减小的原因为:
更新时间:2024-01-08 17:44:27
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】可逆反应2SO2(g)+O2(g) 2SO3(g)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
2SO3(g)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
(1)使用 V2O5催化该反应时,涉及到催化剂 V2O5的热化学反应有:
①V2O5(s)+SO2(g) V2 O4(s)+SO3(g) △H1=+59.6kJ·mol-1
V2 O4(s)+SO3(g) △H1=+59.6kJ·mol-1
②2V2O4(s)+O2(g) 2V2O5(s) △H2=-314.4kJ·mol-1
2V2O5(s) △H2=-314.4kJ·mol-1
则2SO2(g)+O2(g) 2SO3(g) △H3=
2SO3(g) △H3=_____ ,若降低温度,该反应速率会_____ (填“增大”或“减小”)
(2)向 10 L 密闭容器中加入 V2O4(s)、SO2(g)各 1 mol 及一定量的 O2,改变加入 O2的量,在常温下反应一段时间后,测得容器中 V2O4、V2O5、SO2和 SO3的量随反应前加入 O2的变化如图甲所示,图中没有 生成 SO3的可能原因是____________________________________________________ 。
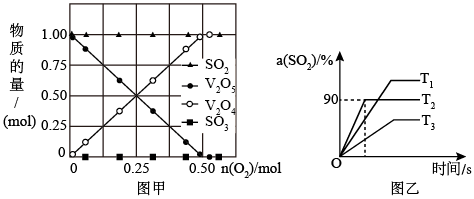
(3)向 10 L 密闭容器中加入 V2O5(s)、SO2(g)各 0.6mol,O2(g)0.3mol,保持恒压的条件下 分别在 T1、T2、T3三种温度下进行反应,测得容器中 SO2的转化率如图乙所示。
①T1_____ T2(填“>”或“<”)。
②T2时,2SO2(g)+O2(g) 2SO3(g)的平衡常数K=
2SO3(g)的平衡常数K=_____ 。若向该容器通入高温 He(g)(不参加反应,高于T2),SO3的产率将______ 选填“增大”“减小”“不变”“无法确定”),理由是_____ 。
③结合化学方程式及相关文字,解释反应为什么在 T3条件下比 T2条件下的速率慢:__________ 。
(4)T2时使用 V2O5进行反应:2SO2(g)+O2(g) 2SO3(g),在保证 O2(g)的浓度不变的条件下,增大容器的体积,平衡
2SO3(g),在保证 O2(g)的浓度不变的条件下,增大容器的体积,平衡_____ (填字母代号)。
A.向正反应方向移动 B.不移动 C.向逆反应方向移动 D.无法确定
 2SO3(g)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
2SO3(g)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。(1)使用 V2O5催化该反应时,涉及到催化剂 V2O5的热化学反应有:
①V2O5(s)+SO2(g)
 V2 O4(s)+SO3(g) △H1=+59.6kJ·mol-1
V2 O4(s)+SO3(g) △H1=+59.6kJ·mol-1②2V2O4(s)+O2(g)
 2V2O5(s) △H2=-314.4kJ·mol-1
2V2O5(s) △H2=-314.4kJ·mol-1则2SO2(g)+O2(g)
 2SO3(g) △H3=
2SO3(g) △H3=(2)向 10 L 密闭容器中加入 V2O4(s)、SO2(g)各 1 mol 及一定量的 O2,改变加入 O2的量,在常温下反应一段时间后,测得容器中 V2O4、V2O5、SO2和 SO3的量随反应前加入 O2的变化如图甲所示,图中没有 生成 SO3的可能原因是

(3)向 10 L 密闭容器中加入 V2O5(s)、SO2(g)各 0.6mol,O2(g)0.3mol,保持恒压的条件下 分别在 T1、T2、T3三种温度下进行反应,测得容器中 SO2的转化率如图乙所示。
①T1
②T2时,2SO2(g)+O2(g)
 2SO3(g)的平衡常数K=
2SO3(g)的平衡常数K=③结合化学方程式及相关文字,解释反应为什么在 T3条件下比 T2条件下的速率慢:
(4)T2时使用 V2O5进行反应:2SO2(g)+O2(g)
 2SO3(g),在保证 O2(g)的浓度不变的条件下,增大容器的体积,平衡
2SO3(g),在保证 O2(g)的浓度不变的条件下,增大容器的体积,平衡A.向正反应方向移动 B.不移动 C.向逆反应方向移动 D.无法确定
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】控制、治理氮氧化物对大气的污染是改善大气质量的重要方法。回答下列与雾霾治理有关的问题:
Ⅰ.(1)在催化剂作用下,甲烷可还原氮氧化物,从而达到治理氮氧化物污染的目的。已知:①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1;②4NO2(g)+2N2(g)= 8NO(g) ΔH=+586 kJ·mol-1。则CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) ΔH=________ kJ·mol-1。
(2)工业烟气中的氮氧化物可用NH3催化还原,反应原理如图所示。
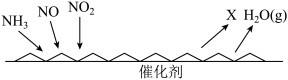
其中X为一种无毒的气体,则NH3催化还原氮氧化物的化学方程式为______ 。
(3)用NH3催化还原烟气中的氮氧化物时,当 =x,用Fe作催化剂时,在NH3充足的条件下,不同x值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图所示,当x=
=x,用Fe作催化剂时,在NH3充足的条件下,不同x值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图所示,当x=_____ 时,脱氮效果最佳,最佳的脱氮温度是____ ℃。

Ⅱ.(4)甲醇是一种绿色燃料,甲醇的工业合成方法较多,如CO(g)+2H2(g) CH3OH(g)。在2 L恒容密闭容器中充入1 mol CO和2 mol H2混合原料气,充分反应达到平衡,测得平衡时混合物中CH3OH的体积分数与压强、温度的关系如图所示。
CH3OH(g)。在2 L恒容密闭容器中充入1 mol CO和2 mol H2混合原料气,充分反应达到平衡,测得平衡时混合物中CH3OH的体积分数与压强、温度的关系如图所示。
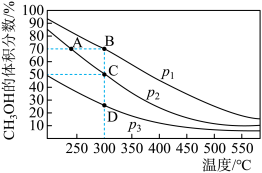
①图中压强p1、p2、p3的大小关系是_______ 。
②C点平衡常数K=___ ,A、B、D三点的平衡常数K(分别用KA、KB、KD表示)的大小关系是_____ 。
Ⅰ.(1)在催化剂作用下,甲烷可还原氮氧化物,从而达到治理氮氧化物污染的目的。已知:①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1;②4NO2(g)+2N2(g)= 8NO(g) ΔH=+586 kJ·mol-1。则CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) ΔH=
(2)工业烟气中的氮氧化物可用NH3催化还原,反应原理如图所示。

其中X为一种无毒的气体,则NH3催化还原氮氧化物的化学方程式为
(3)用NH3催化还原烟气中的氮氧化物时,当
 =x,用Fe作催化剂时,在NH3充足的条件下,不同x值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图所示,当x=
=x,用Fe作催化剂时,在NH3充足的条件下,不同x值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图所示,当x=
Ⅱ.(4)甲醇是一种绿色燃料,甲醇的工业合成方法较多,如CO(g)+2H2(g)
 CH3OH(g)。在2 L恒容密闭容器中充入1 mol CO和2 mol H2混合原料气,充分反应达到平衡,测得平衡时混合物中CH3OH的体积分数与压强、温度的关系如图所示。
CH3OH(g)。在2 L恒容密闭容器中充入1 mol CO和2 mol H2混合原料气,充分反应达到平衡,测得平衡时混合物中CH3OH的体积分数与压强、温度的关系如图所示。
①图中压强p1、p2、p3的大小关系是
②C点平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】清洁能源的综合利用可有效降低碳排放,是实现“碳中和、碳达峰”的重要途径。
(1)一种借助光将 转化为
转化为 的催化机理如图所示。
的催化机理如图所示。
 转化为
转化为 过程总反应的热化学方程式是
过程总反应的热化学方程式是________ ;该反应在________ (填“高温”、“低温”或“任意温度”)下能自发进行。
(2)采用真空封管法制备磷化硼纳米颗粒,成功实现了高选择性电催化还原 制备甲醇(
制备甲醇( ),该反应历程如图所示。
),该反应历程如图所示。________ 。
②上述合成甲醇的反应速率较慢,要使反应速率加快,需要降低某步骤的能量变化,写出该基元反应的化学方程式________ 。
(3)工业中, 和
和 在催化剂作用下可发生两个平行反应,分别生成CO和
在催化剂作用下可发生两个平行反应,分别生成CO和 。
。
反应a:
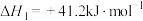
反应b:
在传统的催化固定反应床(CFBR)中, 转化率和甲醇选择性通常都比较低,科学团队研制了一种具有反应和分离双功能的分子筛膜催化反应器(CMR),极大地改善了该问题,原理如图所示
转化率和甲醇选择性通常都比较低,科学团队研制了一种具有反应和分离双功能的分子筛膜催化反应器(CMR),极大地改善了该问题,原理如图所示 投入一定量
投入一定量 和
和 ,不同反应模式下
,不同反应模式下 的平衡转化率和甲醇选择性的相关实验数据如下表所示。已知:
的平衡转化率和甲醇选择性的相关实验数据如下表所示。已知: 选择性
选择性
①在CMR模式下,上述条件下发生反应,下列不能说明反应b达到平衡状态的标志是________ (填标号)。
A.气体压强不再变化 B.气体平均相对分子质量不再变化
C.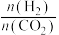 不再变化 D.混合气体的密度不再变化
不再变化 D.混合气体的密度不再变化
②由表中数据可知CMR模式下, 的转化率明显提高,结合具体反应分析可能的原因
的转化率明显提高,结合具体反应分析可能的原因________ 。
③压力平衡常数 是指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压
是指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压 的物质的量分数。根据表中数据计算CFBR模式下,温度为230℃时,反应b的
的物质的量分数。根据表中数据计算CFBR模式下,温度为230℃时,反应b的 值为
值为________ (写数值表达式,无需计算结果)。
(1)一种借助光将
 转化为
转化为 的催化机理如图所示。
的催化机理如图所示。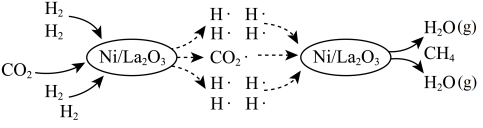
 转化为
转化为 过程总反应的热化学方程式是
过程总反应的热化学方程式是(2)采用真空封管法制备磷化硼纳米颗粒,成功实现了高选择性电催化还原
 制备甲醇(
制备甲醇( ),该反应历程如图所示。
),该反应历程如图所示。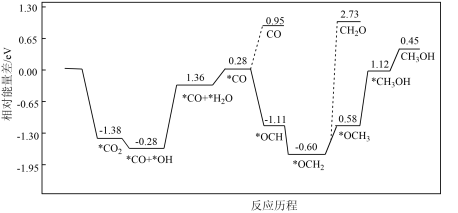
②上述合成甲醇的反应速率较慢,要使反应速率加快,需要降低某步骤的能量变化,写出该基元反应的化学方程式
(3)工业中,
 和
和 在催化剂作用下可发生两个平行反应,分别生成CO和
在催化剂作用下可发生两个平行反应,分别生成CO和 。
。反应a:

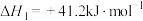
反应b:

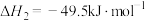
在传统的催化固定反应床(CFBR)中,
 转化率和甲醇选择性通常都比较低,科学团队研制了一种具有反应和分离双功能的分子筛膜催化反应器(CMR),极大地改善了该问题,原理如图所示
转化率和甲醇选择性通常都比较低,科学团队研制了一种具有反应和分离双功能的分子筛膜催化反应器(CMR),极大地改善了该问题,原理如图所示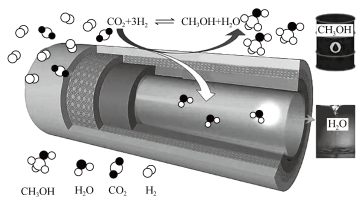
 投入一定量
投入一定量 和
和 ,不同反应模式下
,不同反应模式下 的平衡转化率和甲醇选择性的相关实验数据如下表所示。已知:
的平衡转化率和甲醇选择性的相关实验数据如下表所示。已知: 选择性
选择性
实验组 | 反应模式 |
| 压强/MPa | 温度/℃ |
|
|
① | CFBR | 3 | 5 | 250 | 25.6 | 61.3 |
② | CFBR | 3 | 5 | 230 | 20.0 | 70.0 |
③ | CMR | 3 | 5 | 260 | 36.1 | 100 |
A.气体压强不再变化 B.气体平均相对分子质量不再变化
C.
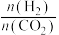 不再变化 D.混合气体的密度不再变化
不再变化 D.混合气体的密度不再变化②由表中数据可知CMR模式下,
 的转化率明显提高,结合具体反应分析可能的原因
的转化率明显提高,结合具体反应分析可能的原因③压力平衡常数
 是指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压
是指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压 的物质的量分数。根据表中数据计算CFBR模式下,温度为230℃时,反应b的
的物质的量分数。根据表中数据计算CFBR模式下,温度为230℃时,反应b的 值为
值为
您最近一年使用:0次
【推荐1】研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应Ⅰ:CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g) ∆H1=-49.6 kJ/mol
反应Ⅱ:CH3OCH3(g)+H2O(g) ⇌2CH3OH(g) ∆H2=+23.4 kJ/mol
反应Ⅲ:2CO2(g)+6H2(g) ⇌CH3OCH3(g)+3H2O(g) ∆H3
(1)∆H3=_______ kJ/mol
(2)恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,发生反应I。下列描述能说明反应I达到平衡状态的是_______ (填序号)
A.反应体系总压强保持不变
B.容器内的混合气体的密度保持不变
C.水分子中断裂2NA个H-O键,同时氢分子中断裂3NA个H-H键
D.CH3OH和H2O的浓度之比保持不变
(3)反应II在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到某时刻测得各组分浓度如表:
当反应达到平衡状态时,混合气体中CH3OH体积分数(CH3OH)% =_______ %
(4)在某压强下,反应III在不同温度、不同投料比时,CO2的平衡转化率如图所示。T1温度下,将6mol CO2和12mol H2充入2 L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3)=_______ ;KA、KB、KC三者之间的大小关系为_______

(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应I和反应III,在相同的时间段内CH3OH的选择性和产率随温度的变化如图。其中:CH3OH的选择性=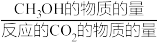 ×100%
×100%
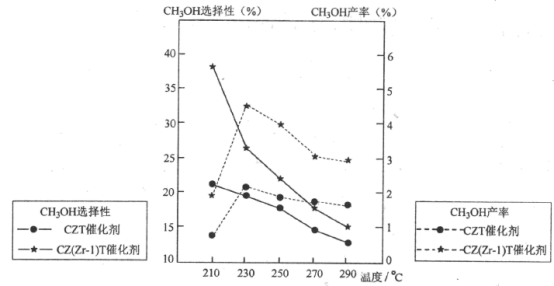
①温度高于230℃,CH3OH产率随温度升高而下降的原因是_______
②在上述条件下合成甲醇的工业条件是_______
A.210℃ B.230℃ C.催化剂CZT D.催化剂CZ(Zr-1)T
反应Ⅰ:CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g) ∆H1=-49.6 kJ/mol
反应Ⅱ:CH3OCH3(g)+H2O(g) ⇌2CH3OH(g) ∆H2=+23.4 kJ/mol
反应Ⅲ:2CO2(g)+6H2(g) ⇌CH3OCH3(g)+3H2O(g) ∆H3
(1)∆H3=
(2)恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,发生反应I。下列描述能说明反应I达到平衡状态的是
A.反应体系总压强保持不变
B.容器内的混合气体的密度保持不变
C.水分子中断裂2NA个H-O键,同时氢分子中断裂3NA个H-H键
D.CH3OH和H2O的浓度之比保持不变
(3)反应II在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到某时刻测得各组分浓度如表:
| 物质 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
| 浓度/mol·L-1 | 1.8 | 1.8 | 0.4 |
(4)在某压强下,反应III在不同温度、不同投料比时,CO2的平衡转化率如图所示。T1温度下,将6mol CO2和12mol H2充入2 L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3)=

(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应I和反应III,在相同的时间段内CH3OH的选择性和产率随温度的变化如图。其中:CH3OH的选择性=
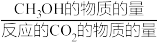 ×100%
×100%
①温度高于230℃,CH3OH产率随温度升高而下降的原因是
②在上述条件下合成甲醇的工业条件是
A.210℃ B.230℃ C.催化剂CZT D.催化剂CZ(Zr-1)T
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】近日,科学家开发钢基掺杂锌催化剂[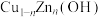 ]提高乙炔加氢制备乙烯的活性。
]提高乙炔加氢制备乙烯的活性。
反应1: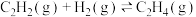
 ;
;
反应2: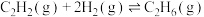
 。
。
回答下列问题:
(1)已知:①
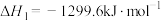 ;
;
②
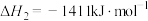 ;
;
③
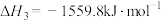 ;
;
④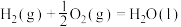
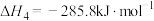 ;
;
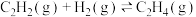

___________  。化学上,曾用“热值”表示单位质量可燃物完全燃烧时政出热量的多少,下列四种可燃物中,热值最大的是
。化学上,曾用“热值”表示单位质量可燃物完全燃烧时政出热量的多少,下列四种可燃物中,热值最大的是___________ (填字母,下同)。
A. B.
B. C.
C. D.
D.
(2)在恒容密闭容器中发生反应1: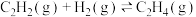
 。仅改变下列一个条件,能提高反应速率的是___________。
。仅改变下列一个条件,能提高反应速率的是___________。
(3)向恒温、恒容反应容器中充入 和
和 ,同时发生反应1和反应2.下列情况能表明化学反应一定达到平衡状态的是___________。
,同时发生反应1和反应2.下列情况能表明化学反应一定达到平衡状态的是___________。
(4)100℃下,在2L恒容反应器中充入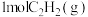 和
和 制备
制备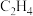 ,实验测得单位时间内乙炔的转化率、乙烷的选择性[乙烷的选择性
,实验测得单位时间内乙炔的转化率、乙烷的选择性[乙烷的选择性 ,即乙烷的物质的量与乙炔转化量之比]与
,即乙烷的物质的量与乙炔转化量之比]与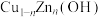 中n值关系如图1所示,
中n值关系如图1所示,
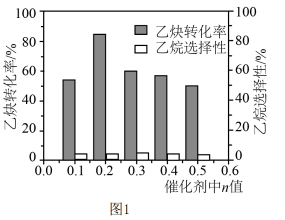
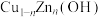 中n最佳值为
中n最佳值为___________ 。若在10min内乙炔转化率为80%,乙烷选择性为4%,则生成乙烯的反应速率为___________  。
。
(5)一定条件下,向密闭容器中充入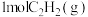 和
和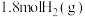 仅发生反应1,图2表示压强为0.1MPa和5.0MPa下
仅发生反应1,图2表示压强为0.1MPa和5.0MPa下 的平衡转化率随温度的变化关系。
的平衡转化率随温度的变化关系。
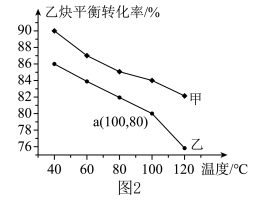
已知:相同温度下,压强增大,乙炔的平衡转化率增大。
①甲曲线代表的压强为___________ 。乙曲线a点对应的 平衡转化率为
平衡转化率为___________ %(保留3位有效数字)。
②根据图像可知,压强相同,随着温度升高,乙炔的平衡转化率___________ (填“增大”“减小”或“不变”)。
(6)乙烷—空气碱性燃料电池的能量转化率较高。下列叙述正确的是___________。
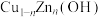 ]提高乙炔加氢制备乙烯的活性。
]提高乙炔加氢制备乙烯的活性。反应1:
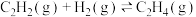
 ;
;反应2:
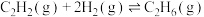
 。
。回答下列问题:
(1)已知:①

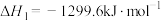 ;
;②

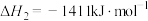 ;
;③

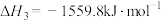 ;
;④
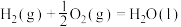
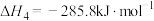 ;
;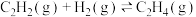

 。化学上,曾用“热值”表示单位质量可燃物完全燃烧时政出热量的多少,下列四种可燃物中,热值最大的是
。化学上,曾用“热值”表示单位质量可燃物完全燃烧时政出热量的多少,下列四种可燃物中,热值最大的是A.
 B.
B. C.
C. D.
D.
(2)在恒容密闭容器中发生反应1:
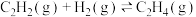
 。仅改变下列一个条件,能提高反应速率的是___________。
。仅改变下列一个条件,能提高反应速率的是___________。| A.加入高效催化剂 | B.增大氯气浓度 | C.降低反应温度 | D.充入惰性气体 |
 和
和 ,同时发生反应1和反应2.下列情况能表明化学反应一定达到平衡状态的是___________。
,同时发生反应1和反应2.下列情况能表明化学反应一定达到平衡状态的是___________。| A.容器内气体密度不随时间变化 | B.容器内气体总压强不随时间变化 |
| C.含碳分子的总浓度不随时间变化 | D.容器内 |
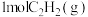 和
和 制备
制备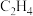 ,实验测得单位时间内乙炔的转化率、乙烷的选择性[乙烷的选择性
,实验测得单位时间内乙炔的转化率、乙烷的选择性[乙烷的选择性 ,即乙烷的物质的量与乙炔转化量之比]与
,即乙烷的物质的量与乙炔转化量之比]与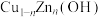 中n值关系如图1所示,
中n值关系如图1所示,
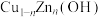 中n最佳值为
中n最佳值为 。
。(5)一定条件下,向密闭容器中充入
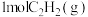 和
和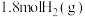 仅发生反应1,图2表示压强为0.1MPa和5.0MPa下
仅发生反应1,图2表示压强为0.1MPa和5.0MPa下 的平衡转化率随温度的变化关系。
的平衡转化率随温度的变化关系。
已知:相同温度下,压强增大,乙炔的平衡转化率增大。
①甲曲线代表的压强为
 平衡转化率为
平衡转化率为②根据图像可知,压强相同,随着温度升高,乙炔的平衡转化率
(6)乙烷—空气碱性燃料电池的能量转化率较高。下列叙述正确的是___________。
| A.在正极上充入乙烷,负极上发生氧化反应 |
B.电池放电时, 向负极迁移 向负极迁移 |
C.负极反应式为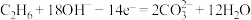 |
| D.正极消耗11.2L(标准状况)气体时转移1mol电子 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】氮的氢化物和氧化物是氮元素的两类重要化合物,与人们的日常生活和生产关系密切。请回答下列问题:
(1)肼(N2H4)是一种氮的氢化物,作为火箭燃料是其主要用途。
①写出肼的电子式:___________ 。
②已知反应:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH1=-1048.9kJ·mol-1 (i)
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2kJ·mol-1 (ii)
则N2(g)+2O2(g)=N2O4(l) ΔH=___________ 。
(2)工业合成氨为农业的丰收奠定了基础。为探究工业合成氨反应原理,进行下列实验:温度为T1时,将20.4gNH3和11.2gN2通入到容积为1.0L的恒容密闭容器中,0.5h达到平衡时,H2体积分数为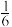 。化学反应速率v(H2)=
。化学反应速率v(H2)=___________ mol·L-1·h-1,NH3分解率=___________ 。
(3)氮的氧化物很多,且多数不稳定,最稳定的氮氧化物是NO2.在恒容密闭容器中投入一定量的N2O4,发生反应:N2O4(g)⇌2NO2(g) △H,N2O4的平衡转化率[a(N2O4)]随温度(T1、……T4逐渐升高)的变化关系如下图:
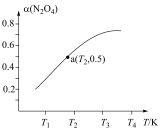
N2O4(g)转化为NO2(g)的△H___________ 0(填“>”或“<”)。若容器中通入N2O4的起始压强102kPa,则a点温度下的平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,P分=P总×物质的量分数)。
(4)在汽车消音器管道中安装三元催化转化器,可发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g)。在某1.0L恒容密闭容器中各通入1.0mol的CO和NO,发生上述反应,经10min达到平衡状态,容器内压强变为原来的
2CO2(g)+N2(g)。在某1.0L恒容密闭容器中各通入1.0mol的CO和NO,发生上述反应,经10min达到平衡状态,容器内压强变为原来的 。
。
①下列能判断该反应达到平衡状态的是___________ (填序号)。
a.容器中,v正(CO)=v逆(NO) b.容器中的气体颜色不再变化
c.容器中气体的密度不再变化 d.容器内总分子数不再变化
②反应达到平衡后,仅将NO、CO2两种气体的浓度均增加1倍,则平衡___________ (填“向右移动”“向左移动”或“不移动”)。
(1)肼(N2H4)是一种氮的氢化物,作为火箭燃料是其主要用途。
①写出肼的电子式:
②已知反应:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH1=-1048.9kJ·mol-1 (i)
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2kJ·mol-1 (ii)
则N2(g)+2O2(g)=N2O4(l) ΔH=
(2)工业合成氨为农业的丰收奠定了基础。为探究工业合成氨反应原理,进行下列实验:温度为T1时,将20.4gNH3和11.2gN2通入到容积为1.0L的恒容密闭容器中,0.5h达到平衡时,H2体积分数为
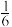 。化学反应速率v(H2)=
。化学反应速率v(H2)=(3)氮的氧化物很多,且多数不稳定,最稳定的氮氧化物是NO2.在恒容密闭容器中投入一定量的N2O4,发生反应:N2O4(g)⇌2NO2(g) △H,N2O4的平衡转化率[a(N2O4)]随温度(T1、……T4逐渐升高)的变化关系如下图:

N2O4(g)转化为NO2(g)的△H
(4)在汽车消音器管道中安装三元催化转化器,可发生反应:2NO(g)+2CO(g)
 2CO2(g)+N2(g)。在某1.0L恒容密闭容器中各通入1.0mol的CO和NO,发生上述反应,经10min达到平衡状态,容器内压强变为原来的
2CO2(g)+N2(g)。在某1.0L恒容密闭容器中各通入1.0mol的CO和NO,发生上述反应,经10min达到平衡状态,容器内压强变为原来的 。
。①下列能判断该反应达到平衡状态的是
a.容器中,v正(CO)=v逆(NO) b.容器中的气体颜色不再变化
c.容器中气体的密度不再变化 d.容器内总分子数不再变化
②反应达到平衡后,仅将NO、CO2两种气体的浓度均增加1倍,则平衡
您最近一年使用:0次



