资源的高效利用对保护环境、促进经济持续健康发展具有重要作用,如回收利用电解精炼铜的阳极泥中含有的银、铂、金等贵重金属。提炼阳极泥的方法有多种,湿法提炼是其中重要的一种,其主要生产流程如下:
(1)各步生产流程中都涉及了同一种分离方法,该方法需要的玻璃仪器有玻璃棒和___________ 。
(2)脱铜渣A中含有AgCl,它溶于浓氨水的离子方程式为___________ 。
(3)已知N2H4 被银氨溶液氧化的产物是氮气,则每生成1 mol Ag,需要消耗___________ g N2H4。
(4)固体B中单质Au在酸性环境下与NaClO3、NaCl反应生成NaAuCl4,在NaAuCl4中Au元素的化合价为___________ ,该反应的离子方程式为___________ 。
(5)阳极泥中的铜可以用FeCl3 溶液浸出,所得溶液主要含有的阳离子为Cu2+、Fe3+和Fe2+;结合下图分析:(其中的纵坐标代表金属阳离子浓度的对数)___________ (用离子方程式表示),然后加入适量的CuO调节pH=3.7,除去___________ (离子);
②根据图中数据计算可得Cu(OH)2的Ksp约为___________ 。
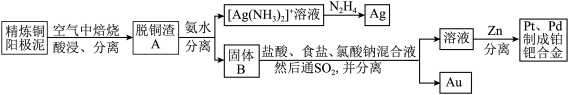
(1)各步生产流程中都涉及了同一种分离方法,该方法需要的玻璃仪器有玻璃棒和
(2)脱铜渣A中含有AgCl,它溶于浓氨水的离子方程式为
(3)已知N2H4 被银氨溶液氧化的产物是氮气,则每生成1 mol Ag,需要消耗
(4)固体B中单质Au在酸性环境下与NaClO3、NaCl反应生成NaAuCl4,在NaAuCl4中Au元素的化合价为
(5)阳极泥中的铜可以用FeCl3 溶液浸出,所得溶液主要含有的阳离子为Cu2+、Fe3+和Fe2+;结合下图分析:(其中的纵坐标代表金属阳离子浓度的对数)
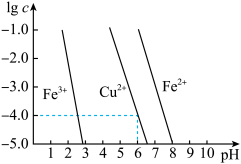
②根据图中数据计算可得Cu(OH)2的Ksp约为
23-24高三上·四川内江·阶段练习 查看更多[2]
更新时间:2024-01-10 16:20:39
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:

已知NaHCO3在低温下溶解度较小。
(1)反应Ⅰ的化学方程式为_______ 。
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中 Na2CO3的含量。
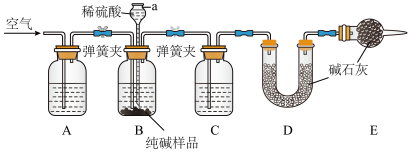
(2)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若_______ ,说明装置不漏气。
(3)装置A中的试剂为_______ ,装置C中的试剂为_______ 。装置E的作用是_______ 。
(4)实验前称取28.80 g样品,实验后测得D装置增重8.80 g,则样品中Na2CO3的质量分数为_______ (保留一位小数);若缺少E装置,会使测定结果_______ (填“偏高”或“偏低”)。

已知NaHCO3在低温下溶解度较小。
(1)反应Ⅰ的化学方程式为
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中 Na2CO3的含量。

(2)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若
(3)装置A中的试剂为
(4)实验前称取28.80 g样品,实验后测得D装置增重8.80 g,则样品中Na2CO3的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铝箔可以有效减少热辐射,因此常用于食品的保温。铝土矿(主要成分为 ,还含有
,还含有 、
、 )是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
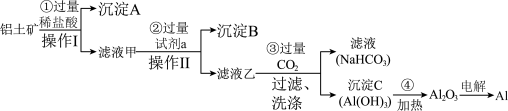
(1)步骤②中试剂a为___________ 。
(2)步骤③中通入过量 ,产生沉淀C的离子反应方程式为
,产生沉淀C的离子反应方程式为___________ 。
(3)在生活中常利用铝热反应来进行焊接钢轨。除了 ,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________。
,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________。
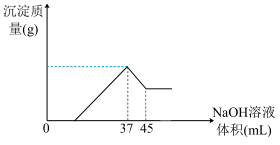
(4)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后向滤液中加入 的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中
的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中 的百分含量为
的百分含量为___________ 。
 ,还含有
,还含有 、
、 )是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
(1)步骤②中试剂a为
(2)步骤③中通入过量
 ,产生沉淀C的离子反应方程式为
,产生沉淀C的离子反应方程式为(3)在生活中常利用铝热反应来进行焊接钢轨。除了
 ,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________。
,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________。| A.MgO | B. | C. | D. |
(4)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后向滤液中加入
 的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中
的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中 的百分含量为
的百分含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】物质的量是高中化学中常用的物理量,请回答下列问题:
(1)某硫酸钠溶液中含有3.01×1023个Na+,则溶液中SO42-的物质的量是_____ mol。
(2)在标准状况下,4.48 L HCl气体溶于水配成500 mL溶液,其物质的量浓度为_____________ 。
(3)在标准状况下,1.7 g氨气所占的体积约为_________ L,与_____ mol H2S含有相同的氢原子数。
(4)7.8 g Na2X中含Na+ 0.2 mol,则X的摩尔质量是_____________________ 。
(5)实验室需要0.3 mol•L-1硫酸溶液480 mL。
①配制过程用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管、试剂瓶外,还需要______________ 。
②需量取质量分数为98%、密度为1.84 g•cm-3的浓硫酸的体积为______ mL。
③配制过程中需先在烧杯中将浓硫酸进行稀释,操作方法是:_______________ 。
(1)某硫酸钠溶液中含有3.01×1023个Na+,则溶液中SO42-的物质的量是
(2)在标准状况下,4.48 L HCl气体溶于水配成500 mL溶液,其物质的量浓度为
(3)在标准状况下,1.7 g氨气所占的体积约为
(4)7.8 g Na2X中含Na+ 0.2 mol,则X的摩尔质量是
(5)实验室需要0.3 mol•L-1硫酸溶液480 mL。
①配制过程用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管、试剂瓶外,还需要
②需量取质量分数为98%、密度为1.84 g•cm-3的浓硫酸的体积为
③配制过程中需先在烧杯中将浓硫酸进行稀释,操作方法是:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】已知元素X位于Y的下一周期,X、Y的原子序数均不大于20.某含氧酸盐甲的化学式 为XYO3。请回答:
(1)常温下X的单质能与水发生反应,395℃时,甲能发生分解反应生成两种盐,一种是 含Y元素的无氧酸盐,则X位于周期表_____ ,甲发生分解反应的化学方程式是_____ 。
(2) 若甲难溶于水,且甲与盐酸反应生成能使品红溶液褪色的气体.
①则甲为_____ (填化学式)该气体能使酸性高锰酸钾溶液褪色, 该反应的离子方程式为_____ ;
②X、Y形成简单离子半径大小关系为 > (用离子符号表示)._________
③25℃时,甲在水中的沉淀溶解平衡曲线如右图所示,若要使溶液 X2+离子沉淀完全,则 YO32-离子的最小浓度为_____ mol·L-1。
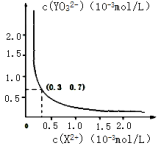
(当离子浓度小于 1×10-5mol·L-1 时,该离子沉淀完全)
(3)若甲能与盐酸反应,生成无色、无味的气体乙.则:
①乙的电子式为_____ ;
②甲在水中持续加热生成一种更难溶的物质并逸出气体乙,该反应的化学方程式为___ 。
(1)常温下X的单质能与水发生反应,395℃时,甲能发生分解反应生成两种盐,一种是 含Y元素的无氧酸盐,则X位于周期表
(2) 若甲难溶于水,且甲与盐酸反应生成能使品红溶液褪色的气体.
①则甲为
②X、Y形成简单离子半径大小关系为 > (用离子符号表示).
③25℃时,甲在水中的沉淀溶解平衡曲线如右图所示,若要使溶液 X2+离子沉淀完全,则 YO32-离子的最小浓度为

(当离子浓度小于 1×10-5mol·L-1 时,该离子沉淀完全)
(3)若甲能与盐酸反应,生成无色、无味的气体乙.则:
①乙的电子式为
②甲在水中持续加热生成一种更难溶的物质并逸出气体乙,该反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】活性自由基HO 可有效除去废水中的苯酚等有机污染物。
可有效除去废水中的苯酚等有机污染物。
(1)H2O2在Fe3O4催化剂表面产生HO 除去废水中的苯酚的原理如图-1所示。
除去废水中的苯酚的原理如图-1所示。
①酸性条件下,该催化过程中产生HO 的反应的离子方程式为
的反应的离子方程式为___________ 。
②在不同初始pH条件下,研究苯酚的去除率随时间的变化,结果表明:在反应开始时,初始pH=6的溶液中苯酚的去除率明显低于初始pH=3的溶液,但一段时间后两者接近,原因是___________ 。
(2)掺杂了Cr3+的Fe3O4催化剂催化氧化原理如图-2所示。在Fe3O4催化剂中掺杂少量Cr3+,可提高催化效率,但浓度太高,反而会降低催化效率,其原因是___________ 。
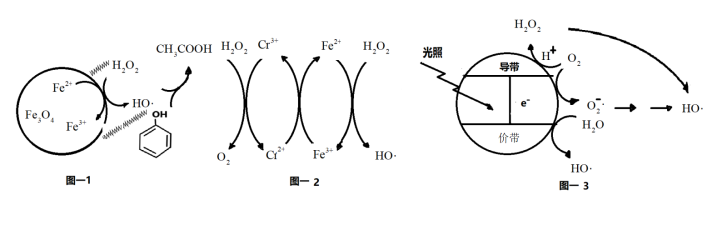
(3)光催化氧化技术也可生成HO 降解有机污染物。其原理如图-3.光照时,价带失去电子产生有强氧化性的空穴。价带上生成HO
降解有机污染物。其原理如图-3.光照时,价带失去电子产生有强氧化性的空穴。价带上生成HO 的电极反应式为
的电极反应式为___________ 。图中,HO 还有另外的产生途径,描述其产生过程:
还有另外的产生途径,描述其产生过程:___________ 。
 可有效除去废水中的苯酚等有机污染物。
可有效除去废水中的苯酚等有机污染物。(1)H2O2在Fe3O4催化剂表面产生HO
 除去废水中的苯酚的原理如图-1所示。
除去废水中的苯酚的原理如图-1所示。①酸性条件下,该催化过程中产生HO
 的反应的离子方程式为
的反应的离子方程式为②在不同初始pH条件下,研究苯酚的去除率随时间的变化,结果表明:在反应开始时,初始pH=6的溶液中苯酚的去除率明显低于初始pH=3的溶液,但一段时间后两者接近,原因是
(2)掺杂了Cr3+的Fe3O4催化剂催化氧化原理如图-2所示。在Fe3O4催化剂中掺杂少量Cr3+,可提高催化效率,但浓度太高,反而会降低催化效率,其原因是

(3)光催化氧化技术也可生成HO
 降解有机污染物。其原理如图-3.光照时,价带失去电子产生有强氧化性的空穴。价带上生成HO
降解有机污染物。其原理如图-3.光照时,价带失去电子产生有强氧化性的空穴。价带上生成HO 的电极反应式为
的电极反应式为 还有另外的产生途径,描述其产生过程:
还有另外的产生途径,描述其产生过程:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为测定某草酸晶体( ,
,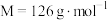 )产品的纯度,称取14.000g产品溶于水,配制成500mL溶液,每次所取待测液体积均为25.00mL,用
)产品的纯度,称取14.000g产品溶于水,配制成500mL溶液,每次所取待测液体积均为25.00mL,用 的酸性溶液(浓度为0.1000mol/L)进行滴定,实验结果记录如下表。(杂质不与高锰酸钾反应)
的酸性溶液(浓度为0.1000mol/L)进行滴定,实验结果记录如下表。(杂质不与高锰酸钾反应)
已知反应:
(1)滴定终点的现象是___________ 。
(2)通过实验数据,计算该产品的纯度为___________ (用百分数表示,写出计算过程)。
(3)下列滴定操作会导致测定结果偏低的是___________。
 ,
,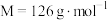 )产品的纯度,称取14.000g产品溶于水,配制成500mL溶液,每次所取待测液体积均为25.00mL,用
)产品的纯度,称取14.000g产品溶于水,配制成500mL溶液,每次所取待测液体积均为25.00mL,用 的酸性溶液(浓度为0.1000mol/L)进行滴定,实验结果记录如下表。(杂质不与高锰酸钾反应)
的酸性溶液(浓度为0.1000mol/L)进行滴定,实验结果记录如下表。(杂质不与高锰酸钾反应)| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗溶液体积/mL | 20.05 | 19.95 | 24.36 |

(1)滴定终点的现象是
(2)通过实验数据,计算该产品的纯度为
(3)下列滴定操作会导致测定结果偏低的是___________。
| A.锥形瓶用待测液润洗 |
B.装 的酸性溶液的滴定管没有润洗 的酸性溶液的滴定管没有润洗 |
| C.滴定前滴定管尖嘴处有气泡,滴定结束后气泡消失 |
D.滴定前平视装有 的酸性溶液的滴定管,滴定结束时俯视 的酸性溶液的滴定管,滴定结束时俯视 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】运用溶液中离子平衡的相关知识,解决下列问题。
(1)含酚酞的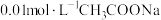 溶液显浅红色的原因为
溶液显浅红色的原因为_______ (用离子方程式)。
(2)室温下,用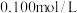 盐酸溶液滴定
盐酸溶液滴定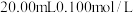 的某氨水溶液,滴定曲线如图所示。
的某氨水溶液,滴定曲线如图所示。
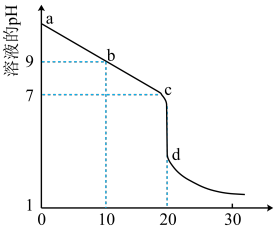
①d点所示的溶液中离子浓度由大到小的顺序依次为_______ 。
②b点所示的溶液中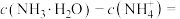
_______ (用溶液中的其它离子浓度表示)。
③ 的氨水与
的氨水与 的
的 溶液中,由水电离出的
溶液中,由水电离出的 之比为
之比为_______ 。
(3)已知 ,
, 。向含有
。向含有 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中
沉淀生成时,溶液中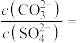
_______ (保留三位有效数字)。
我国国标推荐的食品药品中Ca元素含量的测定方法之一:利用 将处理后的样品中的
将处理后的样品中的 沉淀,过滤洗涤,然后将所得
沉淀,过滤洗涤,然后将所得 固体溶于过量的强酸,最后使用已知浓度的
固体溶于过量的强酸,最后使用已知浓度的 溶液通过滴定来测定溶液中
溶液通过滴定来测定溶液中 的含量。针对该实验中的滴定过程,回答以下问题:
的含量。针对该实验中的滴定过程,回答以下问题:
(4) 溶液应该用
溶液应该用_______ (填“酸式”或“碱式”)滴定管盛装。
(5)写出滴定过程中反应的离子方程式_______ 。
(6)滴定终点的现象:_______ 。
(7)以下哪些操作会导致测定的结果偏高_______ (填字母编号)。
a.装入 溶液前未润洗滴定管
溶液前未润洗滴定管
b.滴定结束后俯视读数
c.滴定结束后,滴定管尖端悬有一滴溶液
d.滴定过程中,振荡时将待测液洒出
(1)含酚酞的
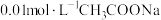 溶液显浅红色的原因为
溶液显浅红色的原因为(2)室温下,用
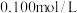 盐酸溶液滴定
盐酸溶液滴定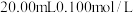 的某氨水溶液,滴定曲线如图所示。
的某氨水溶液,滴定曲线如图所示。
①d点所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中
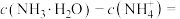
③
 的氨水与
的氨水与 的
的 溶液中,由水电离出的
溶液中,由水电离出的 之比为
之比为(3)已知
 ,
, 。向含有
。向含有 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中
沉淀生成时,溶液中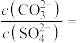
我国国标推荐的食品药品中Ca元素含量的测定方法之一:利用
 将处理后的样品中的
将处理后的样品中的 沉淀,过滤洗涤,然后将所得
沉淀,过滤洗涤,然后将所得 固体溶于过量的强酸,最后使用已知浓度的
固体溶于过量的强酸,最后使用已知浓度的 溶液通过滴定来测定溶液中
溶液通过滴定来测定溶液中 的含量。针对该实验中的滴定过程,回答以下问题:
的含量。针对该实验中的滴定过程,回答以下问题:(4)
 溶液应该用
溶液应该用(5)写出滴定过程中反应的离子方程式
(6)滴定终点的现象:
(7)以下哪些操作会导致测定的结果偏高
a.装入
 溶液前未润洗滴定管
溶液前未润洗滴定管b.滴定结束后俯视读数
c.滴定结束后,滴定管尖端悬有一滴溶液
d.滴定过程中,振荡时将待测液洒出
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上,用生物堆浸法处理低品位黄铜矿(主要成分是CuFeS2)制备两“矾",其简易流程如下:

已知:①T.f细菌在1.0<pH<6.0范围内保持生物活性。
②几种离子沉淀的pH如下表所示:
回答下列问题:
(1)生物堆浸包括两个反应过程:①CuFeS2+4H++O2=Cu2++Fe2++2S+2H2O2;②4Fe2++O2+4H+=4Fe3++2H2O,在反应①中,氧化产物是___________ 。
(2)生物堆浸效率与温度的关系如图所示:

温度高于40℃时,生物堆浸效率降低的主要原因可能是___________ 。
(3)生物堆浸过程中不断补充稀硫酸,调节pH的范围为___________ ,其目的是___________ 。
(4)“氧化”中1molCuS完全反应转移2mol电子,该反应的离了方程式为___________ 。
(5)室温下,滤液M中c(Cu2+)=1.0×10-5mol/L,c(S2-)=1.3×10-31mol/L,则Ksp(CuS)=___________ 。
(6)测定绿矾(FeSO4·7H2O)的纯度。取30g绿矾溶于稀硫酸中配制成100mL溶液。取25.00mL溶液于锥形瓶中,用0.2000mol/L标准KMnO4溶液滴定至溶液出现粉红色,且30s内不褪色。三次平行实验所消耗标准KMnO4溶液体积依次为23.56mL、24.95mL、25.05mL。
①通过计算可得该绿矾的纯度为___________ (结果保留4位有效数字)。
②用“偏高”“偏低”“无影响”,填写下列实验操作可能对实验结果造成的影响。
A.取用绿矾溶液的滴定管末用待测液润洗___________
B.开始滴定时,滴定管尖嘴处有气泡,滴定完毕气泡排出___________
C.滴定过程中振荡时有液滴溅出___________
D.滴定前读数时仰视,滴定完毕读数时俯视___________
③如果操作都正确,测得纯度高于实际纯度,其可能原因是___________ 。

已知:①T.f细菌在1.0<pH<6.0范围内保持生物活性。
②几种离子沉淀的pH如下表所示:
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀时的pH | 1.5 | 6.3 | 4.2 |
| 完全沉淀时的pH | 2.8 | 8.3 | 6.7 |
(1)生物堆浸包括两个反应过程:①CuFeS2+4H++O2=Cu2++Fe2++2S+2H2O2;②4Fe2++O2+4H+=4Fe3++2H2O,在反应①中,氧化产物是
(2)生物堆浸效率与温度的关系如图所示:

温度高于40℃时,生物堆浸效率降低的主要原因可能是
(3)生物堆浸过程中不断补充稀硫酸,调节pH的范围为
(4)“氧化”中1molCuS完全反应转移2mol电子,该反应的离了方程式为
(5)室温下,滤液M中c(Cu2+)=1.0×10-5mol/L,c(S2-)=1.3×10-31mol/L,则Ksp(CuS)=
(6)测定绿矾(FeSO4·7H2O)的纯度。取30g绿矾溶于稀硫酸中配制成100mL溶液。取25.00mL溶液于锥形瓶中,用0.2000mol/L标准KMnO4溶液滴定至溶液出现粉红色,且30s内不褪色。三次平行实验所消耗标准KMnO4溶液体积依次为23.56mL、24.95mL、25.05mL。
①通过计算可得该绿矾的纯度为
②用“偏高”“偏低”“无影响”,填写下列实验操作可能对实验结果造成的影响。
A.取用绿矾溶液的滴定管末用待测液润洗
B.开始滴定时,滴定管尖嘴处有气泡,滴定完毕气泡排出
C.滴定过程中振荡时有液滴溅出
D.滴定前读数时仰视,滴定完毕读数时俯视
③如果操作都正确,测得纯度高于实际纯度,其可能原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】高纯MnCO3在电子工业中有重要的应用,工业上利用软锰矿(主要成分是MnO2,还含有Fe2O3、CaCO3、CuO等杂质)制取碳酸锰的流程如图所示:
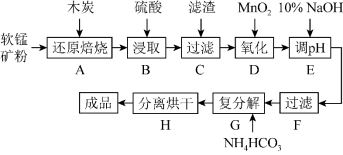
已知:还原焙烧主反应为2MnO2+C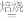 2MnO+CO2↑。
2MnO+CO2↑。
可能用到的数据如表所示:
根据要求回答下列问题:
(1)在实验室进行步骤A,用到的主要由硅酸盐产品制成的仪器有____ 。“浸取”时温度控制在90~95℃之间,并且要连续搅拌的目的是____ 。
(2)步骤C中的滤渣为____ 。
(3)步骤D发生反应的离子方程式为____ 。
(4)步骤E中调节pH的范围为____ ,其目的是___ 。
(5)步骤G中Mn2+恰好沉淀完全时测得溶液中 的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=
的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=___ 。
(6)现用滴定法测定产品中锰元素的含量。实验步骤:称取3.300g试样,向其中加入稍过量的磷酸和硝酸,加热使产品中MnCO3完全转化为[Mn(PO4)2]3-(其中 完全转化为
完全转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应 +
+  =N2↑+2H2O以除去
=N2↑+2H2O以除去 ;加入稀硫酸酸化,再加入60.00mL0.500mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2
;加入稀硫酸酸化,再加入60.00mL0.500mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2 ;用5.00mL0.500mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。
;用5.00mL0.500mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。
①写出酸性K2Cr2O7溶液与Fe2+反应的离子方程式:____ ;
②试样中锰元素的质量分数为___ 。

已知:还原焙烧主反应为2MnO2+C
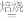 2MnO+CO2↑。
2MnO+CO2↑。可能用到的数据如表所示:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 1.5 | 6.5 | 4.2 | 8.1 |
| 沉淀完全pH | 3.7 | 9.7 | 7.4 | 10.1 |
(1)在实验室进行步骤A,用到的主要由硅酸盐产品制成的仪器有
(2)步骤C中的滤渣为
(3)步骤D发生反应的离子方程式为
(4)步骤E中调节pH的范围为
(5)步骤G中Mn2+恰好沉淀完全时测得溶液中
 的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=
的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=(6)现用滴定法测定产品中锰元素的含量。实验步骤:称取3.300g试样,向其中加入稍过量的磷酸和硝酸,加热使产品中MnCO3完全转化为[Mn(PO4)2]3-(其中
 完全转化为
完全转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应 +
+  =N2↑+2H2O以除去
=N2↑+2H2O以除去 ;加入稀硫酸酸化,再加入60.00mL0.500mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2
;加入稀硫酸酸化,再加入60.00mL0.500mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2 ;用5.00mL0.500mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。
;用5.00mL0.500mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。①写出酸性K2Cr2O7溶液与Fe2+反应的离子方程式:
②试样中锰元素的质量分数为
您最近一年使用:0次
【推荐1】硫酸铜可用作家禽养殖饲料的添加剂。一种以含砷氧化铜矿[含CuO、Cu(OH)2·CuCO3、砷的化合物及铅的化合物]为原料制备饲料级硫酸铜的工艺流程如图所示。回答下列问题:
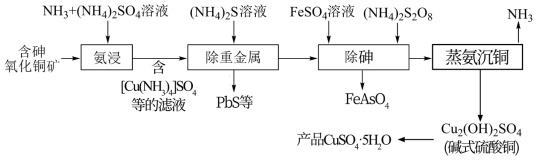
(1)“氨浸”时控制温度为45℃,液固比为1:4,c(NH3)+c(NH )=1 mol·L-1且c(NH3)=c(NH
)=1 mol·L-1且c(NH3)=c(NH )。
)。
①温度不宜超过55℃,这是因为___ 。
②“氨浸”时,Cu(OH)2·CuCO3转化为[Cu(NH3)4]SO4和NH4HCO3的化学方程式为__ 。
③溶液中Cu2+、[Cu(NH3)n]2+(n=1~4)的物质的量分数δ(x)与lgc(NH3)的关系如图所示。
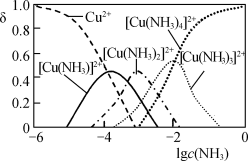
lgc(NH3)=-3时,浓度最大的含铜微粒是__ ,lgc(NH3)由-1→0时,发生反应的离子方程式为__ 。
(2)“除砷”时控制pH=9,AsO 最终转化为FeAsO4沉淀,AsO
最终转化为FeAsO4沉淀,AsO 中As的化合价为
中As的化合价为__ ,该转化过程中每生成1 mol FeAsO4,转移__ mol电子。
(3)“蒸氨沉铜”的尾气可返回__ 工序循环使用,由碱式硫酸铜制取产品硫酸铜晶体的方法:将碱式硫酸铜先溶于硫酸,再__ 、洗涤、干燥。

(1)“氨浸”时控制温度为45℃,液固比为1:4,c(NH3)+c(NH
 )=1 mol·L-1且c(NH3)=c(NH
)=1 mol·L-1且c(NH3)=c(NH )。
)。①温度不宜超过55℃,这是因为
②“氨浸”时,Cu(OH)2·CuCO3转化为[Cu(NH3)4]SO4和NH4HCO3的化学方程式为
③溶液中Cu2+、[Cu(NH3)n]2+(n=1~4)的物质的量分数δ(x)与lgc(NH3)的关系如图所示。

lgc(NH3)=-3时,浓度最大的含铜微粒是
(2)“除砷”时控制pH=9,AsO
 最终转化为FeAsO4沉淀,AsO
最终转化为FeAsO4沉淀,AsO 中As的化合价为
中As的化合价为(3)“蒸氨沉铜”的尾气可返回
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】氯化磷酸三钠[(Na3PO4·12H2O)4·NaOCl]具有良好的洗涤、去污和消毒杀菌功能。以湿法磷酸(含杂质Fe3+,Al3+及H2SiF6等)为原料制取氯化磷酸三钠的工艺流程如下:
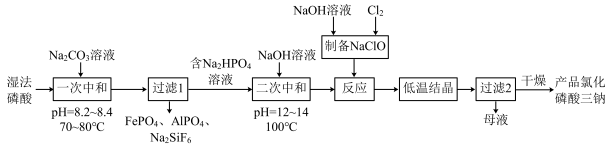
回答下列问题:
(1)“一次中和”生成Na2HPO4的化学方程式为____________________________________ ;反应需保温20min,使沉淀颗粒长大,其目的是___________________________________ 。
(2)“二次中和”不用Na2CO3溶液,其可能原因是_________________________________ 。
(3)制备NaClO的离子方程式为__________________________________________________ 。
(4)“低温结晶”时,控制温度不超过60℃的目的是________________________________ 。
(5)“过滤2”所得母液中溶质主要有_____________________________________ 和NaClO。

回答下列问题:
(1)“一次中和”生成Na2HPO4的化学方程式为
(2)“二次中和”不用Na2CO3溶液,其可能原因是
(3)制备NaClO的离子方程式为
(4)“低温结晶”时,控制温度不超过60℃的目的是
(5)“过滤2”所得母液中溶质主要有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为VO2·xH2O、Cr(OH)3及少量的SiO2。一种初步分离钒铬还原渣中钒铬并获得Na2Cr2O7的工艺流程如下:
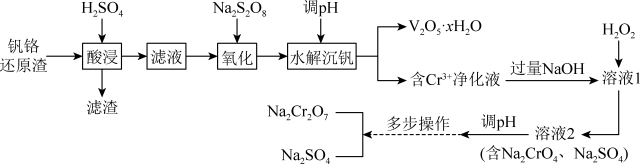
已知:①“酸浸”后VO2·xH2O转化为VO2+;
②Cr(OH)3的Ksp近似为1×10-30;
③有关物质的溶解度(g/100gH2O)如下表所示:
回答下列问题:
(1)“滤渣”的主要成分是___________ ,“氧化”生成VO ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(2)若“含Cr3+净化液”中c(Cr3+)=0.1mol/L,则“水解沉钒”调pH的范围是2.5~___________ 。
(3)“溶液1”中含CrO ,加入H2O2后发生反应的离子方程式为
,加入H2O2后发生反应的离子方程式为___________ ,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)“多步操作”包括蒸发浓缩、___________ 、冷却结晶、过滤、洗涤等步骤。
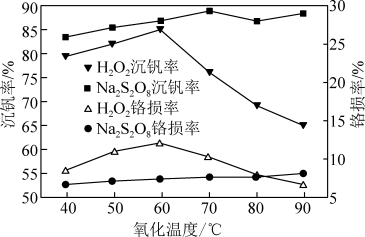
(5)研究温度对Na2S2O8与H2O2的氧化—水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在90℃左右,降低温度能耗增加。由图可知,分别采用H2O2、Na2S2O8进行“氧化”时,应选择的适宜温度是___________ 、___________ ,与Na2S2O8相比,采用H2O2氧化的主要不足之处有___________ (写出两点)。

已知:①“酸浸”后VO2·xH2O转化为VO2+;
②Cr(OH)3的Ksp近似为1×10-30;
③有关物质的溶解度(g/100gH2O)如下表所示:
| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| Na2Cr2O7 | 183.6 | 215.1 | 269.2 | 376.4 | 415.0 |
| Na2SO4 | 19.5 | 48.8 | 45.3 | 43.7 | 42.5 |
(1)“滤渣”的主要成分是
 ,发生反应的离子方程式为
,发生反应的离子方程式为(2)若“含Cr3+净化液”中c(Cr3+)=0.1mol/L,则“水解沉钒”调pH的范围是2.5~
(3)“溶液1”中含CrO
 ,加入H2O2后发生反应的离子方程式为
,加入H2O2后发生反应的离子方程式为(4)“多步操作”包括蒸发浓缩、
(5)研究温度对Na2S2O8与H2O2的氧化—水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在90℃左右,降低温度能耗增加。由图可知,分别采用H2O2、Na2S2O8进行“氧化”时,应选择的适宜温度是

您最近一年使用:0次



