将标准状况下的22.4LSO2通入含3molNaOH的溶液中,下列用来解释事实的方程式中不合理的是(已知室温下饱和Na2SO3溶液的pH约为8.3)
A.上述反应后所得溶液的pH约为12,原因是 +H2O +H2O  +OH- +OH- |
B.标准状况下的22.4LSO2通入含3molNaOH的溶液,涉及反应:2OH-+SO2= +H2O +H2O |
C.向上述反应后所得溶液中,通入氯气,pH下降:SO3+Cl2+2OH-= +2Cl-+H2O +2Cl-+H2O |
D.向上述反应后所得溶液中,滴加少量H2O2和BaCl2溶液的混合液,产生白色沉淀: +Ba2++H2O2=BaSO4↓+H2O +Ba2++H2O2=BaSO4↓+H2O |
更新时间:2024-01-17 11:38:48
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式不正确的是
A.硫酸铝溶液中加入氢氧化钡溶液:Ba2++ == BaSO4↓ == BaSO4↓ |
| B.硫酸亚铁溶液中加入过氧化氢溶液:2Fe2+ + H2O2 + 2H+ == 2Fe3+ + 2H2O |
C.向NaHCO3 溶液中加入NaOH溶液: + OH-== + OH-== + H2O + H2O |
| D.向AgCl悬浊液中加入Na2S溶液:2AgCl + S2-== Ag2S + 2Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式正确的是
| A.二氧化硅溶于氢氟酸溶液中: SiO2+4H++4F-=SiF4↑ +2H2O |
| B.偏铝酸钠溶液中通入过量的CO2:2AlO2- + CO2+3H2O=2Al(OH)3↓+ CO32- |
C.稀硫酸加入氢氧化钡溶液中:H+ + + Ba2+ + OH-=BaSO4↓+ H2O + Ba2+ + OH-=BaSO4↓+ H2O |
| D.硫酸铝溶液中加入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式书写正确的是
A.铝和过量NaOH溶液反应:Al+4OH-= +2H2O +2H2O |
B.惰性电极电解MgCl2水溶液:2Cl- +2H2O 2OH-+Cl2↑十H2↑ 2OH-+Cl2↑十H2↑ |
C.酸性高锰酸钾溶液与草酸溶液反应:5 +2 +2 +16H+ = 2Mn2++10CO2↑+8H2O +16H+ = 2Mn2++10CO2↑+8H2O |
D.水玻璃中通入过量二氧化碳: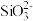 +2CO2+2H2O = H2SiO3↓+2 +2CO2+2H2O = H2SiO3↓+2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】“宏观辨识与微观探析”是化学核心素养之一。下列离子方程式错误的是
A.向盐酸中逐滴滴入过量 溶液: 溶液: |
B. 溶于NaOH溶液: 溶于NaOH溶液: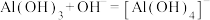 |
C.向 溶液中加入过量澄清石灰水: 溶液中加入过量澄清石灰水: |
D. 溶于稀硝酸: 溶于稀硝酸: |
您最近一年使用:0次
【推荐3】NaClO是漂白液的有效成分,某研究小组探究NaClO溶液的性质,设计了下列实验:
下列判断不正确的是
| 装置图 | 试剂X | 实验现象 | |
 | ① | 0.2mol•L-1盐酸 | 产生黄绿色气体 |
| ② | 0.2mol•L-1KI-淀粉溶液 | 溶液变蓝 | |
| ③ | 0.2mol•L-1FeSO4(H+)和KSCN混合溶液 | 溶液变红 | |
| ④ | 0.2mol•L-1AlCl3溶液 | 产生白色沉淀 | |
| A.实验①中发生的主要反应是ClO-+Cl-+2H+=Cl2↑+H2O |
| B.实验②中发生的主要反应是ClO-+2I-+2H+=Cl-+I2+H2O |
| C.实验③中该条件下氧化性强弱ClO-<Fe3+ |
| D.实验④中ClO-与Al3+相互促进水解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,下列实验方案能达到探究目的的是
| 选项 | 实验方案 | 探究目的 |
| A | 向 、 、 混合溶液中依次加入少量氯水和 混合溶液中依次加入少量氯水和 ,振荡后静置,观察 ,振荡后静置,观察 层颜色 层颜色 | 氧化性: |
| B | 向溶液 中加入盐酸,将产生的气体通入品红溶液中,观察溶液颜色变化 中加入盐酸,将产生的气体通入品红溶液中,观察溶液颜色变化 | 溶液 中是否含有 中是否含有 或 或 |
| C | 测定浓度均为 的 的 、 、 溶液的 溶液的 |  和 和 的电离能力 的电离能力 |
| D |  用饱和 用饱和 溶液浸泡一段时间后过滤、洗涤,向所得滤渣上滴加盐酸,产生无色气体 溶液浸泡一段时间后过滤、洗涤,向所得滤渣上滴加盐酸,产生无色气体 | 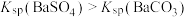 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各组溶液混合后,溶液显碱性的是( )
| A.1mL 0.1 mol·L-1NH3﹒H2 O 与 1mL 0.1 mol·L-1 HCl |
| B.1mL 0.1 mol·L-1K2S与1mL 0.1 mol·L-1K2SO4 |
| C.1mL 0.1 mol·L-1KOH 与 1mL 0.1 mol·L-1KHCO3 ,再加入1 mL 0.1 mol·L-1BaCl2 |
| D.1mL 0.1 mol·L-1NaOH 与 1mL 0.1 mol·L-1H2 SO 4 |
您最近一年使用:0次

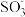 ,通过“水分子桥”,处于纳米液滴中的
,通过“水分子桥”,处于纳米液滴中的
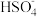
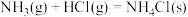 常温下能自发进行,则该反应的
常温下能自发进行,则该反应的
 的值增大
的值增大

