近日,西安建筑科技大学云斯宁教授“新能源材料”研究团队通过三元非金属掺杂缺陷工程策略,合成了一种由 B、C、N、S 四种元素组成的新型催化剂(BSN-C催化剂),该催化剂对“HER”和“IRR”过程表现出优异的电催化活性(如图所示)。下列有关说法错误的是
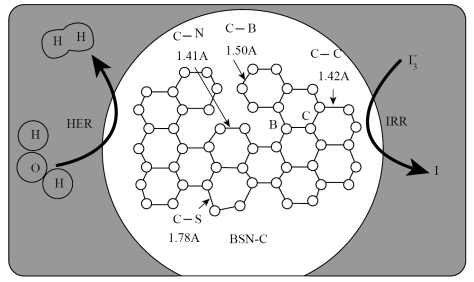

| A.该催化剂涉及的四种元素中第一电离能最大的是N |
| B.该催化剂中B原子与相邻的3个C原子构成平面结构 |
C.1mol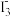 的中心原子上的价层电子对数为5NA 的中心原子上的价层电子对数为5NA |
| D.在发生“HER” 过程中生成22.4L H2时失去 1mol电子 |
更新时间:2024-01-18 08:19:30
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设阿伏加德罗常数的数值为NA,下列说法正确的是
| A.标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA |
B.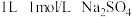 溶液中所含氧原子总数目为4NA 溶液中所含氧原子总数目为4NA |
C.标况下,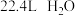 所含电子数10NA 所含电子数10NA |
D.46g的 和 和 的混合气体中共含有NA个氧原子 的混合气体中共含有NA个氧原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.1 mol CO2的体积约为22.4 L |
| B.标准状况下,2 mol CO的体积约为44.8 L |
| C.标准状况下,水的体积约为22.4 L |
| D.25℃、101KPa时,1 mol N2的体积约为22.4 L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
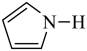
【推荐1】对于超分子聚合物和材料的组装而言,B—N配位键的动态性质和易于调节的特性起着重要作用。某种超分子的结构如图。下列叙述错误的是
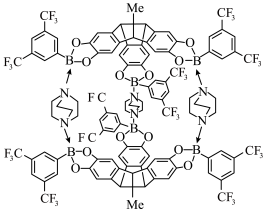
| A.该超分子中涉及的元素均为p区元素 |
| B.第一电离能:F>N>O>C>B |
| C.超分子具有分子识别和自组装的特征 |
| D.该超分子形成的B—N配位键中,N原子提供孤电子对 |
您最近一年使用:0次
【推荐2】短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外电子只有一种自旋取向,Y、Z两种原子核外s能级上的电子总数与p能级上电子总数相等,W原子的价电子中,在不同形状的原子轨道中运动的电子数之比为2:1。下列说法正确的是
| A.W的第一电离能比同周期相邻元素的小 |
| B.原子半径:r(X)<r(Y)<r(Z)<r(W) |
| C.工业上电解熔融化合物ZY制备单质Z |
| D.W的最高价氧化物不可能是非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】乙炔水化法、乙烯氧化法是工业上制备乙醛的两个重要方法,反应原理分别为: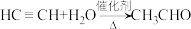 ,
,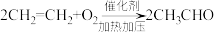 。以下叙述错误的是
。以下叙述错误的是
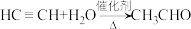 ,
,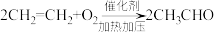 。以下叙述错误的是
。以下叙述错误的是A. 的电子式 的电子式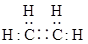 |
B.根据价层电子互斥模型,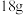 水的中心原子含有 水的中心原子含有 孤电子对 孤电子对 |
C.乙烯氧化法中,生成 乙醛时,转移的电子数约为 乙醛时,转移的电子数约为 |
D.标准状况下, 乙醛中含有 乙醛中含有 键的数目约为 键的数目约为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】乙炔水化法、乙烯氧化法是工业上制备乙醛的两个重要方法,反应原理分别为:HC≡CH+H2O CH3CHO,2H2C=CH2+O2
CH3CHO,2H2C=CH2+O2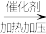 2CH3CHO。以下叙述不正确的是
2CH3CHO。以下叙述不正确的是
 CH3CHO,2H2C=CH2+O2
CH3CHO,2H2C=CH2+O2 2CH3CHO。以下叙述不正确的是
2CH3CHO。以下叙述不正确的是A.C2H4的电子式为 |
| B.根据价层电子互斥模型,18g水的中心原子含有2mol孤电子对 |
| C.乙烯氧化法中,生成0.1mol乙醛时,转移的电子数约为1.204×1024 |
| D.标准状况下,11.2LC2H2中含有π键的数目约为6.02×1023 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】大气中存在一种潜在的温室气体SF5-CF3,关于SF5-CF3的说法正确的是
| A.所有原子在同一平面内,C原子的杂化方式为sp3 |
| B.分子中有σ键无π键 |
| C.分子中所有原子均满足8电子稳定结构 |
| D.1molSF5-CF3分子中含9个共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】氯元素有多种化合价,可形成 等离子.下列说法错误的是
等离子.下列说法错误的是
 等离子.下列说法错误的是
等离子.下列说法错误的是A.基态 原子核外电子的空间运动状态有9种 原子核外电子的空间运动状态有9种 |
B.键角: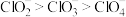 |
C. 提供孤电子对与 提供孤电子对与 可形成 可形成 |
D. 中 中 的杂化方式相同 的杂化方式相同 |
您最近一年使用:0次

 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是 含有的分子数为
含有的分子数为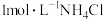 溶液中含
溶液中含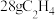 含有σ键的数目为
含有σ键的数目为
 和
和 的混合气体中质子数为
的混合气体中质子数为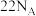
 ),分子中σ键与π键的数目之比为5:2
),分子中σ键与π键的数目之比为5:2 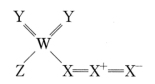


 具有强氧化性
具有强氧化性


