填空。
(1)写出基态As原子的核外电子排布式:___________ ,根据元素周期律,原子半径Ga___________ (填“大于”或“小于”,下同)As,第一电离能Ga___________ As。
(2)C、N、O的第一电离能由大到小的顺序为___________ ;H、O、S电负性由大到小的顺序是___________ 。B和N相比,电负性较大的是___________ ;BN中B元素的化合价为___________ ;从电负性角度分析,C、Si、O的非金属活泼性由强至弱的顺序为___________ 。
(3)铬基态原子的电子排布式为___________ ,氯元素的基态原子的价层电子排布式是___________ ,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有___________ (填元素符号)。
(4)基态Fe3+的M层电子排布式为___________ ,基态铝原子核外自旋平行的电子最多有___________ 个,与铝同族的第四周期元素原子的价层电子排布式为___________ ,基态磷原子的核外电子运动状态共有___________ 种,其价层电子排布式为___________ 。在硼、氧、氟、氮中第一电离能由大到小的顺序是___________ (用元素符号表示)。
(1)写出基态As原子的核外电子排布式:
(2)C、N、O的第一电离能由大到小的顺序为
(3)铬基态原子的电子排布式为
(4)基态Fe3+的M层电子排布式为
更新时间:2024-01-19 00:45:44
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:对于基态Cr原子,下列叙述正确的是_______ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列为元素周期表中前4周期的元素,根据要求回答下列各小题:
(1)写出下列微粒的核外电子排布式:
①8O_______ ;
②29Cu_______ 。
(2)写出25Mn的原子结构示意图:_______ 。
(3)写出下列微粒的核外电子排布图:
①6C_______ ;
②7N3-_______ 。
(4)26Fe 原子的核外电子中,有_______ 种运动状态不同的电子,有_______ 种能量不同的电子;Fe3+的化学性质比Fe2+稳定,其原因是_______ 。
(1)写出下列微粒的核外电子排布式:
①8O
②29Cu
(2)写出25Mn的原子结构示意图:
(3)写出下列微粒的核外电子排布图:
①6C
②7N3-
(4)26Fe 原子的核外电子中,有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】超临界状态是一种特殊的流体,用超临界CO2/CH3CN及水作电解质,使用碳作载体的铜基催化剂可高效将CO2还原为HCOOH。回答下列问题:
(1)CO2电子式为___________ 。
(2)碳元素位于元素周期表的___________ 区,基态碳原子核外电子有___________ 种空间运动状态。第二周期中基态原子与基态碳原子具有相同未成对电子数的元素是___________ (填元素符号)。
(3)基态Cu和Cu2+未成对电子数之比为___________ 。
(4)CO2和HCOOH分子中C原子的杂化形式分别为___________ 和___________ 。
(5)HCOOH通常以二聚体(含八元环)形式存在(如图),该二聚体中含有的微粒间作用力有___________ 。
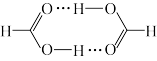
(1)CO2电子式为
(2)碳元素位于元素周期表的
(3)基态Cu和Cu2+未成对电子数之比为
(4)CO2和HCOOH分子中C原子的杂化形式分别为
(5)HCOOH通常以二聚体(含八元环)形式存在(如图),该二聚体中含有的微粒间作用力有
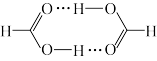
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】同族的氮、磷、砷元素的化合物在医药生产中有许多重要用途。请回答下列问题:
(1)砷的外围电子排布式是___________ ,其基态能量最低的能级电子云轮廓图为___________ 。
(2)氮、磷、砷的气态氢化物中,最不稳定的是___________ (填化学式),从结构上看其主要原因是___________ 。
(3) 与
与 可形成
可形成 ,产物中氮原子的
,产物中氮原子的 杂化轨道与硼原子的
杂化轨道与硼原子的___________ 轨道重叠成键。
(4)不同聚集状态的 ,结构不同。
,结构不同。
①固态 是一种白色晶体,经X射线研究证明,是由一种正四面体形阳离子和一种正八面体形阴离子构成,晶胞如图1所示,正八面体形离子的化学式为
是一种白色晶体,经X射线研究证明,是由一种正四面体形阳离子和一种正八面体形阴离子构成,晶胞如图1所示,正八面体形离子的化学式为___________ ;
②气态 的结构如图2所示,是
的结构如图2所示,是___________ 分子(填“极性”或“非极性”)。
(1)砷的外围电子排布式是
(2)氮、磷、砷的气态氢化物中,最不稳定的是
(3)
 与
与 可形成
可形成 ,产物中氮原子的
,产物中氮原子的 杂化轨道与硼原子的
杂化轨道与硼原子的(4)不同聚集状态的
 ,结构不同。
,结构不同。①固态
 是一种白色晶体,经X射线研究证明,是由一种正四面体形阳离子和一种正八面体形阴离子构成,晶胞如图1所示,正八面体形离子的化学式为
是一种白色晶体,经X射线研究证明,是由一种正四面体形阳离子和一种正八面体形阴离子构成,晶胞如图1所示,正八面体形离子的化学式为
②气态
 的结构如图2所示,是
的结构如图2所示,是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ti、Fe、Cr、Mn等均为过渡元素,在生产生活中起着不可替代的重要作用,对其单质和化合物的应用研究是目前科学研究的前沿之一。请回答下列问题:
(1)Cr元素的基态原子电子排布式为_____________________ ,比较Fe和 Mn的各级电离能后发现,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子______ (填“难”或“易”)。
(2)Cu元素处于周期表____________ 区,向盛有硫酸铜的试管里加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,此时的离子方程式为______________ ,若加入乙醇将析出____________ 色的晶体,其配离子的离子构型为_____________
(3)某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应(巨磁电阻效应)。用A、B、O表示这类特殊晶体的化学式:_____________ 。
(4)有一种蓝色晶体可表示为:[KxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,K+位于上述晶胞体心,且K+空缺率为50%(体心中没有K+的占总体心的百分比),其晶体中的阴离子晶胞结构如上图的图2所示,该晶体的化学式可表示为____________ 。
(1)Cr元素的基态原子电子排布式为
(2)Cu元素处于周期表
(3)某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应(巨磁电阻效应)。用A、B、O表示这类特殊晶体的化学式:

(4)有一种蓝色晶体可表示为:[KxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,K+位于上述晶胞体心,且K+空缺率为50%(体心中没有K+的占总体心的百分比),其晶体中的阴离子晶胞结构如上图的图2所示,该晶体的化学式可表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究氮原子的结构及其化合物具有重要意义
(1)氮原子的基态电子排布式为_______ 。
(2)NH3的电子式_______ 。
(3)实验室制备NH3化学方程式是_______ 。
(4)①工业合成的NH3化学方程式是_______ 。
②i.合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量
ii.氮气和氢气断裂其共价键吸收的能量如图:

请计算:1 mol N-H键断裂吸收的能量约等于_______ kJ。
(5)工业上以NH3为原料合成硝酸的路线如图,写出相关反应的化学方程式

①_______ 。②_______ 。③_______ 。
(1)氮原子的基态电子排布式为
(2)NH3的电子式
(3)实验室制备NH3化学方程式是
(4)①工业合成的NH3化学方程式是
②i.合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量
ii.氮气和氢气断裂其共价键吸收的能量如图:

请计算:1 mol N-H键断裂吸收的能量约等于
(5)工业上以NH3为原料合成硝酸的路线如图,写出相关反应的化学方程式

①
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铜及其化合物在工农业生产中有广泛的应用。
I. 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(1)向 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有_______ (填字母)。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键 E.氢键
(2) 可以与乙二胺
可以与乙二胺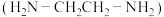 形成配离子,如图所示:
形成配离子,如图所示:
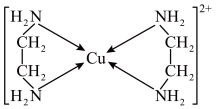
(1)C、N、O三种元素的第一电离能从大到小的顺序为_______ 。
(2)该配离子中的配体数与配位数之比为_______ 。
II.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
(3)下列物质中,属于顺磁性物质的是_______(填字母)。
III.请回答以下问题:
(4)① ②
② ③
③
将上述物质键角按由大到小的顺序排列:_______ (用序号表示)。
(5)三甲胺(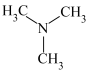 )和异丙胺(
)和异丙胺(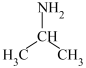 )的沸点大小关系为:三甲胺
)的沸点大小关系为:三甲胺_______ (填“>”“<”或“=”)异丙胺,原因是_______ 。
(6)基态原子的核外电子填充在5个轨道中的元素有_______ 种。
I.
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(1)向
 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有A.离子键 B.金属键 C.极性共价键 D.非极性共价键 E.氢键
(2)
 可以与乙二胺
可以与乙二胺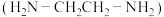 形成配离子,如图所示:
形成配离子,如图所示:
(1)C、N、O三种元素的第一电离能从大到小的顺序为
(2)该配离子中的配体数与配位数之比为
II.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
(3)下列物质中,属于顺磁性物质的是_______(填字母)。
A. | B. | C. | D. |
III.请回答以下问题:
(4)①
 ②
② ③
③
将上述物质键角按由大到小的顺序排列:
(5)三甲胺(
 )和异丙胺(
)和异丙胺( )的沸点大小关系为:三甲胺
)的沸点大小关系为:三甲胺(6)基态原子的核外电子填充在5个轨道中的元素有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据下列五种元素的电离能数据(单位: ),回答下列问题。
),回答下列问题。
(1)在周期表中,最可能处于同一族的是___________ 。
A. 和
和 B.
B. 和
和 C.
C. 和
和 D.
D. 和
和 E.
E. 和
和
(2)它们的氯化物的化学式,最可能正确的是___________ 。
A.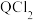 B.
B. C.
C. D.
D. E.
E.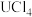
(3) 元素最可能是
元素最可能是___________ 。
A. 区元素 B.稀有气体元素 C.
区元素 B.稀有气体元素 C. 区元素 D.准金属 E.
区元素 D.准金属 E. 区元素
区元素
(4)下列元素中,化学性质和物理性质最像 元素的是
元素的是___________ 。
A.硼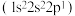 B.铍
B.铍 C.锂
C.锂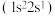 D.氢
D.氢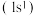 E.氦
E.氦
 ),回答下列问题。
),回答下列问题。| 元素代号 |  | 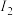 | 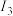 |  |
 | 2080 | 4000 | 6100 | 9400 |
 | 500 | 4600 | 6900 | 9500 |
 | 740 | 1400 | 7700 | 10500 |
 | 580 | 1800 | 2700 | 11600 |
 | 420 | 3100 | 4400 | 5900 |
(1)在周期表中,最可能处于同一族的是
A.
 和
和 B.
B. 和
和 C.
C. 和
和 D.
D. 和
和 E.
E. 和
和
(2)它们的氯化物的化学式,最可能正确的是
A.
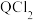 B.
B. C.
C. D.
D. E.
E.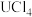
(3)
 元素最可能是
元素最可能是A.
 区元素 B.稀有气体元素 C.
区元素 B.稀有气体元素 C. 区元素 D.准金属 E.
区元素 D.准金属 E. 区元素
区元素(4)下列元素中,化学性质和物理性质最像
 元素的是
元素的是A.硼
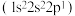 B.铍
B.铍 C.锂
C.锂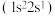 D.氢
D.氢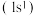 E.氦
E.氦
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】非金属氮化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态N原子核外电子的运动状态有_____ 种;N、O、F第一电离能由大到小的顺序为_____ 。氟化硝酰NO2F可用作火箭推进剂中的氧化剂,NO2F中心原子的杂化方式为_____ 。气态N2O5的分子结构为 ,而固态N2O5则由一种直线型的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为
,而固态N2O5则由一种直线型的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为_____ ,Y的离域键可表达为_____ 。
(2)人体内氧气的输送主要由红细胞内的血红蛋白负责,而红细胞以及血浆中还有少量的血蓝蛋白也能和氧气反应。用配体L,Cu离子和氧气能合成类似血监蛋白的模型配合物Cu2L2O22,该结构呈现出强烈的OO键断裂趋势,成键形态X与断键形态Y达成快速平衡。(iPr为异丙基)_____ ,含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。1molY离子中通过螯合作用形成的配位键有_____ mol。
(1)基态N原子核外电子的运动状态有
 ,而固态N2O5则由一种直线型的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为
,而固态N2O5则由一种直线型的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为(2)人体内氧气的输送主要由红细胞内的血红蛋白负责,而红细胞以及血浆中还有少量的血蓝蛋白也能和氧气反应。用配体L,Cu离子和氧气能合成类似血监蛋白的模型配合物Cu2L2O22,该结构呈现出强烈的OO键断裂趋势,成键形态X与断键形态Y达成快速平衡。(iPr为异丙基)

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载,锌是生命体必需的微量元素,被称为“生命之花”。(已知阿伏加德罗常数的值为NA)
(1)基态Zn原子核外的最高能层符号是___________ ,基态Zn2+最外层电子排布式为___________ 。
(2)乳酸锌[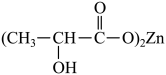 ]是一种很好的食品锌强化剂,其中存在的作用力有
]是一种很好的食品锌强化剂,其中存在的作用力有___________ (填字母)。1 mol乳酸锌中含有___________ 个σ键。
A.离子键 B.极性共价键
C.金属键 D.配位键
E.范德华力
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是___________ ,H2O分子的立体构型为___________ 形,Zn2+的配位数为___________ 。甘氨酸(H2N—CH2—COOH)中N原子的杂化轨道类型为___________ ;甘氨酸易溶于水,试从结构角度解释___________ 。
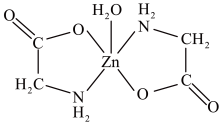
(1)基态Zn原子核外的最高能层符号是
(2)乳酸锌[
 ]是一种很好的食品锌强化剂,其中存在的作用力有
]是一种很好的食品锌强化剂,其中存在的作用力有A.离子键 B.极性共价键
C.金属键 D.配位键
E.范德华力
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铝及其化合物在制造、化工等领域都有广泛应用。回答下列问题:
(1)基态铝原子的核外电子排布式为_______ ,占据最高能级的电子云轮廓图形状为_______ 。基态铝原子比基态镁原子的第一电离能小,其原因是_______ 。
(2)通常情况下, 可由六氟铝酸铵[
可由六氟铝酸铵[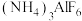 ]受热分解制得,反应的化学方程式为
]受热分解制得,反应的化学方程式为_______ 。
(3) 具有较高的熔点(1040℃),属于
具有较高的熔点(1040℃),属于_______ (填晶体类型)晶体。 在178℃时升华,
在178℃时升华, 、
、 的晶体类型不同的原因是
的晶体类型不同的原因是_______ 。
(4) 在水溶液中实际上是以
在水溶液中实际上是以 的形式存在。其中
的形式存在。其中 为配离子,Al原子的杂化方式为
为配离子,Al原子的杂化方式为_______ ,该阴离子中存在的化学键有_______ (填标号)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(1)基态铝原子的核外电子排布式为
(2)通常情况下,
 可由六氟铝酸铵[
可由六氟铝酸铵[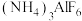 ]受热分解制得,反应的化学方程式为
]受热分解制得,反应的化学方程式为(3)
 具有较高的熔点(1040℃),属于
具有较高的熔点(1040℃),属于 在178℃时升华,
在178℃时升华, 、
、 的晶体类型不同的原因是
的晶体类型不同的原因是(4)
 在水溶液中实际上是以
在水溶液中实际上是以 的形式存在。其中
的形式存在。其中 为配离子,Al原子的杂化方式为
为配离子,Al原子的杂化方式为A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】表为周期表的一部分,其中的编号代表对应的元素。
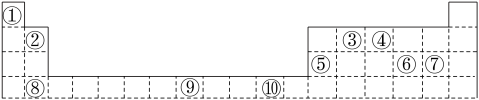
请回答下列问题:
(1)表中属于d区的元素是________ (填编号)。
(2)写出元素⑧的基态原子的电子排布式__________________________ 。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为________ 对。
(4)元素④的氢化物的分子构型为________ ,中心原子的杂化形式为________ 。
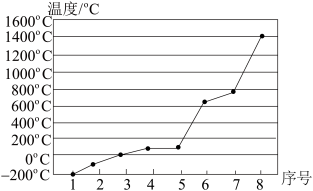
(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表________ (填元素符号);其中电负性最大的是________ (填图中的序号)。

请回答下列问题:
(1)表中属于d区的元素是
(2)写出元素⑧的基态原子的电子排布式
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为
(4)元素④的氢化物的分子构型为

(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表
您最近一年使用:0次



