工业燃煤、石油等化石燃料烧释放出大量 等气体,严重污染空气。对废气进行处理可实现绿色环保、废物利用。目前,在常温下处理
等气体,严重污染空气。对废气进行处理可实现绿色环保、废物利用。目前,在常温下处理 主要采用碱液吸收法。
主要采用碱液吸收法。
(1)用过量的烧碱溶液吸收 ,发生反应
,发生反应 ,若向所得的
,若向所得的 溶液滴入过氧化氢溶液,发生反应的离子方程式为
溶液滴入过氧化氢溶液,发生反应的离子方程式为_______ 。
(2)研究发现, 溶液也可以用来处理废气中的
溶液也可以用来处理废气中的 ,发生反应
,发生反应 ,查阅资料可知,常温下,
,查阅资料可知,常温下, 电离平衡常数:
电离平衡常数: ,
, 。
。
①写出 发生水解反应的离子方程式:
发生水解反应的离子方程式:_______ ;常温下,该反应的
_______ 。
② 溶液中
溶液中
_______ (填“>”、“<”或“=”) 。
。
(3)常温下,若向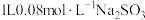 溶液中缓慢通入
溶液中缓慢通入 ,整个过程无气体逸出,忽略溶液体积的变化,测得溶液的pH与通入
,整个过程无气体逸出,忽略溶液体积的变化,测得溶液的pH与通入 物质的量之间的变化曲线如图所示:
物质的量之间的变化曲线如图所示:
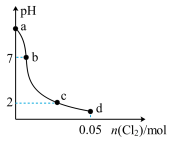
①a点
_______ (精确到小数点后一位)。
②下列说法错误的是_______ (填标号)。
A.c点溶液中存在
B.b点
C.d点溶液中溶质只有 、
、 和
和
D.a点溶液中存在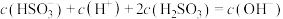
(4)还可以采用多步法来处理废气中的 :
:
第1步:用过理的浓氨水吸收 ,并在空气中氧化;
,并在空气中氧化;
第2步:加入石灰水,发生反应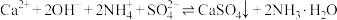 K。
K。
则
_______ [已知: ,
,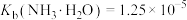 ]。
]。
 等气体,严重污染空气。对废气进行处理可实现绿色环保、废物利用。目前,在常温下处理
等气体,严重污染空气。对废气进行处理可实现绿色环保、废物利用。目前,在常温下处理 主要采用碱液吸收法。
主要采用碱液吸收法。(1)用过量的烧碱溶液吸收
 ,发生反应
,发生反应 ,若向所得的
,若向所得的 溶液滴入过氧化氢溶液,发生反应的离子方程式为
溶液滴入过氧化氢溶液,发生反应的离子方程式为(2)研究发现,
 溶液也可以用来处理废气中的
溶液也可以用来处理废气中的 ,发生反应
,发生反应 ,查阅资料可知,常温下,
,查阅资料可知,常温下, 电离平衡常数:
电离平衡常数: ,
, 。
。①写出
 发生水解反应的离子方程式:
发生水解反应的离子方程式:
②
 溶液中
溶液中
 。
。(3)常温下,若向
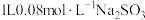 溶液中缓慢通入
溶液中缓慢通入 ,整个过程无气体逸出,忽略溶液体积的变化,测得溶液的pH与通入
,整个过程无气体逸出,忽略溶液体积的变化,测得溶液的pH与通入 物质的量之间的变化曲线如图所示:
物质的量之间的变化曲线如图所示:
①a点

②下列说法错误的是
A.c点溶液中存在

B.b点

C.d点溶液中溶质只有
 、
、 和
和
D.a点溶液中存在
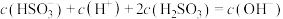
(4)还可以采用多步法来处理废气中的
 :
:第1步:用过理的浓氨水吸收
 ,并在空气中氧化;
,并在空气中氧化;第2步:加入石灰水,发生反应
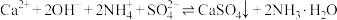 K。
K。则

 ,
,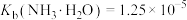 ]。
]。
更新时间:2024-01-21 21:40:11
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】常温下,几种物质的溶度积常数见下表:
(1)写出 的溶度积常数表达式
的溶度积常数表达式___________ 。
(2)某酸性 溶液中含少到的
溶液中含少到的 ,为制得纯净的
,为制得纯净的 溶液,宜加入
溶液,宜加入___________ 调至溶液 ,使
,使 转化为
转化为 沉淀,此时溶液中的
沉淀,此时溶液中的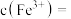
___________ 。
(3)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成 写出反应的离子方程式:
写出反应的离子方程式:___________ 。
(4)某工业废水中含有 等重金属离子,最适宜向此工业废水中加入过量的
等重金属离子,最适宜向此工业废水中加入过量的___________ (填字母)除去它们。
A.NaOH B. C.Na2S
C.Na2S
| 物质 |  |  |  |  |  |
 | 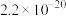 |  |  | 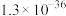 | 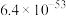 |
 的溶度积常数表达式
的溶度积常数表达式(2)某酸性
 溶液中含少到的
溶液中含少到的 ,为制得纯净的
,为制得纯净的 溶液,宜加入
溶液,宜加入 ,使
,使 转化为
转化为 沉淀,此时溶液中的
沉淀,此时溶液中的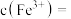
(3)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成
 写出反应的离子方程式:
写出反应的离子方程式:(4)某工业废水中含有
 等重金属离子,最适宜向此工业废水中加入过量的
等重金属离子,最适宜向此工业废水中加入过量的A.NaOH B.
 C.Na2S
C.Na2S
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料制备铵铁蓝Fe(NH4)Fe(CN)6颜料。工艺流程如下:
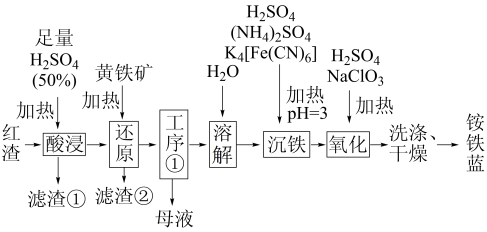
(1)还原工序中,不生成S单质的反应的化学方程式为_______ 。
(2)沉铁工序产生的白色沉淀Fe(NH4)2Fe(CN)6中Fe的化合价为_______ ,氧化工序发生反应的离子方程式为_______ 。

(1)还原工序中,不生成S单质的反应的化学方程式为
(2)沉铁工序产生的白色沉淀Fe(NH4)2Fe(CN)6中Fe的化合价为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】根据信息书写指定反应的方程式。
(1)①工业制取漂白粉的化学方程式:_______ 。
②将少量钠投入氯化铁溶液中发生的两个过程中化学方程式分别为_______ 、_______ 。
③向饱和Na2CO3溶液中通入过量的CO2,有NaHCO3晶体析出,写出反应的离子方程式_______ 。
(2)CuCl常用作杀菌剂、催化剂等。一种利用废弃铜锌合金制取CuCl的流程如下图所示:

④碱溶Zn时还会产生H2,写出碱溶时Zn反应的化学方程式:_______ 。
⑤已知稀硝酸氧化Cu时会产生污染空气的NO气体,该反应的离子方程式为_______ 。
⑥写出沉铜时反应的离子方程式:_______ 。
(1)①工业制取漂白粉的化学方程式:
②将少量钠投入氯化铁溶液中发生的两个过程中化学方程式分别为
③向饱和Na2CO3溶液中通入过量的CO2,有NaHCO3晶体析出,写出反应的离子方程式
(2)CuCl常用作杀菌剂、催化剂等。一种利用废弃铜锌合金制取CuCl的流程如下图所示:

④碱溶Zn时还会产生H2,写出碱溶时Zn反应的化学方程式:
⑤已知稀硝酸氧化Cu时会产生污染空气的NO气体,该反应的离子方程式为
⑥写出沉铜时反应的离子方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】含氮化合物在生活、生产和科技等方面有重要的应用。
⑴已知298 K时,亚硝酸(HNO2)的电离平衡常数Ka=5.1×10-4,H2CO3的电离平衡常数 Ka1=4.2×10-7、Ka2=5.61×10-11。
① NaNO2溶液呈____ (填“酸性”“碱性”或“中性”),原因是_________ (用离子方程式表示)。
②向含有1 mol碳酸钠的溶液中加入1 mol HNO2后,溶液中c(CO32-)、c(HCO3-)、c(NO2-)由大到小的顺序为________________ 。
(2)电化学催化净化NO是处理含氮化合物的一种新方法,原理如图所示,固体电解质起到传导O2-的作用。b极为电源的_____ (填“正极”或“负极”),通入NO的电极上的电极反应式为______ 。
⑶N2O5是绿色硝化剂,能溶于水生成硝酸。常温下,向0.1 mol·L-1的氨水中加入少量N2O5,使溶液中c(NH3•H2O):c(NH4+)=5 : 9,此时溶液中 c(NH4+)+c(H+) — c(NO3-)=_____ 。 (25℃时,NH3•H2O的电离常数Kb=1.8×10-5)
⑴已知298 K时,亚硝酸(HNO2)的电离平衡常数Ka=5.1×10-4,H2CO3的电离平衡常数 Ka1=4.2×10-7、Ka2=5.61×10-11。
① NaNO2溶液呈
②向含有1 mol碳酸钠的溶液中加入1 mol HNO2后,溶液中c(CO32-)、c(HCO3-)、c(NO2-)由大到小的顺序为
(2)电化学催化净化NO是处理含氮化合物的一种新方法,原理如图所示,固体电解质起到传导O2-的作用。b极为电源的
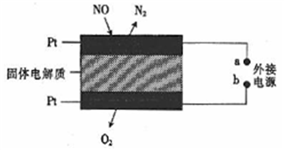
⑶N2O5是绿色硝化剂,能溶于水生成硝酸。常温下,向0.1 mol·L-1的氨水中加入少量N2O5,使溶液中c(NH3•H2O):c(NH4+)=5 : 9,此时溶液中 c(NH4+)+c(H+) — c(NO3-)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】氨气的水溶液称为氨水,它的主要存在微粒是NH3·H2O。已知:
a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5mol/L b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O
则CH3COONH4溶液呈_________ 性(填“酸”、“碱”或“中”),NH4HCO3溶液呈____ 性(填“酸”、“碱”或“中”),NH4HCO3溶液中浓度最大的离子是_______ (填离子的化学式)。
a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5mol/L b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O
则CH3COONH4溶液呈
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】现有HA、HB和H2C三种酸。常温下用0.1mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图所示。

(1)HA、HB两种酸的酸性强弱关系为HA_______ HB(填“>”“<”或“=”)。
(2)a点时的溶液中由水电离出的c(H+)=_______ mol·L-1,Ka(HB)=_______ 。
(3)与曲线I上的c点对应的溶液中各离子浓度由大到小的顺序为_______ ;b点对应的溶液中c(HB)_______ c(B-)(填“>”“<”或“=”)
(4)已知常温下向0.1mol·L-1的NaHC溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHC的电离方程式为_______ 。
②若在此溶液中能检测到H2C分子,则此溶液中c(C2-)_______ c(H2C)(填“>”“<”或“=”)。
③若H2C的一级电离为H2C=H++HC-,常温下0.1mol·L-1H2C溶液中的c(H+)=0.11mol·L-1,则0.1mol·L-1NaHC溶液中的c(H+)_______ 0.01mol·L-1(填“>”“<”或“=”)。

(1)HA、HB两种酸的酸性强弱关系为HA
(2)a点时的溶液中由水电离出的c(H+)=
(3)与曲线I上的c点对应的溶液中各离子浓度由大到小的顺序为
(4)已知常温下向0.1mol·L-1的NaHC溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHC的电离方程式为
②若在此溶液中能检测到H2C分子,则此溶液中c(C2-)
③若H2C的一级电离为H2C=H++HC-,常温下0.1mol·L-1H2C溶液中的c(H+)=0.11mol·L-1,则0.1mol·L-1NaHC溶液中的c(H+)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】填空。
(1)书写对应的化学用语:
①氯化铁溶液可作净水剂,离子方程式解释其原理为___________ 。
②氯碱工业对应的离子方程式为___________ 。
(2)已知Ag2CrO4、AgCl的Ksp数值分别为2.0×10-12和2.0×10-10,在化学分析中采用K2CrO4作指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-6mol/L)时,溶液中c(Ag+)为
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-6mol/L)时,溶液中c(Ag+)为___________ mol/L,此时溶液中c( )等于
)等于___________ mol/L。
(3)常温下,有下列4种溶液
a:pH=11的氨水 b:pH=11的氢氧化钠溶液 c:pH=3的醋酸 d:pH=3的盐酸
①在a和b中分别加入适量的氯化铵晶体后,两种溶液的pH均___________ ,(填“增大”“减小”或“不变”),从平衡移动角度解释a溶液中pH变化的原因___________ 。
②将溶液a和d按比例混合后溶液恰好为中性,所得溶液中离子浓度从大到小排列的顺序为___________ ,该溶液中水电离的氢离子浓度为___________ mol/L。
③将xL溶液d与yL溶液b混合后,所得溶液的pH=4,则x:y=___________ 。
(1)书写对应的化学用语:
①氯化铁溶液可作净水剂,离子方程式解释其原理为
②氯碱工业对应的离子方程式为
(2)已知Ag2CrO4、AgCl的Ksp数值分别为2.0×10-12和2.0×10-10,在化学分析中采用K2CrO4作指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与
 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-6mol/L)时,溶液中c(Ag+)为
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-6mol/L)时,溶液中c(Ag+)为 )等于
)等于(3)常温下,有下列4种溶液
a:pH=11的氨水 b:pH=11的氢氧化钠溶液 c:pH=3的醋酸 d:pH=3的盐酸
①在a和b中分别加入适量的氯化铵晶体后,两种溶液的pH均
②将溶液a和d按比例混合后溶液恰好为中性,所得溶液中离子浓度从大到小排列的顺序为
③将xL溶液d与yL溶液b混合后,所得溶液的pH=4,则x:y=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】
(1)向0.1 mol•L-1的氨水中加入少量的明矾,溶液中的NH 的浓度
的浓度______ (填“增大”或“减小”);
(2)25℃,在0.l0mol•L-1溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图 (忽略溶液体积的变化、H2S的挥发)。
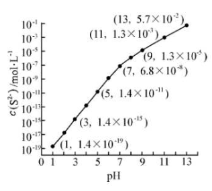
①pH = 13 时,溶液中的 c(H2S) +c(HS-) =________ mol•L-1;
②某溶液含0.020mol•L-1Mn2+0.l0mol•L-1H2S,当溶液pH =____ 时,Mn2+开始沉淀(已知:[Ksp(MnS)=28×10-13)。
(3)25℃,两种酸的电离平衡常数如下表。
①0.l0mol•L-1NaHSO3溶液中离子浓度由大到小的顺序为__________ ;
②向NaHCO3溶液中通入少量二氧化硫时反应的离子方程式为_________ ;
(4)银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知Ksp(AgCl)=1.8×l0-10,若向 5mL0.018mol•L-1的 AgNO3 溶液中加入5mL 0.020mol•L-1的盐酸,混合后溶液中的Ag+的浓度为________ mol•L-1。
(1)向0.1 mol•L-1的氨水中加入少量的明矾,溶液中的NH
 的浓度
的浓度(2)25℃,在0.l0mol•L-1溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图 (忽略溶液体积的变化、H2S的挥发)。

①pH = 13 时,溶液中的 c(H2S) +c(HS-) =
②某溶液含0.020mol•L-1Mn2+0.l0mol•L-1H2S,当溶液pH =
(3)25℃,两种酸的电离平衡常数如下表。
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
①0.l0mol•L-1NaHSO3溶液中离子浓度由大到小的顺序为
②向NaHCO3溶液中通入少量二氧化硫时反应的离子方程式为
(4)银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知Ksp(AgCl)=1.8×l0-10,若向 5mL0.018mol•L-1的 AgNO3 溶液中加入5mL 0.020mol•L-1的盐酸,混合后溶液中的Ag+的浓度为
您最近一年使用:0次



