类比和推理是重要的学习方法。下列类比或推理合理的是
| 选项 | 已知 | 方法 | 结论 |
| A | 常温下,Kb(NH3·H2O)=1.8×10-5、Ka(HF)=6.3×10-4 | 推理 | NH4F溶液显酸性 |
| B | Ksp:Ag2CrO4<AgCl | 推理 | 溶解度:Ag2CrO4<AgCl |
| C | Fe+CuSO4(aq)=FeSO4+Cu | 类比 | 2Na+CuSO4(aq)=Na2SO4+Cu |
| D | 工业电解熔融氯化镁制镁 | 类比 | 工业电解熔融氯化铝制铝 |
| A.A | B.B | C.C | D.D |
更新时间:2024-01-18 19:04:48
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知25℃时,几种弱酸的电离平衡常数如下: HCOOH:K离=1.77×10-4,HCN:K离=4.9×10-10,H2CO3:Ka1=4.4×10-7,K a2=4.7×10-11,则以下方程式不正确的是( )
| A.HCOOH+NaCN=HCOONa+HCN | B.Na2CO3+HCN=NaHCO3+NaCN |
| C.2NaCN+H2O+CO2=2HCN+Na2CO3 | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )
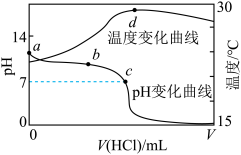

| A.a点由水电离出的c(H+)=1.0×10-14mol/L |
| B.b点时c(NH4+)+c(NH3·H2O)>c(Cl-) |
| C.c点时消耗的盐酸体积:V(HCl)=20.00mL |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】常温下,某PbI2悬浊液中存在平衡PbI2(s)  Pb2+(aq)+2I-(aq),加入少量KI固体并完全溶解。下列说法错误的是
Pb2+(aq)+2I-(aq),加入少量KI固体并完全溶解。下列说法错误的是
 Pb2+(aq)+2I-(aq),加入少量KI固体并完全溶解。下列说法错误的是
Pb2+(aq)+2I-(aq),加入少量KI固体并完全溶解。下列说法错误的是| A.溶度积常数Ksp(PbI2)减小 | B.溶液中c(I-)增大 |
| C.沉淀溶解平衡向左移动 | D.悬浊液中固体质量增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列实验操作、对应的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 室温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸 | 有气泡产生 | Ksp(BaCO3)< Ksp(BaSO4) |
| B | 将浸透石蜡油的石棉放置在硬质试管底部,加入少量碎瓷片并加强热,将生成的气体通入酸性高锰酸钾溶液中。 | 高锰酸钾溶液 褪色 | 石蜡油分解产物中含有不饱和烃 |
| C | 向鸡蛋清溶液中滴加几滴CuSO4溶液 | 产生白色沉淀 | 蛋白质发生盐析 |
| D | 室温下,测定同浓度Na2CO3 和Na2SO3 溶液的pH | pH前者大于 后者 | 碳元素非金属性弱于硫 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
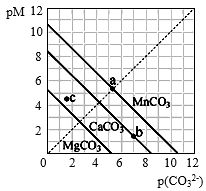
【推荐3】一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示。已知:pM=-lg c(M),p(CO )=-lg c(CO
)=-lg c(CO ),下列说法不正确的是
),下列说法不正确的是
 )=-lg c(CO
)=-lg c(CO ),下列说法不正确的是
),下列说法不正确的是
| A.MgCO3、CaCO3、MnCO3的Ksp依次增大 |
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO ) ) |
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)>c(CO ) ) |
D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO ) ) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关海水综合利用的说法中,不正确的是
| A.用氯气从海水中提溴的关键反应:Cl2+2Br-=2Cl-+Br2 |
| B.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |
| C.由海水制取粗盐的方法主要是蒸发结晶法 |
| D.从海水中可以得到氯化镁,再经过电解可制金属镁 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】海水是镁资源的贮存库,从海水中提取MgCl2用于制取金属镁以被广泛的应用于工业生产,其中制取镁的方法是
| A.热分解法 | B.用CO还原 | C.电解法 | D.湿法治金 |
您最近一年使用:0次

 某一元酸HA在水中有
某一元酸HA在水中有 发生电离,下列叙述不正确的是
发生电离,下列叙述不正确的是 ;
;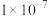 ;
; 约为水电离出的
约为水电离出的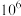 倍;
倍;

