神舟十五号顺利发射升空,标志着我国航天事业的飞速发展。
Ⅰ.火箭推进剂的研究是航天工业中的重要课题,常见推进剂的燃料包括汽油液肼(N2H4)、液氢等,具有不同的推进效能。回答下列问题:
(1)火箭推进剂可用N2H4作燃料,N2O4作氧化剂,反应的热化学方程式可表示为2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H1。
相关物质的摩尔生成焓∆HfHm如下表所示。
注:一定温度下,由元素的最稳定单质生成1mol纯物质的热效应称为该物质的摩尔生成焓,用∆HfHm表示。如N2H4(1)的摩尔生成焓:N2(g)+2H2(g)=N2H4(l) ∆HfHm =+165.8kJ/mol
①∆H1=___________ kJ/mol。
②结合化学反应原理分析,N2H4(l)作推近剂燃料可与N2O4(g)自发进行反应的原因是___________ 。
(2)火箭推进器内氢氧燃烧的简化反应历程如下图所示,分析其反应机理。
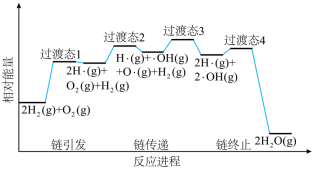
该历程分步进行,其中氢氧燃烧决速步对应的反应方程式为___________ 。
Ⅱ.在温度T下,容积固定的密闭容器中充入3 mol NO和2 mol H2发生2H2(g)+2NO(g) N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
(3)则NO的平衡转化率α(NO)=___________ (结果保留三位有效数字),该反应的平衡常数Kp=___________ (用含P0的代数式表示)
Ⅰ.火箭推进剂的研究是航天工业中的重要课题,常见推进剂的燃料包括汽油液肼(N2H4)、液氢等,具有不同的推进效能。回答下列问题:
(1)火箭推进剂可用N2H4作燃料,N2O4作氧化剂,反应的热化学方程式可表示为2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H1。
相关物质的摩尔生成焓∆HfHm如下表所示。
| 物质 | N2O4(g) | N2H4(l) | H2O(g) |
| 摩尔生成焓∆HfHm(kJ/mol) | +10.8 | +165.8. | -242.0 |
①∆H1=
②结合化学反应原理分析,N2H4(l)作推近剂燃料可与N2O4(g)自发进行反应的原因是
(2)火箭推进器内氢氧燃烧的简化反应历程如下图所示,分析其反应机理。

该历程分步进行,其中氢氧燃烧决速步对应的反应方程式为
Ⅱ.在温度T下,容积固定的密闭容器中充入3 mol NO和2 mol H2发生2H2(g)+2NO(g)
 N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,(3)则NO的平衡转化率α(NO)=
更新时间:2024-01-26 16:26:55
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】苯乙烯是一种重要的有机化工原料,可利用乙苯催化脱氢法制备,实际生产中常在体系中充入一定量的CO2,主要反应如下:
I.C8H10(g)=C8H8(g)+H2(g) ΔH1=+117.6kJ·mol-1;
II.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1。
回答下列问题:
(1)相比于乙苯直接脱氢制苯乙烯,工业实际生产中充入一定量CO2的优点为___________ (任写一点);二氧化碳与乙苯气体反应生成苯乙烯气体、一氧化碳和水蒸气的热化学方程式为___________ 。
(2)一定温度下,起始向10L盛放催化剂的恒容密闭容器中充入2 mol C8H10(g)和1 molCO2(g)发生反应I和反应II.20min末达到平衡时,C8H8(g)、H2O(g)的体积分数分别为25%和5%。
①0~20 min内,用C8H10的物质的量浓度变化表示的平均反应速率v(C8H10)=___________ 。
②反应II的平衡常数Kc=___________ 。
③起始投料量不变,在不同温度、压强下重复实验,测得H2的平衡体积分数与温度和压强的关系如图所示。
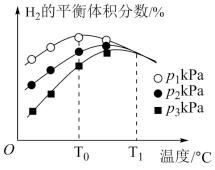
由图可知,温度低于T0℃时,以反应___________ (填“I”或“II”)为主,理由为___________ ;T1℃时,三条曲线几乎相交的原因为___________ ,P1、P2、P3由大到小的顺序为___________ 。
(3)若乙苯催化脱氢过程中发生积碳反应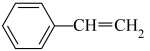 (g)=8C(s)+4H2(g) ΔH3=-126 kJ·mol-1.积碳反应可能导致的后果为
(g)=8C(s)+4H2(g) ΔH3=-126 kJ·mol-1.积碳反应可能导致的后果为___________ (任写一点)。
I.C8H10(g)=C8H8(g)+H2(g) ΔH1=+117.6kJ·mol-1;
II.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1。
回答下列问题:
(1)相比于乙苯直接脱氢制苯乙烯,工业实际生产中充入一定量CO2的优点为
(2)一定温度下,起始向10L盛放催化剂的恒容密闭容器中充入2 mol C8H10(g)和1 molCO2(g)发生反应I和反应II.20min末达到平衡时,C8H8(g)、H2O(g)的体积分数分别为25%和5%。
①0~20 min内,用C8H10的物质的量浓度变化表示的平均反应速率v(C8H10)=
②反应II的平衡常数Kc=
③起始投料量不变,在不同温度、压强下重复实验,测得H2的平衡体积分数与温度和压强的关系如图所示。

由图可知,温度低于T0℃时,以反应
(3)若乙苯催化脱氢过程中发生积碳反应
 (g)=8C(s)+4H2(g) ΔH3=-126 kJ·mol-1.积碳反应可能导致的后果为
(g)=8C(s)+4H2(g) ΔH3=-126 kJ·mol-1.积碳反应可能导致的后果为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】碳、氮和铝的单质及其化合物在工农业生产和生活中有重要用途.
(1)真空碳热还原一氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlC13(g)+3C(s)═3AlCl(g)+3CO(g)△H=a kJ•mol﹣1
3AlCl(g)═2Al(l)+AlC13(g)△H=b kJ•mol﹣1
用含a、b的代数式表示反应:Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=_____ kJ•mol﹣1.
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g)△H=Q kJ•mol﹣1.在T1℃时,反应进行到不同时间测得各物质的浓度如下(时间单位为min,浓度单位为mol/L):
①0~10min内,NO的平均反应速率v(NO)=_____ ,T1℃时,该反应的平衡常数K=_____ .
②30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q_____ 0(填“>”、“<”或“═”)
③在恒容条件下,能判断该反应一定达到化学平衡状态的依据是_____ (填选项编号).
a.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
b.反应体系的压强不再发生改变
c.混合气体的密度保持不变
d.混合气体的平均相对分子质量保持不变
④若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)=_____ mol/L.NO的转化率_____ (填“增大”、“减小”或“不变”).
(3)直接排放煤燃烧产生的烟气会引起严重的环境问题,将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图.电极b表面发生的电极反应式为_____ .

(1)真空碳热还原一氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlC13(g)+3C(s)═3AlCl(g)+3CO(g)△H=a kJ•mol﹣1
3AlCl(g)═2Al(l)+AlC13(g)△H=b kJ•mol﹣1
用含a、b的代数式表示反应:Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g)△H=Q kJ•mol﹣1.在T1℃时,反应进行到不同时间测得各物质的浓度如下(时间单位为min,浓度单位为mol/L):
 | 0 | 10 | 20 | 30 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 |
| N2 | 0 | 0.16 | 0.25 | 0.25 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 |
①0~10min内,NO的平均反应速率v(NO)=
②30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q
③在恒容条件下,能判断该反应一定达到化学平衡状态的依据是
a.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
b.反应体系的压强不再发生改变
c.混合气体的密度保持不变
d.混合气体的平均相对分子质量保持不变
④若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)=
(3)直接排放煤燃烧产生的烟气会引起严重的环境问题,将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图.电极b表面发生的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】大气环境中 的减量化排放受到国内外广泛关注。利用碳还原NO的反应为:
的减量化排放受到国内外广泛关注。利用碳还原NO的反应为: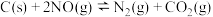 。回答下列问题:
。回答下列问题:
(1)该反应在常温下可以自发进行,则反应的
________ 0(填“ ”“
”“ ”或“
”或“ ”),有利于提高NO平衡转化率的条件是
”),有利于提高NO平衡转化率的条件是________ (任写一条)。
(2)以上反应可分为如下四步反应历程,写出其中第三步的反应:
第一步: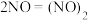
第二步: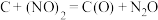
第三步:________
第四步: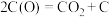
(3)对比研究活性炭负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、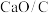 、
、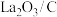 ,通入
,通入 使其浓度达到
使其浓度达到 。不同温度下,测得第2小时NO去除率如图所示:
。不同温度下,测得第2小时NO去除率如图所示:
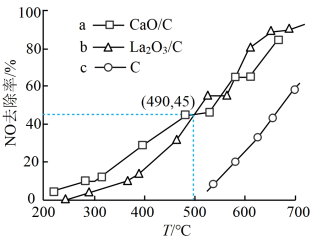
①据图分析,490℃以下,三种情况下反应的活化能最小的是________ (用a、b、c表示);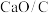 、
、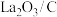 去除NO效果比C更好,其依据是
去除NO效果比C更好,其依据是________ (写一条)。
②上述实验中,490℃时,若测得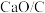 对NO的去除率为60%,则可能采取的措施是
对NO的去除率为60%,则可能采取的措施是________ 。
A.及时分离出 B.压缩体积
B.压缩体积
C.恒容下,向体系中通入氮气 D.寻找更好的催化剂
③490℃时的反应速率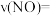
________ 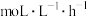 ,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为
,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为________ (保留二位有效数字)。
 的减量化排放受到国内外广泛关注。利用碳还原NO的反应为:
的减量化排放受到国内外广泛关注。利用碳还原NO的反应为: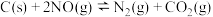 。回答下列问题:
。回答下列问题:(1)该反应在常温下可以自发进行,则反应的

 ”“
”“ ”或“
”或“ ”),有利于提高NO平衡转化率的条件是
”),有利于提高NO平衡转化率的条件是(2)以上反应可分为如下四步反应历程,写出其中第三步的反应:
第一步:
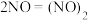
第二步:
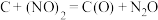
第三步:
第四步:
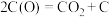
(3)对比研究活性炭负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、
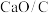 、
、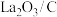 ,通入
,通入 使其浓度达到
使其浓度达到 。不同温度下,测得第2小时NO去除率如图所示:
。不同温度下,测得第2小时NO去除率如图所示:
①据图分析,490℃以下,三种情况下反应的活化能最小的是
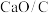 、
、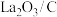 去除NO效果比C更好,其依据是
去除NO效果比C更好,其依据是②上述实验中,490℃时,若测得
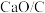 对NO的去除率为60%,则可能采取的措施是
对NO的去除率为60%,则可能采取的措施是A.及时分离出
 B.压缩体积
B.压缩体积C.恒容下,向体系中通入氮气 D.寻找更好的催化剂
③490℃时的反应速率
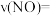
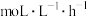 ,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为
,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】目前很多航空航天领域的研究内容与化学相关,如材料制备、反应条件选择等。
(1) 晶体是航天领域涉及的一种强关联二维材料,在一定条件下可发生如下反应:
晶体是航天领域涉及的一种强关联二维材料,在一定条件下可发生如下反应:
该反应在体积为 恒容密闭容器中,在温度分别为
恒容密闭容器中,在温度分别为 和
和 时进行两组实验,反应物起始物质的量,及到达平衡时部分物质的物质的量如下表:
时进行两组实验,反应物起始物质的量,及到达平衡时部分物质的物质的量如下表:
①则

___________ 0,该反应在一定条件下能自发进行的原因是___________ 。
②该反应的平衡常数表达式为___________ 。 时,向第一组实验达平衡后的容器中再充入
时,向第一组实验达平衡后的容器中再充入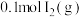 和
和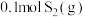 ,下列说法错误的是
,下列说法错误的是___________ 。
A.当 时,反应到达新的平衡
时,反应到达新的平衡
B.重新达平衡前
C.达新平衡时, 的平衡转化率大于33.3%
的平衡转化率大于33.3%
D.体系总压强不再改变时,反应达新平衡
E.当混合气体的颜色不再变化时,反应达新平衡
F.当混合气体的密度不再变化时,反应达新平衡
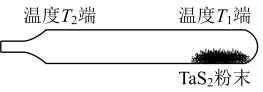
③利用“化学蒸气转移法”可以提纯含难挥发杂质的 粉末。反应在如图所示的石英真空管中进行。先在温度为
粉末。反应在如图所示的石英真空管中进行。先在温度为 的一端放入未提纯的
的一端放入未提纯的 粉末,充入少量
粉末,充入少量 ,一段时间后在温度为
,一段时间后在温度为 的一端得到了纯净
的一端得到了纯净 晶体。则温度较低的是
晶体。则温度较低的是___________ 端(填“ ”或“
”或“ ”)。
”)。
(2)某空间站生命保障系统功能之一是实现氧循环,其中涉及反应: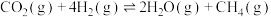 ,在相同条件下,
,在相同条件下, 与
与 还会发生不利于氧循环的副反应:
还会发生不利于氧循环的副反应: ,在一固定容积的反应器中按
,在一固定容积的反应器中按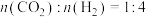 通入反应物,在不同温度、不同催化剂条件下,反应进行到
通入反应物,在不同温度、不同催化剂条件下,反应进行到 时,测得反应器中
时,测得反应器中 、
、 浓度
浓度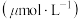 如下表所示。
如下表所示。
①在350℃时,催化剂Ⅰ的作用下,生成 的反应的活化能
的反应的活化能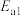
___________ 生成 的反应的活化能
的反应的活化能 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
②若该空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃的反应条件,原因是___________ 。
(1)
 晶体是航天领域涉及的一种强关联二维材料,在一定条件下可发生如下反应:
晶体是航天领域涉及的一种强关联二维材料,在一定条件下可发生如下反应:
该反应在体积为
 恒容密闭容器中,在温度分别为
恒容密闭容器中,在温度分别为 和
和 时进行两组实验,反应物起始物质的量,及到达平衡时部分物质的物质的量如下表:
时进行两组实验,反应物起始物质的量,及到达平衡时部分物质的物质的量如下表:| 起始时 | 平衡时 | ||||||||
 |  | 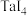 |  |  |  | 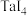 |  | ||
| 第一组 |  |  |  | 0 | 0 |  | |||
| 第二组 |  | 0 | 0 |  |  | 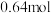 | |||


②该反应的平衡常数表达式为
 时,向第一组实验达平衡后的容器中再充入
时,向第一组实验达平衡后的容器中再充入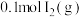 和
和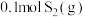 ,下列说法错误的是
,下列说法错误的是A.当
 时,反应到达新的平衡
时,反应到达新的平衡B.重新达平衡前

C.达新平衡时,
 的平衡转化率大于33.3%
的平衡转化率大于33.3%D.体系总压强不再改变时,反应达新平衡
E.当混合气体的颜色不再变化时,反应达新平衡
F.当混合气体的密度不再变化时,反应达新平衡
③利用“化学蒸气转移法”可以提纯含难挥发杂质的
 粉末。反应在如图所示的石英真空管中进行。先在温度为
粉末。反应在如图所示的石英真空管中进行。先在温度为 的一端放入未提纯的
的一端放入未提纯的 粉末,充入少量
粉末,充入少量 ,一段时间后在温度为
,一段时间后在温度为 的一端得到了纯净
的一端得到了纯净 晶体。则温度较低的是
晶体。则温度较低的是 ”或“
”或“ ”)。
”)。
(2)某空间站生命保障系统功能之一是实现氧循环,其中涉及反应:
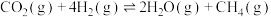 ,在相同条件下,
,在相同条件下, 与
与 还会发生不利于氧循环的副反应:
还会发生不利于氧循环的副反应: ,在一固定容积的反应器中按
,在一固定容积的反应器中按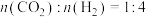 通入反应物,在不同温度、不同催化剂条件下,反应进行到
通入反应物,在不同温度、不同催化剂条件下,反应进行到 时,测得反应器中
时,测得反应器中 、
、 浓度
浓度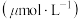 如下表所示。
如下表所示。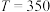 ℃ ℃ | 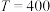 ℃ ℃ | |||
 |  |  |  | |
| 催化剂Ⅰ | 10.8 | 12722 | 345.2 | 42780 |
| 催化剂Ⅱ | 9.2 | 10775 | 34 | 38932 |
 的反应的活化能
的反应的活化能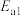
 的反应的活化能
的反应的活化能 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。②若该空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃的反应条件,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】2019年10月1日,我国成功举办国庆七十周年阅兵活动。其中阅兵仪式上混合动力车等新能源车辆的亮相,展示了综合国力、国防科技发展水平。同时也说明能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
工业上用天然气为原料,分为两阶段制备甲醇:
(i)制备合成气:CH4(g)+H2O(g) ⇌CO(g)+3H2(g) ΔH= +206.0kJ•mol-1
(ii)合成甲醇:CO(g)+2H2(g)⇌CH3OH(g) ΔH= -90.67kJ•mol-1
(1)制备合成气:工业生产中为解决合成气中H2过量而 CO 不足的问题,原料气中需添加CO2,发生的反应(iii):CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH= +41.17kJ•mol-1,为了使合成气配比最佳,理论上原料气中二氧化碳与甲烷质量比为_______ 。
(2)为节约化石能源、减少碳排放,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①请写出二氧化碳加氢合成水蒸气和甲醇的热化学方程式____________ 。
②研究表明在二氧化碳合成甲醇的原料气的反应中,保持其它条件不变,采用Ⅰ、Ⅱ、Ⅲ三种催化剂,反应进行相同时间后,CO2的转化率随反应体系的温度变化如图所示:
a~d 点中反应一定处于平衡状态的点是____ ;CO2的转化率 a 点比 c 点高的原因是 ____ 。
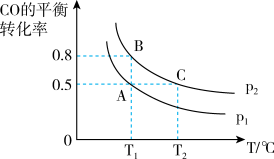
③最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:
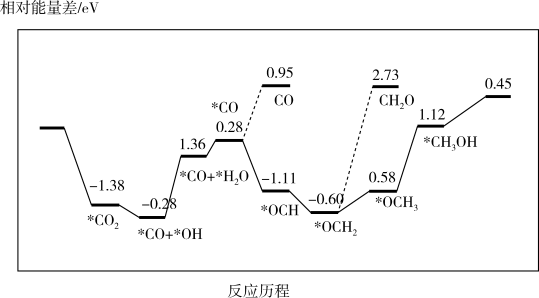
容易得到的副产物有 CO 和CH2O,其中相对较少的副产物为___ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中____ (填字母)的能量变化。
A.*CO → *OCH B.*CO+*OH→*CO+*H2O
C.*OCH2→*OCH3D.*OCH3→*CH3OH
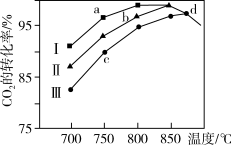
(3)在一容积可变的密闭容器中充入10molCO和20molH2合成甲醇,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
①比较A、B 两点压强大小PA_______ PB填“>、<、 =”)
②若达到化学平衡状态 A 时,容器的体积为 10 L,如果反应开始时仍充入 10molCO和20molH2,则在平衡状态 B 时,容器的体积V(B)=_______ L;
工业上用天然气为原料,分为两阶段制备甲醇:
(i)制备合成气:CH4(g)+H2O(g) ⇌CO(g)+3H2(g) ΔH= +206.0kJ•mol-1
(ii)合成甲醇:CO(g)+2H2(g)⇌CH3OH(g) ΔH= -90.67kJ•mol-1
(1)制备合成气:工业生产中为解决合成气中H2过量而 CO 不足的问题,原料气中需添加CO2,发生的反应(iii):CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH= +41.17kJ•mol-1,为了使合成气配比最佳,理论上原料气中二氧化碳与甲烷质量比为
(2)为节约化石能源、减少碳排放,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①请写出二氧化碳加氢合成水蒸气和甲醇的热化学方程式
②研究表明在二氧化碳合成甲醇的原料气的反应中,保持其它条件不变,采用Ⅰ、Ⅱ、Ⅲ三种催化剂,反应进行相同时间后,CO2的转化率随反应体系的温度变化如图所示:


a~d 点中反应一定处于平衡状态的点是
③最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:

容易得到的副产物有 CO 和CH2O,其中相对较少的副产物为
A.*CO → *OCH B.*CO+*OH→*CO+*H2O
C.*OCH2→*OCH3D.*OCH3→*CH3OH
(3)在一容积可变的密闭容器中充入10molCO和20molH2合成甲醇,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
①比较A、B 两点压强大小PA
②若达到化学平衡状态 A 时,容器的体积为 10 L,如果反应开始时仍充入 10molCO和20molH2,则在平衡状态 B 时,容器的体积V(B)=
您最近一年使用:0次
【推荐3】氨是重要的无机化工产品,工业合成涉及到的主反应是N2(g)+3H2(g)⇌2NH3(g)。回答下列问题:
(1)已知1molN2中的共价键断裂吸收Q1kJ能量;1molH2中的共价键断裂吸收Q2kJ能量;形成1molN-H释放Q3kJ能量。
①N2(g)+3H2(g)⇌2NH3(g) △H=_______ kJ·mol-1。
②Fe3O4为该反应的催化剂,使用时常加入Al2O3与之生成合金FeO·Al2O3使Fe3O4分布均匀,其目的是_______ 。
(2)用平衡分压p(NH3)、p(N2)、p(H2)代替平衡浓度表示化学平衡常数。温度不变,将平衡时体系的总压强p1增加到原来的两倍,则此时Qp=_______ (用含Kp的代数式表示)。
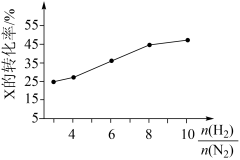
(3)T℃时,在有催化剂的恒容密闭容器只中充入N2和H2。如图所示为不同投料比[ ]时某反应物X的的平衡转化率的变化曲线。反应物X是
]时某反应物X的的平衡转化率的变化曲线。反应物X是_______ (填“N2”或“H2”),判断依据是______________ 。
(4)工业上可通过反应CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1制备原料气氢气。
①制备过程中一般采用较高的压强(3.0MPa),原因是_______ ;原料气在进入氨合成塔前需除去CO,原因是_______ 。
②在镍催化剂表面存在如下反应机理(*表示镍表面活性中心,上标*表示组分被活性中心吸附):
I.CH4+2*=CH3*+H*(慢)H2O+*=H2+O*
II.CH3*+*=CH2*+H*
III.CH2*+*=CH*+H*
IV.CH*+O*=CO*+H*
V.CO*=CO+*
甲烷在镍催化表面发生的五个基元反应中,活化能最大的是_______ (填标号)。若反应CH4(g)+H2O(g)=CO(g)+3H2(g)在任意温度下能自发进行,则ΔH1_______ 0(填“大于”或“小于”)。
(1)已知1molN2中的共价键断裂吸收Q1kJ能量;1molH2中的共价键断裂吸收Q2kJ能量;形成1molN-H释放Q3kJ能量。
①N2(g)+3H2(g)⇌2NH3(g) △H=
②Fe3O4为该反应的催化剂,使用时常加入Al2O3与之生成合金FeO·Al2O3使Fe3O4分布均匀,其目的是
(2)用平衡分压p(NH3)、p(N2)、p(H2)代替平衡浓度表示化学平衡常数。温度不变,将平衡时体系的总压强p1增加到原来的两倍,则此时Qp=
(3)T℃时,在有催化剂的恒容密闭容器只中充入N2和H2。如图所示为不同投料比[
 ]时某反应物X的的平衡转化率的变化曲线。反应物X是
]时某反应物X的的平衡转化率的变化曲线。反应物X是
(4)工业上可通过反应CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1制备原料气氢气。
①制备过程中一般采用较高的压强(3.0MPa),原因是
②在镍催化剂表面存在如下反应机理(*表示镍表面活性中心,上标*表示组分被活性中心吸附):
I.CH4+2*=CH3*+H*(慢)H2O+*=H2+O*
II.CH3*+*=CH2*+H*
III.CH2*+*=CH*+H*
IV.CH*+O*=CO*+H*
V.CO*=CO+*
甲烷在镍催化表面发生的五个基元反应中,活化能最大的是
您最近一年使用:0次
【推荐1】830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)⇌CO2(g)+H2(g) △H<0。试回答下列问题:
(1)若起始时c(CO)=2 mol·L-1,c(H2O)=3 mol·L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=_______
(2)在相同温度下,若起始时c(CO)=1 mol·L-1,c(H2O)=2 mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时v(正)_______ v(逆)(填“大于”“小于”或“等于”)
(3)若降低温度,该反应的化学反应速率将_______ (均填“增大”“减小”或“不变”)。
(4)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ·mol-1
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=-47.2kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ·mol-1
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:_______ 。
(1)若起始时c(CO)=2 mol·L-1,c(H2O)=3 mol·L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=
(2)在相同温度下,若起始时c(CO)=1 mol·L-1,c(H2O)=2 mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时v(正)
(3)若降低温度,该反应的化学反应速率将
(4)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ·mol-1
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=-47.2kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ·mol-1
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
您最近一年使用:0次
【推荐2】氮及其化合物在工业上有重要用途。请回答下列有关问题:
(1)已知N2(g)+O2(g)=2NO(g) ΔH =+180.5kJ·mol-1,N2(g)+3H2(g) 2NH3(g)ΔH =-92.4kJ·mol-1,2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ·mol-1,写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为
2NH3(g)ΔH =-92.4kJ·mol-1,2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ·mol-1,写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为_________
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g),在恒温恒压下判断该反应达到化学平衡状态的依据是
2NH3(g),在恒温恒压下判断该反应达到化学平衡状态的依据是______ (填序号);
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2) (正)=v(H2) (逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)在有氧条件下,新型催化剂M能催化 与
与 生成
生成 。将一定比例的
。将一定比例的 、
、 和
和 的混合气体,匀速通入装有催化剂M的反应器中反应(装置见图)。
的混合气体,匀速通入装有催化剂M的反应器中反应(装置见图)。
反应相同时间 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在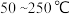 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后上升缓慢,迅速上升段是催化剂活性随温度升高增大,与温度升高共同使
的去除率先迅速上升后上升缓慢,迅速上升段是催化剂活性随温度升高增大,与温度升高共同使 去除反应速率迅速增大,上升阶段缓慢主要是
去除反应速率迅速增大,上升阶段缓慢主要是____________ ;当反应温度高于 时,
时, 的去除率迅速下降的原因可能是
的去除率迅速下降的原因可能是_________ 。
(4)如图为利用肼 —空气燃料电池电解硫酸铜溶液的示意图。
—空气燃料电池电解硫酸铜溶液的示意图。
左图负极反应式为:___________ 。当上图阴极上放出2.24L气体 标准状况
标准状况 时,图中硫酸铜溶液的pH=
时,图中硫酸铜溶液的pH=______ (溶液体积变化忽略不计)。
(4)工业上生产尿素的化学方程式为:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6mol NH3和3mol CO2 。10min反应达到平衡,达到平衡时,c(NH3)=0.5mol·L-1。则10min内的平均反应速率υ(CO2)=
CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6mol NH3和3mol CO2 。10min反应达到平衡,达到平衡时,c(NH3)=0.5mol·L-1。则10min内的平均反应速率υ(CO2)=_______ mol·L-1·min-1。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3mol NH3,则此时反应的v正____ v逆(填“>”“<”或“=”)。
(1)已知N2(g)+O2(g)=2NO(g) ΔH =+180.5kJ·mol-1,N2(g)+3H2(g)
 2NH3(g)ΔH =-92.4kJ·mol-1,2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ·mol-1,写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为
2NH3(g)ΔH =-92.4kJ·mol-1,2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ·mol-1,写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)
 2NH3(g),在恒温恒压下判断该反应达到化学平衡状态的依据是
2NH3(g),在恒温恒压下判断该反应达到化学平衡状态的依据是A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2) (正)=v(H2) (逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)在有氧条件下,新型催化剂M能催化
 与
与 生成
生成 。将一定比例的
。将一定比例的 、
、 和
和 的混合气体,匀速通入装有催化剂M的反应器中反应(装置见图)。
的混合气体,匀速通入装有催化剂M的反应器中反应(装置见图)。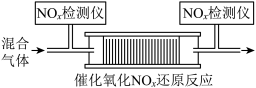
反应相同时间
 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后上升缓慢,迅速上升段是催化剂活性随温度升高增大,与温度升高共同使
的去除率先迅速上升后上升缓慢,迅速上升段是催化剂活性随温度升高增大,与温度升高共同使 去除反应速率迅速增大,上升阶段缓慢主要是
去除反应速率迅速增大,上升阶段缓慢主要是 时,
时, 的去除率迅速下降的原因可能是
的去除率迅速下降的原因可能是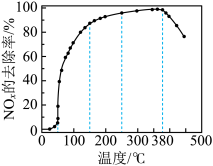
(4)如图为利用肼
 —空气燃料电池电解硫酸铜溶液的示意图。
—空气燃料电池电解硫酸铜溶液的示意图。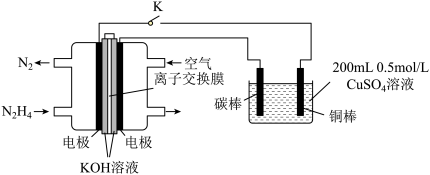
左图负极反应式为:
 标准状况
标准状况 时,图中硫酸铜溶液的pH=
时,图中硫酸铜溶液的pH=(4)工业上生产尿素的化学方程式为:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6mol NH3和3mol CO2 。10min反应达到平衡,达到平衡时,c(NH3)=0.5mol·L-1。则10min内的平均反应速率υ(CO2)=
CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6mol NH3和3mol CO2 。10min反应达到平衡,达到平衡时,c(NH3)=0.5mol·L-1。则10min内的平均反应速率υ(CO2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】研究碳氧化合物、氮氧化物、硫氧化合物等大气污染物的处理方法对缓解环境污染、能源危机具有重要意义。
(1)已知:①C(s)+O2(g) CO2(g) ΔH=-393.5 kJ/mol
CO2(g) ΔH=-393.5 kJ/mol
②N2(g)+O2(g) 2NO(g) ΔH=+180 kJ/mol
2NO(g) ΔH=+180 kJ/mol
则③C(s)+2NO(g) CO2(g)+N2(g)的ΔH=
CO2(g)+N2(g)的ΔH=_______ kJ/mol。
(2)用焦炭还原NO2的反应为2C(s)+2NO2(g) N2(g)+2CO2(g),向两个容积均为2 L,反应温度分别为T1℃、 T2℃的恒温恒容密闭容器中分别加入足量的焦炭和一定量的NO2,测得各容器中n(NO2)随反应时间t的变化情况如下图所示:
N2(g)+2CO2(g),向两个容积均为2 L,反应温度分别为T1℃、 T2℃的恒温恒容密闭容器中分别加入足量的焦炭和一定量的NO2,测得各容器中n(NO2)随反应时间t的变化情况如下图所示:
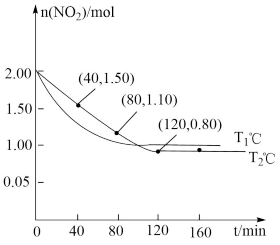
①T1___ T2(填“>”或“<”),该反应为____ 反应。(填“放热”或“吸热”)
②在T2℃下,120 min时达到平衡,则此段时间内用N2表示的平均反应速率v(N2)=________ mol•L-1•min-1。达到平衡时NO2的转化率为________ 。此温度下的化学平衡常数K=_____ 。
③一定条件下,达到平衡后,下列措施能提高NO2的转化率的是___________ 。
A.升高体系温度 B.减小体系压强
C.增加C的用量 D.将CO2从体系中分离出去
④T2℃时,反应达到平衡,120 min时,向容器中再加入焦炭和NO2各1 mol,在t时刻再次达到平衡,化学平衡常数K___________ 。(填“增大”“减小”或“不变”)。
(3)工业上消除氮氧化物的常用方法是SCR(选择性催化还原)脱硝法,反应原理为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH<0。
4N2(g)+6H2O(g) ΔH<0。
当反应温度过高时,会发生以下副反应:2NH3(g)+2O2(g) N2O(g)+3H2O(g)、4NH3(g)+5O2(g)
N2O(g)+3H2O(g)、4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。
4NO(g)+6H2O(g)。
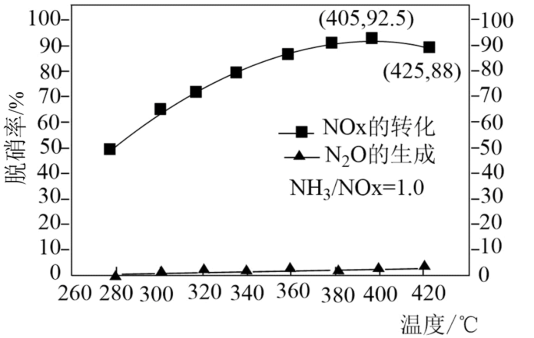
某科研小组通过系列实验,分析得出脱硝率与温度的关系如下图所示,当温度高于405℃后,脱硝率会逐渐减小,原因是_____________________________________ 。
(1)已知:①C(s)+O2(g)
 CO2(g) ΔH=-393.5 kJ/mol
CO2(g) ΔH=-393.5 kJ/mol②N2(g)+O2(g)
 2NO(g) ΔH=+180 kJ/mol
2NO(g) ΔH=+180 kJ/mol则③C(s)+2NO(g)
 CO2(g)+N2(g)的ΔH=
CO2(g)+N2(g)的ΔH=(2)用焦炭还原NO2的反应为2C(s)+2NO2(g)
 N2(g)+2CO2(g),向两个容积均为2 L,反应温度分别为T1℃、 T2℃的恒温恒容密闭容器中分别加入足量的焦炭和一定量的NO2,测得各容器中n(NO2)随反应时间t的变化情况如下图所示:
N2(g)+2CO2(g),向两个容积均为2 L,反应温度分别为T1℃、 T2℃的恒温恒容密闭容器中分别加入足量的焦炭和一定量的NO2,测得各容器中n(NO2)随反应时间t的变化情况如下图所示:
①T1
②在T2℃下,120 min时达到平衡,则此段时间内用N2表示的平均反应速率v(N2)=
③一定条件下,达到平衡后,下列措施能提高NO2的转化率的是
A.升高体系温度 B.减小体系压强
C.增加C的用量 D.将CO2从体系中分离出去
④T2℃时,反应达到平衡,120 min时,向容器中再加入焦炭和NO2各1 mol,在t时刻再次达到平衡,化学平衡常数K
(3)工业上消除氮氧化物的常用方法是SCR(选择性催化还原)脱硝法,反应原理为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) ΔH<0。
4N2(g)+6H2O(g) ΔH<0。当反应温度过高时,会发生以下副反应:2NH3(g)+2O2(g)
 N2O(g)+3H2O(g)、4NH3(g)+5O2(g)
N2O(g)+3H2O(g)、4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。
4NO(g)+6H2O(g)。某科研小组通过系列实验,分析得出脱硝率与温度的关系如下图所示,当温度高于405℃后,脱硝率会逐渐减小,原因是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示:(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)

(1)由图可知,决定反应速率的一步是_______ 。(填a、b、c……)
(2)下列关于工业合成氨的说法正确的是_______。
(3)请用平衡移动原理来解释在合成氨中及时分离出氨的原因_______ 。
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示 物质的量,
物质的量, %表示
%表示 的百分含量)。
的百分含量)。
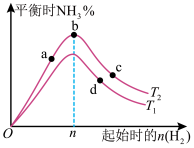
①图像中 和
和 的关系是:
的关系是:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②a、b、c、d四点所处的平衡状态中,反应物 的转化率最高的是
的转化率最高的是_______ (填字母)。
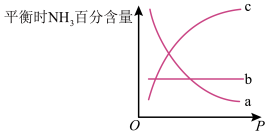
(5)其他条件不变,表示平衡时氨的百分含量随压强变化关系的曲线为_______ (填字母编号)。
(6)某温度下,向一个 的密闭容器中充入
的密闭容器中充入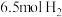 和
和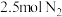 ,反应过程中对
,反应过程中对 的浓度进行检测,得到的数据如下表所示:
的浓度进行检测,得到的数据如下表所示:
此条件下该反应的化学平衡常数
_______ 。
(7)氨氧化法是工业生产中制取硝酸的主要途径。
已知:


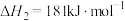

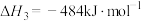
写出氨气催化氧化生成 和水蒸气的热化学方程式
和水蒸气的热化学方程式_______ 。

(1)由图可知,决定反应速率的一步是
(2)下列关于工业合成氨的说法正确的是_______。
A.因为 ,所以该反应一定能自发进行 ,所以该反应一定能自发进行 |
B.因为 ,所以该反应一定不能自发进行 ,所以该反应一定不能自发进行 |
| C.在高温下进行是为了提高反应物的平衡转化率 |
| D.使用催化剂不仅可以加快反应速率还可以降低反应所需的温度 |
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示
 物质的量,
物质的量, %表示
%表示 的百分含量)。
的百分含量)。
①图像中
 和
和 的关系是:
的关系是:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②a、b、c、d四点所处的平衡状态中,反应物
 的转化率最高的是
的转化率最高的是(5)其他条件不变,表示平衡时氨的百分含量随压强变化关系的曲线为

(6)某温度下,向一个
 的密闭容器中充入
的密闭容器中充入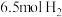 和
和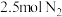 ,反应过程中对
,反应过程中对 的浓度进行检测,得到的数据如下表所示:
的浓度进行检测,得到的数据如下表所示:时间 | 5 | 10 | 15 | 20 | 25 | 30 |
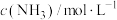 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |

(7)氨氧化法是工业生产中制取硝酸的主要途径。
已知:



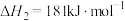

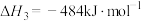
写出氨气催化氧化生成
 和水蒸气的热化学方程式
和水蒸气的热化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,相关反应的热化学方程式为:
ⅰ.CO(g)+2H2(g) CH3OH(g) ΔH=a kJ/mol;
CH3OH(g) ΔH=a kJ/mol;
ⅱ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=b kJ/mol;
CH3OH(g)+H2O(g) ΔH=b kJ/mol;
ⅲ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH=−c kJ/mol。
CO(g)+H2O(g) ΔH=−c kJ/mol。
回答下列问题:
(1)a=______ (用b、c表示),已知反应ⅱ在一定条件下可自发进行,则b______ (填“>”“<”或“=”)0。
(2)在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2与H2,在催化剂的作用下仅发生反应ⅲ。该反应达到平衡时,其他条件不变,通入CO2时,则v(正)___ (填“>”“<”或“=”)v(逆),平衡常数_______ (填“变大”“变小”或“不变”)。
(3)一定温度下,向体积为2L的恒容密闭容器中通入CO、H2、CH3OH,发生反应ⅰ,其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。
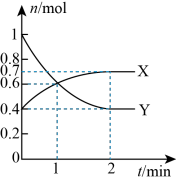
①Y为_____ (填化学式)。
②0~1min时v(CO)为_____ mol/(L·min)。
③该温度下,该反应的平衡常数Kc=______ 。
(4)工业上以 和
和 为原料可制备合成气(CO、H2),已知
为原料可制备合成气(CO、H2),已知 、
、 、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应
、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应

______ 。若该反应的 ,
, (
(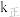 、
、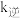 为速率常数,只与温度有关),平衡后降低温度,则
为速率常数,只与温度有关),平衡后降低温度,则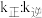
_______ (填“增大”“不变”或“减小”)。
(5)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cm△T计算获得。
①热量的测定:取0.5000mol/LNaOH溶液和0.5500mol/L盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,(c和 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
_____  。
。
②下列操作会使所测得的焓变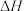 偏小的是
偏小的是______ 。
a.用等物质的量浓度的醋酸代替盐酸实验 b.量热装置绝热效果欠佳 c.NaOH溶液量多了
ⅰ.CO(g)+2H2(g)
 CH3OH(g) ΔH=a kJ/mol;
CH3OH(g) ΔH=a kJ/mol;ⅱ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=b kJ/mol;
CH3OH(g)+H2O(g) ΔH=b kJ/mol;ⅲ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=−c kJ/mol。
CO(g)+H2O(g) ΔH=−c kJ/mol。回答下列问题:
(1)a=
(2)在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2与H2,在催化剂的作用下仅发生反应ⅲ。该反应达到平衡时,其他条件不变,通入CO2时,则v(正)
(3)一定温度下,向体积为2L的恒容密闭容器中通入CO、H2、CH3OH,发生反应ⅰ,其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。
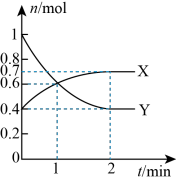
①Y为
②0~1min时v(CO)为
③该温度下,该反应的平衡常数Kc=
(4)工业上以
 和
和 为原料可制备合成气(CO、H2),已知
为原料可制备合成气(CO、H2),已知 、
、 、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应
、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应

 ,
, (
(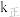 、
、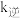 为速率常数,只与温度有关),平衡后降低温度,则
为速率常数,只与温度有关),平衡后降低温度,则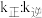
(5)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cm△T计算获得。
①热量的测定:取0.5000mol/LNaOH溶液和0.5500mol/L盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,(c和
 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
 。
。②下列操作会使所测得的焓变
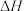 偏小的是
偏小的是a.用等物质的量浓度的醋酸代替盐酸实验 b.量热装置绝热效果欠佳 c.NaOH溶液量多了
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
Ⅰ.研究发现,以 和
和 为原料合成尿素的反应
为原料合成尿素的反应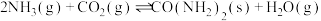
 ,分两步完成,其能量变化如下图甲所示:
,分两步完成,其能量变化如下图甲所示:
第一步: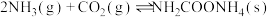

第二步: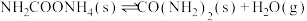

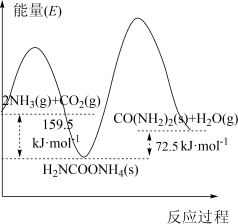
图甲
(1)合成尿素的决速反应是_________ 反应(填“第一步”或“第二步”),理由是_________ 。
(2)已知合成尿素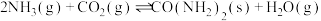
 的活化能Ea(逆)为
的活化能Ea(逆)为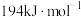 ,则该反应的活化能Ea(正)为
,则该反应的活化能Ea(正)为_________  该反应在
该反应在_________ (填“高温”、“低温”、“任意温度”)下可自发进行。
Ⅱ.以 和
和 催化重整制备合成气发生反应:
催化重整制备合成气发生反应: 。
。
(3)在一定条件下,在密闭容器中通入一定量的 和
和 ,
, 的平衡转化率随温度、压强的变化关系如下图乙所示。
的平衡转化率随温度、压强的变化关系如下图乙所示。
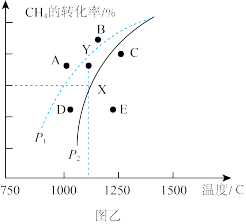
①若反应在恒温、恒压密闭容器中进行,下列叙述能说明反应达到平衡状态的是_________ (填序号)。
A.容器中混合气体的密度保持不变B.容器内CO与 的物质的量之比保持不变
的物质的量之比保持不变
C.反应速率: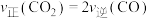 D.断裂
D.断裂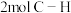 同时断裂
同时断裂 键
键
②由图乙可知,压强
_________  (填“>”、“<”或“=”,下同);压强为
(填“>”、“<”或“=”,下同);压强为 时,对应温度下Y点速率
时,对应温度下Y点速率
_________  。
。
③若在Y点时对反应容器升温的同时扩大容器体积使体系压强减小,重新达到新的平衡状态时,可能是图中:A、B、C、D、E点中的_________ 点。
(4)一定温度下,向容积不变的密闭容器中通入总压强为PkPa的等物质的量的 和
和 以及一定量的水蒸气(水蒸气不参与反应),达到平衡后总压强为1.48PkPa,
以及一定量的水蒸气(水蒸气不参与反应),达到平衡后总压强为1.48PkPa, 的转化率为60%,则该温度下的
的转化率为60%,则该温度下的
_________ (用含P的代数式表示,只列计算表达式;用平衡分压代替平衡浓度,已知气体分压 气体总压
气体总压 气体的物质的量分数)。
气体的物质的量分数)。
Ⅰ.研究发现,以
 和
和 为原料合成尿素的反应
为原料合成尿素的反应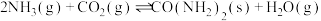
 ,分两步完成,其能量变化如下图甲所示:
,分两步完成,其能量变化如下图甲所示:第一步:
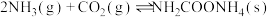

第二步:
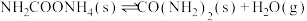


图甲
(1)合成尿素的决速反应是
(2)已知合成尿素
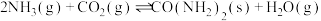
 的活化能Ea(逆)为
的活化能Ea(逆)为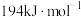 ,则该反应的活化能Ea(正)为
,则该反应的活化能Ea(正)为 该反应在
该反应在Ⅱ.以
 和
和 催化重整制备合成气发生反应:
催化重整制备合成气发生反应: 。
。(3)在一定条件下,在密闭容器中通入一定量的
 和
和 ,
, 的平衡转化率随温度、压强的变化关系如下图乙所示。
的平衡转化率随温度、压强的变化关系如下图乙所示。
①若反应在恒温、恒压密闭容器中进行,下列叙述能说明反应达到平衡状态的是
A.容器中混合气体的密度保持不变B.容器内CO与
 的物质的量之比保持不变
的物质的量之比保持不变C.反应速率:
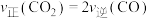 D.断裂
D.断裂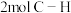 同时断裂
同时断裂 键
键②由图乙可知,压强

 (填“>”、“<”或“=”,下同);压强为
(填“>”、“<”或“=”,下同);压强为 时,对应温度下Y点速率
时,对应温度下Y点速率
 。
。③若在Y点时对反应容器升温的同时扩大容器体积使体系压强减小,重新达到新的平衡状态时,可能是图中:A、B、C、D、E点中的
(4)一定温度下,向容积不变的密闭容器中通入总压强为PkPa的等物质的量的
 和
和 以及一定量的水蒸气(水蒸气不参与反应),达到平衡后总压强为1.48PkPa,
以及一定量的水蒸气(水蒸气不参与反应),达到平衡后总压强为1.48PkPa, 的转化率为60%,则该温度下的
的转化率为60%,则该温度下的
 气体总压
气体总压 气体的物质的量分数)。
气体的物质的量分数)。
您最近一年使用:0次



