反应2NO+Cl2=2NOCl,在295K时,其反应物浓度与反应速率关系的数据如下:
注:①反应物浓度与反应速率关系式为v(Cl2)=k·cm(NO)·cn(Cl2)(式中速率常数 ,其中Ea为活化能,A、R均为大于0的常数,T为温度);②反应级数是反应的速率方程式中各反应物浓度的指数之和。下列说法不正确的是
,其中Ea为活化能,A、R均为大于0的常数,T为温度);②反应级数是反应的速率方程式中各反应物浓度的指数之和。下列说法不正确的是
| c(NO)/(mol·L-1) | c(Cl2)/(mol·L-1) | v(Cl2)/(mol·L-1·s-1) | |
| ① | 0.100 | 0.100 | 8.0×10-3 |
| ② | 0.500 | 0.100 | 2.0×10-1 |
| ③ | 0.100 | 0.500 | 4.0×10-2 |
 ,其中Ea为活化能,A、R均为大于0的常数,T为温度);②反应级数是反应的速率方程式中各反应物浓度的指数之和。下列说法不正确的是
,其中Ea为活化能,A、R均为大于0的常数,T为温度);②反应级数是反应的速率方程式中各反应物浓度的指数之和。下列说法不正确的是| A.m=2,n=1,反应级数为3级 |
| B.当c(NO)=0.200mol·L-1,c(Cl2)=0.300mol·L-1,v(NO)=0.192mol·L-1·s-1 |
| C.加入催化剂可以改变反应途径,也可以增大速率常数k,而加快反应速率 |
| D.升高温度,可以增大反应的活化能Ea,从而使速率常数k增大 |
更新时间:2024-01-31 19:37:16
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】金表面发生分解反应: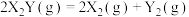 ,其速率方程为
,其速率方程为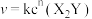 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
下列叙述不正确的是
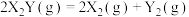 ,其速率方程为
,其速率方程为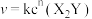 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:t/min c/(mol·L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| X2Y | 0.100 | 0.040 | 0.020 | 0 | ||
| X2 | 0 | 0.020 | ||||
| Y2 | 0 | 0.020 |
| A.提高反应物浓度,反应速率不变 |
B. |
C.其他条件不变,若 起始浓度为 起始浓度为 ,则反应物浓度减半所需时间为 ,则反应物浓度减半所需时间为 |
D.当升高温度,反应 时 时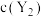 可能小于 可能小于 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定温度时,向容积为 2 L 的密闭容器中充入一定量的 SO2(g)和 O2(g),发生反应:2SO2(g)+ O2(g) 2SO3(g) △H = - 196 kJ/mol。一段时间后反应达到平衡状态,反应过程中测定的部分数据如表所示。
2SO3(g) △H = - 196 kJ/mol。一段时间后反应达到平衡状态,反应过程中测定的部分数据如表所示。
下列说法不正确的是
 2SO3(g) △H = - 196 kJ/mol。一段时间后反应达到平衡状态,反应过程中测定的部分数据如表所示。
2SO3(g) △H = - 196 kJ/mol。一段时间后反应达到平衡状态,反应过程中测定的部分数据如表所示。| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 2 | 1 |
| 5 | 1.2 | |
| 10 | 0.4 | |
| 15 | 0.8 |
下列说法不正确的是
| A.前 5 min 的平均反应速率为υ(SO2) = 0.08 mol/(L·min) |
| B.保持温度不变,向平衡后的容器中再充入 0.2 mol SO2(g)和 0.2 mol SO3(g)时,υ正 > υ逆 |
| C.保持其他条件不变,若起始时向容器中充入 2 mol SO3(g),达到平衡状态时吸收 78.4 kJ的热量 |
| D.相同温度下,起始时向容器中充入 1.5 mol SO3(g),达到平衡状态时 SO3 的转化率为 40% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在一定温度下,将气体X与气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X( g)+Y( g)⇌2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法正确的是( )
| t∕min | 2 | 4 | 7 | 9 |
| n(Y)∕mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应前4min的平均反应速率υ(Z)=0.0125mol•L-1•min-1 |
| B.其他条件不变,降低温度,反应达到新平衡前υ(逆)>υ(正) |
| C.其他条件不变,再向体系中冲入1L氦气,使体系压强增大,则υ(逆)与υ(正)同等程度增大 |
| D.该温度下此反应的平衡常数K=1.44 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列操作能达到实验目的的是
| 选项 | 目的 | 实验操作 |
| A | 探究温度对化学平衡的影响 | 加热0.5mol·L-1CuCl2溶液 |
| B | 证明干燥的氯气不具有漂白性 | 将干燥的氯气通入盛有红色鲜花的集气瓶中 |
| C | 比较AgBr和AgCl的Ksp大小 | 向NaCl和NaBr的混合溶液中逐滴加入少量AgNO3溶液 |
| D | 探究浓度对反应速率的影响 | 向2支分别盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】探究 反应速率的影响因素,有关实验数据如下表所示:
反应速率的影响因素,有关实验数据如下表所示:
下列说法不正确的是
 反应速率的影响因素,有关实验数据如下表所示:
反应速率的影响因素,有关实验数据如下表所示:| 编号 | 温度/℃ | 酸性 溶液 溶液 |  溶液 溶液 |  的体积 的体积(mL) |  溶液褪色平均时间/min 溶液褪色平均时间/min | ||
| 体积/mL | 浓度/( ) ) | 体积/mL | 浓度/( ) ) | ||||
| 1 | 25 | 4 | 0.1 | 8 | 0.2 | 8 | 12 |
| 2 | 80 | 2 | 0.1 | 8 | 0.2 | a | b |
| 3 | 25 | 2 | 0.1 | 8 | 0.2 | 10 | c |
| A.a=10,b<c,6<c<12 |
B.可通过比较收集相同体积的 所消耗的时间来判断反应速率的快慢 所消耗的时间来判断反应速率的快慢 |
C.用 表示该反应速率,v(实验1)为 表示该反应速率,v(实验1)为 |
D.实验时可依次向试管中加入酸性 溶液、 溶液、 溶液和水 溶液和水 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列实验操作正确且能达到目的的是
| 选项 | 目的 | 操作 |
| A. | 根据溶液中既含I2又含I-的实验事实判断该反应是可逆反应 | 取5mL0.1mol/LFeCl3溶液,滴加0.1mol/LKI溶液1mL,充分反应 |
| B. | 探究浓度对反应速率的影响 | 向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液,观察实验现象 |
| C. | 证明氧化性:Fe3+>I2 | 向黄色的Fe(NO3)3溶液中滴加氢碘酸 |
| D. | 证明非金属性:C>Si | 用SiO2与焦炭在高温条件下制备粗硅 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
| A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.活化分子间所发生的碰撞为有效碰撞 |
| D.升高温度能使化学反应速率增大的主要原因是增加了反应物中活化分子的百分数 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】对于合成氨反应N2(g)+3H2(g) 2NH3(g),恒温条件下,向某一2L的密闭容器中充入1molN2和
2NH3(g),恒温条件下,向某一2L的密闭容器中充入1molN2和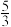 molH2,经10s达到平衡,平衡后压强为初始压强的
molH2,经10s达到平衡,平衡后压强为初始压强的 。则下列说法正确的是
。则下列说法正确的是
 2NH3(g),恒温条件下,向某一2L的密闭容器中充入1molN2和
2NH3(g),恒温条件下,向某一2L的密闭容器中充入1molN2和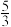 molH2,经10s达到平衡,平衡后压强为初始压强的
molH2,经10s达到平衡,平衡后压强为初始压强的 。则下列说法正确的是
。则下列说法正确的是| A.若要提高N2的转化率同时加快反应速率,可采取的措施有:缩小体积、充入N2、降低温度 |
| B.若该反应的平衡常数发生变化,平衡不一定移动 |
| C.保持温度和压强不变,再向容器中充入2 molN2,此时v正=v逆 |
| D.10s 内,v(NH3)=2mol/(L·s) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】根据下列实验操作和现象所得到的结论不 正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向AgNO3溶液中加入过量的0.1mol•L-1的NaCl溶液,产生白色沉淀。再滴加几滴NaBr溶液,出现浅黄色沉淀 | Ksp(AgBr)<Ksp(AgCl) |
| B | 向a、b两试管中均加入4mL0.01mol•L-1KMnO4溶液和2mL0.01mol•L-1H2C2O4溶液。再向a试管内加入少量MnSO4固体,a中溶液褪色较快 | MnSO4可能是KMnO4和H2C2O4溶反应的催化剂 |
| C | 向饱和NaHCO3溶液中滴加饱和CaCl2溶液,先有白色沉淀产生,后放出无色气泡 | Ca2+与CO 结合促进HCO 结合促进HCO 的电离,溶液中H+浓度增大,与HCO 的电离,溶液中H+浓度增大,与HCO 反应产生CO2 反应产生CO2 |
| D | 向滴加有酚酞的氨水中加入蒸馏水,溶液的红色变浅 | 溶液中c(H+)、c(OH-)浓度均减小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】催化氧化乳酸乙酯制备丙酮酸乙酯,一种可能的反应机理如图所示(其中,—Me表示 、—Et表示
、—Et表示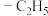 ):
):
 、—Et表示
、—Et表示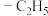 ):
):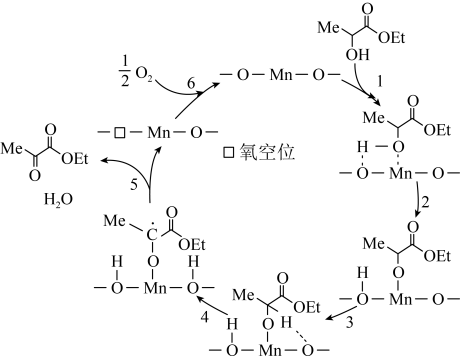
| A.反应过程中,Mn元素的化合价不发生变化 |
B.若不提供 ,则体系中也可产生丙酮酸乙酯 ,则体系中也可产生丙酮酸乙酯 |
C.理论上,消耗 可生成 可生成 丙酮酸乙酯 丙酮酸乙酯 |
D.若提供 ,则产物中含 ,则产物中含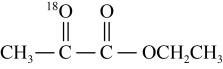 |
您最近一年使用:0次


 2NH3(g)
2NH3(g)  还原为
还原为 ,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是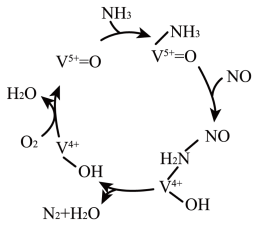
 价电子排布式为
价电子排布式为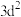 ,未成对电子数是2
,未成对电子数是2 为该反应的中间体
为该反应的中间体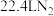 ,转移电子总数为
,转移电子总数为


