常温下,根据表中的几种物质的电离平衡常数回答下列问题:
(1)下列四种离子结合质子能力由大到小的顺序是_____ (填序号)。
a. b.
b. c.
c. d.
d.
(2)下列反应不能发生的是___________ (填序号)。
a.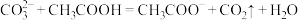
b.
C.
d.
(3)反应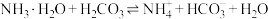 的平衡常数
的平衡常数
________ 。
| 弱酸 |  |  |  | HClO |
| 电离平衡常数 |  | 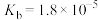 | 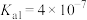 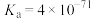 | 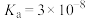 |
a.
 b.
b. c.
c. d.
d.
(2)下列反应不能发生的是
a.
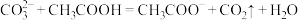
b.

C.

d.

(3)反应
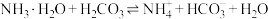 的平衡常数
的平衡常数
更新时间:2024-02-04 09:17:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向0.2mol/LBa(OH)2溶液中滴加0.1mol/L盐酸,测定导电率的变化如图所示,回答下列问题:

(1)写出Ba(OH)2的电离方程式为___________ 。
(2)A—B段,发生的离子反应方程式是___________ 。
(3)B点恰好完全反应,此时溶液中存在的微粒有H2O、___________ 。
(4)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同的是___________ 。
A.Ba(OH)2和H2SO4 B.NaOH和H2SO4 C.Ba(OH)2与HNO3

(1)写出Ba(OH)2的电离方程式为
(2)A—B段,发生的离子反应方程式是
(3)B点恰好完全反应,此时溶液中存在的微粒有H2O、
(4)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同的是
A.Ba(OH)2和H2SO4 B.NaOH和H2SO4 C.Ba(OH)2与HNO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】四个试剂瓶中分别盛有 溶液、
溶液、 溶液、
溶液、 溶液和
溶液和 溶液,就如何检验这四种溶液分别做如下探究。
溶液,就如何检验这四种溶液分别做如下探究。
探究过程:分别取四种溶液各 于四支试管中,做下列实验。
于四支试管中,做下列实验。
(1)在四支试管中分别滴入稀硝酸,依据___________ 现象能检测出的物质是___________ 其离子方程式为___________ 。
(2)在剩余三支试管中分别滴入 溶液,依据
溶液,依据___________ 现象能检测出的物质是___________ ,其离子方程式为___________ 。
(3)在剩余两支试管中分别滴入___________ 溶液,依据___________ 现象能检测出的物质是___________ ,离子方程式为___________ 。
 溶液、
溶液、 溶液、
溶液、 溶液和
溶液和 溶液,就如何检验这四种溶液分别做如下探究。
溶液,就如何检验这四种溶液分别做如下探究。探究过程:分别取四种溶液各
 于四支试管中,做下列实验。
于四支试管中,做下列实验。(1)在四支试管中分别滴入稀硝酸,依据
(2)在剩余三支试管中分别滴入
 溶液,依据
溶液,依据(3)在剩余两支试管中分别滴入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有下列10种物质:
①液态HCl、② 固体、③NaCl固体、④
固体、③NaCl固体、④ 气体、⑤蔗糖溶液、⑥
气体、⑤蔗糖溶液、⑥ 粉末、⑦氢氧化铁胶体、⑧氨水、⑨熔融
粉末、⑦氢氧化铁胶体、⑧氨水、⑨熔融 、⑩液氨
、⑩液氨
(1)上述10种物质中属于电解质___________ ,非电解质___________ ,能导电的___________ (填序号)
(2)向⑦中逐滴加①的水溶液至过量,看到的现象___________ 。
(3)上述10种物质中有两种物质在水溶液中发生反应的离子方程式为 ,则该反应的化学方程式为
,则该反应的化学方程式为___________ 。
(4)少量的④与足量⑥的溶液反应的离子方程式___________ 。
(5)⑥的溶液与少量②的溶液反应的离子方程式___________ 。
(6)在一定温度下,向电解质溶液中加入新物质时溶液的导电能力可能发生变化,实验过程中电流(I)随所加新物质的质量(m)变化的曲线如图所示。

下列各项中与A图变化趋势一致的是___________ (填字母,下同),与B图变化趋势一致的是___________ ,与C图变化趋势一致的是___________ 。
a.向 溶液中滴入
溶液中滴入 溶液至过量
溶液至过量
b.向 溶液中滴入氨水至过量
溶液中滴入氨水至过量
c.向澄清石灰水中通入 至过量
至过量
d.向 溶液中逐渐加入适量NaOH固体
溶液中逐渐加入适量NaOH固体
e.氢氧化钙溶液中逐滴加入碳酸氢铵至过量
f.硫酸溶液中逐滴加入适量氯化钡固体
①液态HCl、②
 固体、③NaCl固体、④
固体、③NaCl固体、④ 气体、⑤蔗糖溶液、⑥
气体、⑤蔗糖溶液、⑥ 粉末、⑦氢氧化铁胶体、⑧氨水、⑨熔融
粉末、⑦氢氧化铁胶体、⑧氨水、⑨熔融 、⑩液氨
、⑩液氨(1)上述10种物质中属于电解质
(2)向⑦中逐滴加①的水溶液至过量,看到的现象
(3)上述10种物质中有两种物质在水溶液中发生反应的离子方程式为
 ,则该反应的化学方程式为
,则该反应的化学方程式为(4)少量的④与足量⑥的溶液反应的离子方程式
(5)⑥的溶液与少量②的溶液反应的离子方程式
(6)在一定温度下,向电解质溶液中加入新物质时溶液的导电能力可能发生变化,实验过程中电流(I)随所加新物质的质量(m)变化的曲线如图所示。

下列各项中与A图变化趋势一致的是
a.向
 溶液中滴入
溶液中滴入 溶液至过量
溶液至过量b.向
 溶液中滴入氨水至过量
溶液中滴入氨水至过量c.向澄清石灰水中通入
 至过量
至过量d.向
 溶液中逐渐加入适量NaOH固体
溶液中逐渐加入适量NaOH固体e.氢氧化钙溶液中逐滴加入碳酸氢铵至过量
f.硫酸溶液中逐滴加入适量氯化钡固体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学课外活动小组欲制取纯Na2CO3溶液并讨论实验过程中的相关问题。可供选择的试剂有:
A.大理石 B.盐酸 C.氢氧化钠溶液 D.澄清石灰水
三名同学设计的制备纯Na2CO3的溶液的实验方案的反应流程分别如下:
甲:NaOH溶液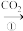 Na2CO3溶液
Na2CO3溶液
乙:NaOH溶液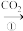 NaHCO3溶液
NaHCO3溶液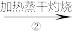 Na2CO3固体
Na2CO3固体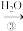 Na2CO3溶液
Na2CO3溶液
丙:NaOH溶液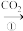 NaHCO3溶液
NaHCO3溶液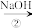 Na2CO3溶液
Na2CO3溶液
(1)请指出甲、乙两方案的主要缺点:
甲方案:___________ ;
乙方案:___________ 。
(2)若采用丙方案制取纯Na2CO3溶液,其实验的关键是:___________ 。
(3)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3,乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学___________ (填“能”或“不能”)达到实验目的:若能,请说明计算所需的数据;若不能,请简要说明理由;___________ 。
(4)已知物质的量浓度均为0.10mol/L的NaHCO3、Na2CO3和Na2S溶液pH如下:
①Na2CO3水溶液呈碱性的原因是___________ (用离子方程式表示)。NaHCO3溶液中滴加酚酞溶液显___________ 色,原因是___________ ;微热溶液颜色变深,可能的原因是___________ (结合离子方程式说明)。
②从表中数据可知,K2CO3溶液中c(CO )
)___________ K2S溶液中的c(S2-)(填“>”“<”或“=”)。
A.大理石 B.盐酸 C.氢氧化钠溶液 D.澄清石灰水
三名同学设计的制备纯Na2CO3的溶液的实验方案的反应流程分别如下:
甲:NaOH溶液
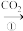 Na2CO3溶液
Na2CO3溶液乙:NaOH溶液
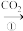 NaHCO3溶液
NaHCO3溶液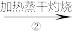 Na2CO3固体
Na2CO3固体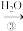 Na2CO3溶液
Na2CO3溶液丙:NaOH溶液
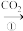 NaHCO3溶液
NaHCO3溶液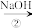 Na2CO3溶液
Na2CO3溶液(1)请指出甲、乙两方案的主要缺点:
甲方案:
乙方案:
(2)若采用丙方案制取纯Na2CO3溶液,其实验的关键是:
(3)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3,乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学
(4)已知物质的量浓度均为0.10mol/L的NaHCO3、Na2CO3和Na2S溶液pH如下:
| 溶液 | NaHCO3 | Na2CO3 | Na2S |
| pH | 8.3 | 11.6 | 12.5 |
①Na2CO3水溶液呈碱性的原因是
②从表中数据可知,K2CO3溶液中c(CO
 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化合物①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONH4、⑥CH3COOH、⑦NH3·H2O,回答:
(1)NH4Cl溶液显___________ 性。
(2)常温下,将pH=12的NaOH和氨水分别加水稀释100倍后,稀释后NaOH的pH___________ 10,氨水的pH___________ 10(填“>”“<”或“=”)
(3)常温下,pH=10的CH3COONa溶液中,水电离出来的c(OH-)为___________ mol/L,在pH=3的CH3COOH溶液中水电离出来的c(H+)为___________ mol/L。
(4)等物质的量浓度的④NH4Cl、⑤CH3COONH4、⑦NH3·H2O溶液中 浓度由大到小的顺序是
浓度由大到小的顺序是___________ (填序号)
(5)某学生用酚酞做指示剂,用标准NaOH溶液测定未知浓度的盐酸溶液,完成填空:滴定终点溶液颜色的变化是___________ 。若滴定中锥形瓶摇荡剧烈,使溶液溅出,则所测浓度___________ 。(填偏大、偏小或无影响)
(1)NH4Cl溶液显
(2)常温下,将pH=12的NaOH和氨水分别加水稀释100倍后,稀释后NaOH的pH
(3)常温下,pH=10的CH3COONa溶液中,水电离出来的c(OH-)为
(4)等物质的量浓度的④NH4Cl、⑤CH3COONH4、⑦NH3·H2O溶液中
 浓度由大到小的顺序是
浓度由大到小的顺序是(5)某学生用酚酞做指示剂,用标准NaOH溶液测定未知浓度的盐酸溶液,完成填空:滴定终点溶液颜色的变化是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】分25℃时,向10 mL 0.1 mol·L-1NH4HSO4溶液中逐滴滴入0.1 mol·L-1NaOH溶液,溶液的pH与NaOH溶液体积关系如右图所示:

(1)用电离方程式表示P点pH<7的原因是________ 。
(2)M、Q两点中,水的电离程度较大的是________ 点。
(3)下列关系中,正确的是________ 。
a.M点c(Na+)>c(NH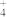 )
)
b.N点c(NH )+c(Na+)=2c(SO
)+c(Na+)=2c(SO )
)
c.Q点c(NH )+c(NH3·H2O)=c(Na+)
)+c(NH3·H2O)=c(Na+)

(1)用电离方程式表示P点pH<7的原因是
(2)M、Q两点中,水的电离程度较大的是
(3)下列关系中,正确的是
a.M点c(Na+)>c(NH
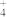 )
)b.N点c(NH
 )+c(Na+)=2c(SO
)+c(Na+)=2c(SO )
)c.Q点c(NH
 )+c(NH3·H2O)=c(Na+)
)+c(NH3·H2O)=c(Na+)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某实验小组利用虚拟感应器技术探究1 mol⋅L 的碳酸钠溶液滴定10.00 mL 1
的碳酸钠溶液滴定10.00 mL 1 的盐酸溶液过程中离子浓度变化。已知:25℃时,
的盐酸溶液过程中离子浓度变化。已知:25℃时, 的
的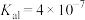 ,
,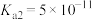 ;
;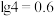 。回答下列问题:
。回答下列问题:
(1)碳酸钠溶液的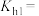
______  。
。
(2)用浓盐酸配制滴定实验需要的1 的盐酸溶液80mL,需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需要
的盐酸溶液80mL,需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需要____________ 。配制完成后.需用_______ 量取10.00 mL 1  的盐酸溶液于锥形瓶中。
的盐酸溶液于锥形瓶中。
(3)滴定时碳酸钠溶液稍过量后,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中 的逸出),如图所示:
的逸出),如图所示:

①由分析可知,
______ mL,曲线Ⅱ是______ 浓度变化曲线。
②图中B3和C2溶液中水的电离程度较大的是______ ,D点
______ 。
 的碳酸钠溶液滴定10.00 mL 1
的碳酸钠溶液滴定10.00 mL 1 的盐酸溶液过程中离子浓度变化。已知:25℃时,
的盐酸溶液过程中离子浓度变化。已知:25℃时, 的
的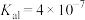 ,
,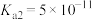 ;
; 。回答下列问题:
。回答下列问题:(1)碳酸钠溶液的
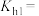
 。
。(2)用浓盐酸配制滴定实验需要的1
 的盐酸溶液80mL,需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需要
的盐酸溶液80mL,需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需要 的盐酸溶液于锥形瓶中。
的盐酸溶液于锥形瓶中。(3)滴定时碳酸钠溶液稍过量后,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中
 的逸出),如图所示:
的逸出),如图所示:
①由分析可知,

②图中B3和C2溶液中水的电离程度较大的是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.在常温下,0. lmol/L一元酸HB溶液的pH=3,回答下列问题:
(1)HB在水溶液中的电离平衡常数Ka≈_______ 。
(2)常温下,有c(H+)相同、体积相同的上述酸HB和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示HB)

II.常温下,几种弱酸的电离平衡常数如下表所示,回答下列问题:
(3)酸性最强的为_______ 。
(4)将少量的CO2通入NaC1O溶液中,反应的离子方程式:_______ 。
(1)HB在水溶液中的电离平衡常数Ka≈
(2)常温下,有c(H+)相同、体积相同的上述酸HB和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

II.常温下,几种弱酸的电离平衡常数如下表所示,回答下列问题:
| 化学式 | HCOOH | H2CO3 | HCN | HClO |
| 电离平衡常数 | K=1.8×10-4 | K1=4.3×10-7 K2= 5.6×10-11 | K=4.9×10-10 | K=3.0×10-8 |
(3)酸性最强的为
(4)将少量的CO2通入NaC1O溶液中,反应的离子方程式:
您最近一年使用:0次



