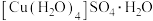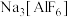下列事实中,不能能用勒夏特列原理解释的是
| A.实验室可用浓氨水和氢氧化钠固体快速制取氨气 |
| B.工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 |
C.对于2HI(g)  H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
| D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
更新时间:2024-02-09 09:48:35
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.向Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| B.实验室保存FeSO4溶液时,常加入少量铁粉 |
C.重铬酸钾溶液中存在:Cr2O (橙色)+H2O⇌2CrO (橙色)+H2O⇌2CrO (黄色)+2H+,若滴加少量NaOH溶液,溶液由橙色变黄色 (黄色)+2H+,若滴加少量NaOH溶液,溶液由橙色变黄色 |
| D.实验室用排饱和食盐水的方法收集Cl2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列不能用勒沙特列原理解释的是
| A.SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| B.棕红色NO2加压后颜色先变深后变浅 |
| C.Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| D.高压比常压有利于NH3的合成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下表是几种弱酸常温下的电离平衡常数:
则下列说法中不正确的是( )
| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
| A.碳酸的酸性强于氢硫酸 |
| B.多元弱酸的酸性主要由第一步电离决定 |
| C.常温下,加水稀释醋酸,电离平衡常数增大 |
| D.向弱酸溶液中加少量NaOH溶液,电离平衡常数不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在醋酸溶液中,CH3COOH的电离达到平衡状态的标志是
| A.c(H+)=c(CH3COO-) |
| B.溶液中:c(H+)>c(OH-) |
| C.CH3COOH分子的浓度不再变化 |
| D.溶液中同时存在H+、CH3COO-、OH-、CH3COOH、H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列叙述正确的是
A.用水稀释 的氨水,则溶液中 的氨水,则溶液中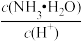 减小 减小 |
B.中和等体积、等 的盐酸和醋酸,消耗 的盐酸和醋酸,消耗 的物质的量相等 的物质的量相等 |
| C.在等体积等浓度的盐酸和醋酸中分别加入等质量的相同锌粒,随着反应的进行,醋酸不断电离出H+,反应速率比盐酸大 |
D.两种氨水的 分别为a和a+1,物质的量浓度分别为c1和c2,则c2<10c1 分别为a和a+1,物质的量浓度分别为c1和c2,则c2<10c1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列不能形成配位键的组合是( )。
| A.Ag+、NH3 | B.H2O、H+ |
| C.Co3+、CO | D.Ag+、H+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】许多过渡金属离子对多种配体有很强的结合力,能形成种类繁多的配合物。下列说法不正确的是
| A.向配合物[CoBr(NH3)5]SO4的溶液中加入BaCl2溶液,有白色沉淀生成 |
| B.配离子[Cu(H2O)6]2+中的Cu2+提供接受孤电子对的空轨道,H2O中的O提供孤电子对 |
| C.配合物[Cu(NH3)4]SO4·H2O的配体为NH3和H2O |
| D.配合物[Ag(NH3)2]OH的配位数为2 |
您最近一年使用:0次

 HBr + HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr + HBrO,当加入AgNO3溶液后,溶液颜色变浅