某兴趣小组用铬铁矿( ,含
,含 等杂质)为主要原料制备重铬酸钾
等杂质)为主要原料制备重铬酸钾 晶体,流程如下:
晶体,流程如下:

已知: 中
中 元素为
元素为 价;
价; 与
与 高温生成可溶于水的
高温生成可溶于水的 ;
; 酸性条件下能转化为
酸性条件下能转化为 。
。
回答下列问题:
(1)“焙烧”时,除生成 和
和 外,还生成一种无色无味的气体,该反应的化学方程式为
外,还生成一种无色无味的气体,该反应的化学方程式为___________ 。
(2)实验室进行“操作1”用到的玻璃仪器有:烧杯、___________ 。
(3)“晶体X”的化学式为___________ 。
(4)交警查酒驾所用检测仪器的工作原理为:
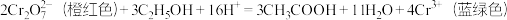
该反应中,还原剂为___________ ;反应消耗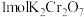 时,转移电子的物质的量为
时,转移电子的物质的量为___________  。
。
(5)“结晶”时,为得到杂质较少的 粗产品,请结合下图从下列选项中选出合理的操作并排序
粗产品,请结合下图从下列选项中选出合理的操作并排序___________ (填字母)。
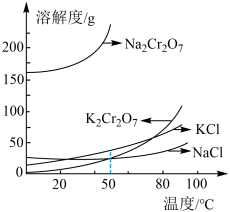
a. 蒸发溶剂 b.
蒸发溶剂 b. 蒸发溶剂 c.过滤 d.冷却至室温
蒸发溶剂 c.过滤 d.冷却至室温
e.蒸发至溶液出现晶膜,停止加热
 ,含
,含 等杂质)为主要原料制备重铬酸钾
等杂质)为主要原料制备重铬酸钾 晶体,流程如下:
晶体,流程如下:
已知:
 中
中 元素为
元素为 价;
价; 与
与 高温生成可溶于水的
高温生成可溶于水的 ;
; 酸性条件下能转化为
酸性条件下能转化为 。
。回答下列问题:
(1)“焙烧”时,除生成
 和
和 外,还生成一种无色无味的气体,该反应的化学方程式为
外,还生成一种无色无味的气体,该反应的化学方程式为(2)实验室进行“操作1”用到的玻璃仪器有:烧杯、
(3)“晶体X”的化学式为
(4)交警查酒驾所用检测仪器的工作原理为:
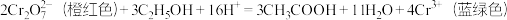
该反应中,还原剂为
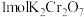 时,转移电子的物质的量为
时,转移电子的物质的量为 。
。(5)“结晶”时,为得到杂质较少的
 粗产品,请结合下图从下列选项中选出合理的操作并排序
粗产品,请结合下图从下列选项中选出合理的操作并排序
a.
 蒸发溶剂 b.
蒸发溶剂 b. 蒸发溶剂 c.过滤 d.冷却至室温
蒸发溶剂 c.过滤 d.冷却至室温e.蒸发至溶液出现晶膜,停止加热
更新时间:2024-02-02 15:06:59
|
相似题推荐
【推荐1】磷及其化合物在工农业生产中具有重要用途。回答下列问题:
(1)如图1所示为提纯白磷样品(含惰性杂质)的工艺流程。过程Ⅰ的化学方程式为_______ 。过程Ⅲ中,还原剂与氧化剂的物质的量之比为_______ 。

(2)磷酸钒锂/碳复合材料[Li3V2(PO4)3/C]是一种十分具有商业潜力的电极材料,它的一种制备流程如图2所示:

①草酸(H2C2O4)是二元弱酸,草酸氢钾(KHC2O4)溶液呈酸性,在0.1 mol/L KHC2O4溶液中,离子的物质的量浓度由大到小的顺序为_______ 。
②A的主要成分为V2(C2O4)3。H2C2O4溶液与V2O5反应生成A的化学方程式为_______ 。
③流程中加入碳球的作用是_______ 。
④已知常温下,Li2CO3微溶于水,LiHCO3可溶于水。工业级Li2CO3中含有少量难溶于水且与CO2不反应的杂质。提纯工业级Li2CO3的实验方案是:将工业级Li2CO3与水混合,_______ ,然后过滤,得到LiHCO3溶液;控温加热使LiHCO3分解形成Li2CO3沉淀,再过滤、洗涤、干燥,得到Li2CO3纯品。
⑤锂离子电池是一种二次电池。若用 和
和 作电极,放电时的电池总反应为
作电极,放电时的电池总反应为 。电池放电时,正极的电极反应式为
。电池放电时,正极的电极反应式为_______ 。
(1)如图1所示为提纯白磷样品(含惰性杂质)的工艺流程。过程Ⅰ的化学方程式为

(2)磷酸钒锂/碳复合材料[Li3V2(PO4)3/C]是一种十分具有商业潜力的电极材料,它的一种制备流程如图2所示:

①草酸(H2C2O4)是二元弱酸,草酸氢钾(KHC2O4)溶液呈酸性,在0.1 mol/L KHC2O4溶液中,离子的物质的量浓度由大到小的顺序为
②A的主要成分为V2(C2O4)3。H2C2O4溶液与V2O5反应生成A的化学方程式为
③流程中加入碳球的作用是
④已知常温下,Li2CO3微溶于水,LiHCO3可溶于水。工业级Li2CO3中含有少量难溶于水且与CO2不反应的杂质。提纯工业级Li2CO3的实验方案是:将工业级Li2CO3与水混合,
⑤锂离子电池是一种二次电池。若用
 和
和 作电极,放电时的电池总反应为
作电极,放电时的电池总反应为 。电池放电时,正极的电极反应式为
。电池放电时,正极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。

I.实验室制取氨气。
(1)图1装置中生成 的化学方程式为
的化学方程式为______________ 。检验圆底烧瓶中已收集满氨气的方法是_______ 。
Ⅱ.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是__________ ;有同学认为需要在无水硫酸铜的后面再接一个装有 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是______ 。
(3)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是__________ (填字母)。

(4)实验中观察到a中 粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为________ ;氨与氧气在高温、催化剂作用下反应的化学方程式为________ 。
(5)若向a中通入标准状况下 的氨气,最终得到铜的质量为
的氨气,最终得到铜的质量为_____ g(保留小数点后一位)。

I.实验室制取氨气。
(1)图1装置中生成
 的化学方程式为
的化学方程式为Ⅱ.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(3)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是

(4)实验中观察到a中
 粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为(5)若向a中通入标准状况下
 的氨气,最终得到铜的质量为
的氨气,最终得到铜的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫及其部分化合物的“价类二维图”如下图所示,回答下列问题:
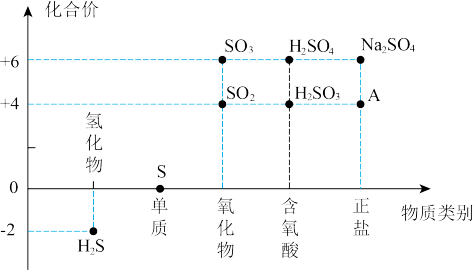
(1)向A的水溶液中滴加NaOH溶液并加热,产生一种能使润湿的红色石蕊试纸变蓝的气体,则A物质的化学式为___________ ,含有的化学键类型为___________ 。
(2)某实验小组为了验证固体A中含有碳酸钠杂质,选用下列装置进行实验:
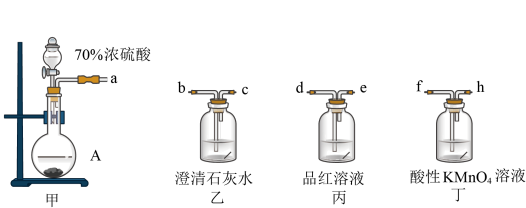
①实验装置的连接顺序为___________ (填选项字母),丁中反应的离子方程式___________ 。
A.abcfhde B.afhedbc C.afhdebc
②能证明固体A中含有碳酸钠的实验现象是___________ 。
(3)向 的水溶液中通入
的水溶液中通入 气体,会产生少量淡黄色沉淀,则反应中氧化剂与还原剂的物质的量之比为
气体,会产生少量淡黄色沉淀,则反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)某实验小组设计了两种制备硫酸铜的方案。
方案Ⅰ: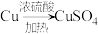
方案Ⅱ: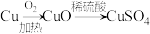
方案___________ (填“Ⅰ”或“Ⅱ”)更合理,理由为___________ 。

(1)向A的水溶液中滴加NaOH溶液并加热,产生一种能使润湿的红色石蕊试纸变蓝的气体,则A物质的化学式为
(2)某实验小组为了验证固体A中含有碳酸钠杂质,选用下列装置进行实验:
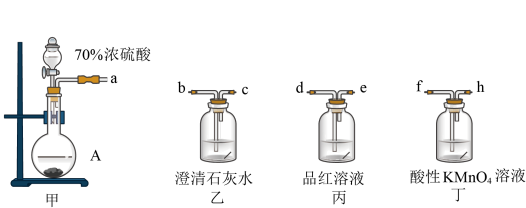
①实验装置的连接顺序为
A.abcfhde B.afhedbc C.afhdebc
②能证明固体A中含有碳酸钠的实验现象是
(3)向
 的水溶液中通入
的水溶液中通入 气体,会产生少量淡黄色沉淀,则反应中氧化剂与还原剂的物质的量之比为
气体,会产生少量淡黄色沉淀,则反应中氧化剂与还原剂的物质的量之比为(4)某实验小组设计了两种制备硫酸铜的方案。
方案Ⅰ:
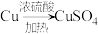
方案Ⅱ:
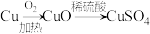
方案
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】锡酸钠(Na2SnO3·xH2O)主要用作电镀铜锡合金和碱性镀锡的基本原料。锡精矿除含SnO2外,还含有少量WO3、S、As、Fe,—种由锡精矿制备锡酸钠的工艺流程如下:
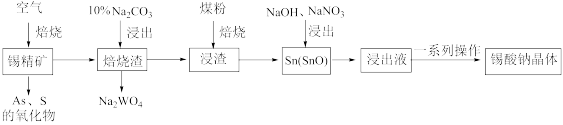
已知:①焙烧后,S、As变为挥发性氧化物而被除去,Fe变为Fe3O4;
②Na2SnO3•xH2O。易溶于水,其在水中的溶解度随着温度的升高而降低。
请回答下列问题:
(1)Sn元素的原子序数为50,其在周期表中的位置为_____________ 。
(2)从“焙烧渣”中除去Fe3O4最简单的方法为_____________ 。加入煤粉焙烧可将SnO2还原为Sn或SnO,Sn或SnO。在碱性条件下均能被NaNO3氧化为Na2SnO3,已知NaNO3的还原产物为NH3,则NaNO3氧化Sn的化学方程式为___________________ 。
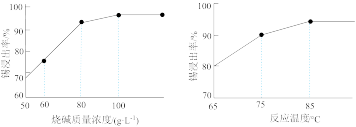
(3)如图为加入NaOH溶液和NaNO3溶液浸出时锡的浸出率与NaOH质量浓度和反应温度间的关系图,则“碱浸”的最适宜条件为_____________ 、___________ ,
(4)从浸出液中获得锡酸钠晶体的“一系列操作”具体是指___________ 、洗涤、干燥。
(5)采用热重分析法测定锡酸钠晶体样品所含结晶水数,将样品加热到140℃时,失掉全部结晶水,失重约20.2%。锡酸钠晶体的化学式为__________ 。
(6)以纯锡为阳极材料,以NaOH和Na2SnO3为电解液,待镀金属为阴极材料,可实现在待镀金属上的持续镀锡,镀锡时阳极的电极反应式为______________ 。

已知:①焙烧后,S、As变为挥发性氧化物而被除去,Fe变为Fe3O4;
②Na2SnO3•xH2O。易溶于水,其在水中的溶解度随着温度的升高而降低。
请回答下列问题:
(1)Sn元素的原子序数为50,其在周期表中的位置为
(2)从“焙烧渣”中除去Fe3O4最简单的方法为
(3)如图为加入NaOH溶液和NaNO3溶液浸出时锡的浸出率与NaOH质量浓度和反应温度间的关系图,则“碱浸”的最适宜条件为

(4)从浸出液中获得锡酸钠晶体的“一系列操作”具体是指
(5)采用热重分析法测定锡酸钠晶体样品所含结晶水数,将样品加热到140℃时,失掉全部结晶水,失重约20.2%。锡酸钠晶体的化学式为
(6)以纯锡为阳极材料,以NaOH和Na2SnO3为电解液,待镀金属为阴极材料,可实现在待镀金属上的持续镀锡,镀锡时阳极的电极反应式为
您最近一年使用:0次
【推荐2】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:

已知生成相应氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)如下:
(1)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O,2MgO·B2O3+2H2SO4=2H3BO3+2MgSO4。
①根据上述反应可知,酸性:H2SO4___________ (填“>”或“<”)H3BO3。
②已知硼酸与过量NaOH溶液发生中和反应的离子方程式为:H3BO3+OH-= 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是___________ (填字母)
A.硼酸是一元酸
B.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
C.硼酸的电离方程式可表示为H3BO3+H2O +H+
+H+
(2)检验褐色浸出液中的杂质离子:取少量浸出液,___________ (填操作和现象),证明溶液中含有Fe2+。
(3)除去浸出液中的杂质离子:用MgO调节溶液的pH至___________ 以上,使杂质离子转化为___________ (填化学式)沉淀,过滤。
(4)获取晶体:
ⅰ.浓缩滤液,使MgSO4溶液和H3BO3溶液接近饱和;
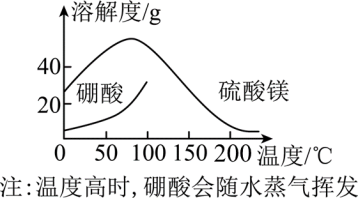
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合图中溶解度曲线,简述ⅱ的方法:将浓缩液加入高压釜中升温结晶得到___________ 晶体,分离后,再将母液降温结晶,分离得到另一种物质的晶体。

已知生成相应氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)如下:
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉定时 | 3.2 | 4.7 | 9.0 | 11.1 |
①根据上述反应可知,酸性:H2SO4
②已知硼酸与过量NaOH溶液发生中和反应的离子方程式为:H3BO3+OH-=
 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是A.硼酸是一元酸
B.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
C.硼酸的电离方程式可表示为H3BO3+H2O
 +H+
+H+(2)检验褐色浸出液中的杂质离子:取少量浸出液,
(3)除去浸出液中的杂质离子:用MgO调节溶液的pH至
(4)获取晶体:
ⅰ.浓缩滤液,使MgSO4溶液和H3BO3溶液接近饱和;
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合图中溶解度曲线,简述ⅱ的方法:将浓缩液加入高压釜中升温结晶得到

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钼是一种重要的过渡金属元素,钼酸钠晶体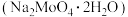 是一种重要的金属缓蚀剂。利用钼矿
是一种重要的金属缓蚀剂。利用钼矿 主要成分
主要成分 为原料冶炼金属钼和制备钼酸钠晶体的主要流程图如下:
为原料冶炼金属钼和制备钼酸钠晶体的主要流程图如下:

已知: 只能和HF反应,不能和其他酸反应。
只能和HF反应,不能和其他酸反应。
注:式量 Mo:96 :206
:206  :242
:242
 煅烧钼矿产生的气体为
煅烧钼矿产生的气体为 ,写出钼矿煅烧的化学方程式
,写出钼矿煅烧的化学方程式 ________________ 。
 用浓氨水溶解粗产品的离子方程式是
用浓氨水溶解粗产品的离子方程式是____________ ,由图中信息可以判断 是
是______________ 氧化物。 填“酸性”、“碱性”或“两性”
填“酸性”、“碱性”或“两性”
 操作I是
操作I是_________ ,操作Ⅱ所得料液的主要成分是__________  填化学式
填化学式 。
。
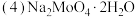 溶于水得到
溶于水得到 的水溶液在
的水溶液在 时密度为
时密度为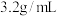 ,则该溶液中
,则该溶液中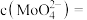
______ 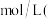 保留2位有效数字
保留2位有效数字
 流程中用 NaClO做氧化剂将矿石中的钼浸出,该过程的化学方程式是
流程中用 NaClO做氧化剂将矿石中的钼浸出,该过程的化学方程式是______ 。
 利用钼矿
利用钼矿 钼的质量分数为
钼的质量分数为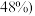 按照上述流程制备
按照上述流程制备 ,理论上,制得晶体
,理论上,制得晶体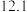 吨则需要的钼矿的质量是
吨则需要的钼矿的质量是_______________ 。
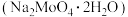 是一种重要的金属缓蚀剂。利用钼矿
是一种重要的金属缓蚀剂。利用钼矿 主要成分
主要成分 为原料冶炼金属钼和制备钼酸钠晶体的主要流程图如下:
为原料冶炼金属钼和制备钼酸钠晶体的主要流程图如下:
已知:
 只能和HF反应,不能和其他酸反应。
只能和HF反应,不能和其他酸反应。注:式量 Mo:96
 :206
:206  :242
:242 煅烧钼矿产生的气体为
煅烧钼矿产生的气体为 ,写出钼矿煅烧的化学方程式
,写出钼矿煅烧的化学方程式  用浓氨水溶解粗产品的离子方程式是
用浓氨水溶解粗产品的离子方程式是 是
是 填“酸性”、“碱性”或“两性”
填“酸性”、“碱性”或“两性”
 操作I是
操作I是 填化学式
填化学式 。
。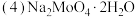 溶于水得到
溶于水得到 的水溶液在
的水溶液在 时密度为
时密度为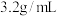 ,则该溶液中
,则该溶液中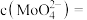
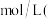 保留2位有效数字
保留2位有效数字
 流程中用 NaClO做氧化剂将矿石中的钼浸出,该过程的化学方程式是
流程中用 NaClO做氧化剂将矿石中的钼浸出,该过程的化学方程式是 利用钼矿
利用钼矿 钼的质量分数为
钼的质量分数为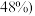 按照上述流程制备
按照上述流程制备 ,理论上,制得晶体
,理论上,制得晶体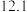 吨则需要的钼矿的质量是
吨则需要的钼矿的质量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】醋酸亚铬[(CH3COO)2Cr·2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂,一般制备方法是先在封闭体系中利用金属锌作还原剂。将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题:

(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是_______ 。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,关闭K3,此时c 中有气体产生,该气体的作用是_______ 。
(3)打开K3,关闭K1和K2,c中亮蓝色溶液流入d,其原因是_______ ;d中析出砖红色沉淀。
(4)指出装置d可能存在的缺点_______ 。

(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,关闭K3,此时c 中有气体产生,该气体的作用是
(3)打开K3,关闭K1和K2,c中亮蓝色溶液流入d,其原因是
(4)指出装置d可能存在的缺点
您最近一年使用:0次
【推荐2】某铬渣主要含有 以及少量的
以及少量的 、
、 等杂质,某研究小组设计以下流程获取
等杂质,某研究小组设计以下流程获取 ,实现铬渣资源化。
,实现铬渣资源化。

资料:
a.焙烧中加入氧化钙的目的是防止物料烧结,并提高物料焙烧温度。
b.常温下,水溶液中存在 ,
, 。
。
c. 与
与 类似,均具有两性。
类似,均具有两性。
d.
(1)为提高“酸浸”速率,可采取的措施有___________ (至少写出两条)。
(2)焙烧时, 被
被 氧化为
氧化为 ,产物中还有
,产物中还有 ,写出该反应的化学方程式
,写出该反应的化学方程式___________
(3)滤液A中加入 发生的氧化反应:
发生的氧化反应:
①含铬元素的微粒参与的还原反应:___________ 。
②实验表明,酸浸时调节pH越低,最终得到的铬回收率越高,原因是___________ 。
③当加入 过量,过量的
过量,过量的 与
与 形成配合物
形成配合物 而稳定存在,对铬回收率的影响是
而稳定存在,对铬回收率的影响是___________ (填“增大”、“减小”、或者“不影响”),理由是___________ 。
(4)滤液A中 发生反应的离子方程式是
发生反应的离子方程式是___________ 。
(5)草酸“除铁”的离子方程式是___________ 。
(6)90℃时,加入 调节pH,不同pH对铬沉淀率的影响如下图所示,请解释铬沉淀率随着pH先增大后减小的原因
调节pH,不同pH对铬沉淀率的影响如下图所示,请解释铬沉淀率随着pH先增大后减小的原因___________ 。

 以及少量的
以及少量的 、
、 等杂质,某研究小组设计以下流程获取
等杂质,某研究小组设计以下流程获取 ,实现铬渣资源化。
,实现铬渣资源化。
资料:
a.焙烧中加入氧化钙的目的是防止物料烧结,并提高物料焙烧温度。
b.常温下,水溶液中存在
 ,
, 。
。c.
 与
与 类似,均具有两性。
类似,均具有两性。d.

(1)为提高“酸浸”速率,可采取的措施有
(2)焙烧时,
 被
被 氧化为
氧化为 ,产物中还有
,产物中还有 ,写出该反应的化学方程式
,写出该反应的化学方程式(3)滤液A中加入
 发生的氧化反应:
发生的氧化反应:
①含铬元素的微粒参与的还原反应:
②实验表明,酸浸时调节pH越低,最终得到的铬回收率越高,原因是
③当加入
 过量,过量的
过量,过量的 与
与 形成配合物
形成配合物 而稳定存在,对铬回收率的影响是
而稳定存在,对铬回收率的影响是(4)滤液A中
 发生反应的离子方程式是
发生反应的离子方程式是(5)草酸“除铁”的离子方程式是
(6)90℃时,加入
 调节pH,不同pH对铬沉淀率的影响如下图所示,请解释铬沉淀率随着pH先增大后减小的原因
调节pH,不同pH对铬沉淀率的影响如下图所示,请解释铬沉淀率随着pH先增大后减小的原因
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】氧化铬 主要用于冶炼金属铬、有机化学合成的催化剂等。工业上以铬铁矿[主要成份:
主要用于冶炼金属铬、有机化学合成的催化剂等。工业上以铬铁矿[主要成份: (亚铬酸亚铁),还含有
(亚铬酸亚铁),还含有 等杂质]为主要原料进行生产,其主要工艺流程如图:
等杂质]为主要原料进行生产,其主要工艺流程如图:

(1)“高温氧化”过程中 转化为
转化为 的化学方程式为
的化学方程式为_______ 。
(2)为了加快水浸速率,提高铬元素的浸出率可采取的措施是_______ 。
(3)为获得纯净 ,需对其洗涤。判断
,需对其洗涤。判断 洗涤干净的操作是
洗涤干净的操作是_______ 。
(4)现用 模拟工业上处理含铬废水
模拟工业上处理含铬废水 (浓度
(浓度 ),处理后所得滤渣主要成分为
),处理后所得滤渣主要成分为 ;(已知:S元素被氧化为可溶性硫酸盐)。
;(已知:S元素被氧化为可溶性硫酸盐)。
① 处理废水的离子方程式为
处理废水的离子方程式为_______ ;若处理10L的“废水”可氧化
_______ mol。
②将滤渣用蒸馏水洗净后,在低温条件下干燥,将干燥后的固体在空气中加热,测得固体质量随温度的变化如图所示。[说明:780℃以上的残留固体为 、
、 的混合物]
的混合物]

A→B固体质量增加的原因是_______ ;
 主要用于冶炼金属铬、有机化学合成的催化剂等。工业上以铬铁矿[主要成份:
主要用于冶炼金属铬、有机化学合成的催化剂等。工业上以铬铁矿[主要成份: (亚铬酸亚铁),还含有
(亚铬酸亚铁),还含有 等杂质]为主要原料进行生产,其主要工艺流程如图:
等杂质]为主要原料进行生产,其主要工艺流程如图:
(1)“高温氧化”过程中
 转化为
转化为 的化学方程式为
的化学方程式为(2)为了加快水浸速率,提高铬元素的浸出率可采取的措施是
(3)为获得纯净
 ,需对其洗涤。判断
,需对其洗涤。判断 洗涤干净的操作是
洗涤干净的操作是(4)现用
 模拟工业上处理含铬废水
模拟工业上处理含铬废水 (浓度
(浓度 ),处理后所得滤渣主要成分为
),处理后所得滤渣主要成分为 ;(已知:S元素被氧化为可溶性硫酸盐)。
;(已知:S元素被氧化为可溶性硫酸盐)。①
 处理废水的离子方程式为
处理废水的离子方程式为
②将滤渣用蒸馏水洗净后,在低温条件下干燥,将干燥后的固体在空气中加热,测得固体质量随温度的变化如图所示。[说明:780℃以上的残留固体为
 、
、 的混合物]
的混合物]
A→B固体质量增加的原因是
您最近一年使用:0次



