有机物M是一种重要的有机合成材料,以A为原料通过以下两步反应可以获得M。
反应I:
 ,反应Ⅱ:
,反应Ⅱ:

一定温度下,向一定体积的密闭容器中加入一定量A和B发生上述两个反应。该体系中A、C、M的浓度随时间变化曲线如图甲所示。两个反应的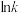 (
( ,k为速率常数,Ea为反应活化能,R和c为常数)与温度T的关系如图乙所示。下列说法正确的是
,k为速率常数,Ea为反应活化能,R和c为常数)与温度T的关系如图乙所示。下列说法正确的是
反应I:

 ,反应Ⅱ:
,反应Ⅱ:

一定温度下,向一定体积的密闭容器中加入一定量A和B发生上述两个反应。该体系中A、C、M的浓度随时间变化曲线如图甲所示。两个反应的
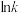 (
( ,k为速率常数,Ea为反应活化能,R和c为常数)与温度T的关系如图乙所示。下列说法正确的是
,k为速率常数,Ea为反应活化能,R和c为常数)与温度T的关系如图乙所示。下列说法正确的是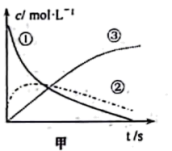

| A.曲线③代表M的浓度变化 |
B.两个反应的焓变关系为 |
C.两个反应的活化能关系为 |
| D.T1温度时,两个反应一定处于平衡状态 |
更新时间:2024-02-02 13:46:45
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】工业制硫酸的关键反应为
 ,在
,在 存在时,该反应的机理为:i.
存在时,该反应的机理为:i. (快);ii.
(快);ii.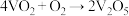 (慢)。下列说法正确的是
(慢)。下列说法正确的是

 ,在
,在 存在时,该反应的机理为:i.
存在时,该反应的机理为:i. (快);ii.
(快);ii.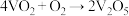 (慢)。下列说法正确的是
(慢)。下列说法正确的是| A.反应i的活化能比反应ii的活化能小 | B.反应i是决速步骤 |
| C.工业生产中应选择低温条件 | D. 是该反应的催化剂 是该反应的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】甲酸分子在活性Pd催化剂表面脱氢的反应历程与能量变化如图所示。
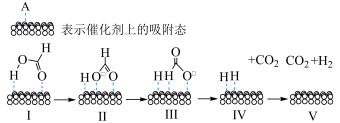
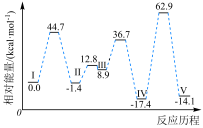
下列说法正确的是


下列说法正确的是
| A.升高温度,甲酸的平衡转化率增大 |
B.在Pd催化剂表面 键的解离速率比 键的解离速率比 键的解离速率快 键的解离速率快 |
C. 键的键能约为 键的键能约为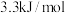 |
D.若用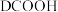 代替 代替 ,可得到 ,可得到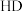 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】光气 (COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g) +CO(g) COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。下列说法不正确的是
COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。下列说法不正确的是


 COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。下列说法不正确的是
COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。下列说法不正确的是

| A.0~6 min内,反应的平均速率v(Cl2)=0.15 mol ·L-1·min-1; |
| B.若保持温度不变,在第7 min 向体系中加入这三种物质各2 mol,则平衡向正反应方向移动; |
| C.随温度升高,该反应平衡常数减小;比较第8 min反应温度T(8)与第15 min反应温度T(15)的高低:T(8) >T(15)。 |
| D.若将初始投料浓度变为c(Cl2)=0.7 mol/L、c(CO)=0.5 mol/L、c(COCl2)=0.5 mol/L,保持反应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6 min时Cl2的体积分数相同; |
您最近一年使用:0次
【推荐2】一定温度下,向容积为2L的恒容密闭容器中充入6molCO2和8molH2,发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,测得n(H2)随时间的变化如曲线I所示。下列说法正确的是


| A.该反应在0~1min内CO2的转化率为25% |
| B.若起始充入4molCO2、2molH2、2molCH3OH和1molH2O,该温度下反应正向进行 |
| C.若起始时向容器中充入3molCO2和4molH2,该温度下平衡时H2O体积分数大于20% |
| D.改变条件得到曲线II、III,则曲线II、III改变的条件分别是升高温度、充入氦气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】判断A(g)+B(g)  C(g)+D(g)是否达到平衡的依据为( )
C(g)+D(g)是否达到平衡的依据为( )
 C(g)+D(g)是否达到平衡的依据为( )
C(g)+D(g)是否达到平衡的依据为( )| A.压强不随时间改变 |
| B.气体的密度不随时间改变 |
| C.c(A)不随时间改变 |
| D.单位时间里生成C和D的物质的量相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在一定条件下,在容积不变的密闭容器中,1molN2和3molH2发生反应N2(g)+3H2(g)  2NH3(g) ΔH= -92kJ·mol-1。下列说法正确的是
2NH3(g) ΔH= -92kJ·mol-1。下列说法正确的是
 2NH3(g) ΔH= -92kJ·mol-1。下列说法正确的是
2NH3(g) ΔH= -92kJ·mol-1。下列说法正确的是| A.N2、H2和NH3的物质的量比为1:3:2时,该反应达到平衡 |
| B.该反应达到平衡时,v正(NH3) =2v逆(N2) |
| C.达到平衡时,再加入1molN2,达到平衡后NH3的浓度和百分含量均增大 |
| D.提高该反应的温度,可以实现H2的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
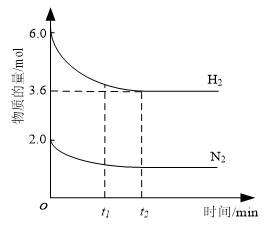
【推荐3】通常状况下,NH3是具有刺激性气味的气体,密度比空气小,易液化成液氨,且它极易溶于水形成氨水,工业上常用氨气制备硝酸。在2.0 L恒温恒容密闭容器中充入2.0 mol N2和6.0 mol H2,加入催化剂发生反应:N2(g)+3H2(g)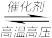 2NH3(g),N2、H2的物质的量随时间的变化如图所示。下列有关说法正确的是
2NH3(g),N2、H2的物质的量随时间的变化如图所示。下列有关说法正确的是
 2NH3(g),N2、H2的物质的量随时间的变化如图所示。下列有关说法正确的是
2NH3(g),N2、H2的物质的量随时间的变化如图所示。下列有关说法正确的是
| A.t1 min时,N2的生成速率等于N2的消耗速率 |
| B.使用催化剂可以缩短到达平衡时所需的时间 |
C.0~t2 min内,v(NH3)=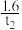 mol·L−1·min−1 mol·L−1·min−1 |
| D.反应中通入足量的N2,可使H2完全转化为NH3 |
您最近一年使用:0次

 ,直接用于温和条件下
,直接用于温和条件下 、
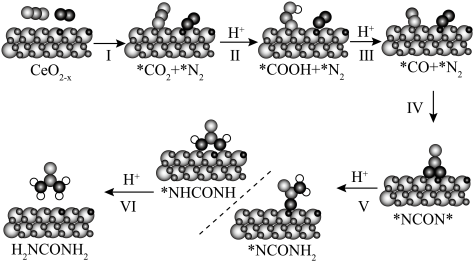
、 的协同光催化反应合成尿素。反应过程中的能量变化及机理如下:
的协同光催化反应合成尿素。反应过程中的能量变化及机理如下: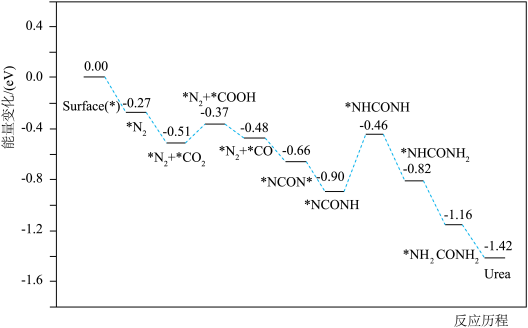
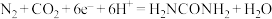
 气体充入1 L密闭容器中,发生反应
气体充入1 L密闭容器中,发生反应 ,
, 、
、 的浓度随时间的变化关系如图,已知
的浓度随时间的变化关系如图,已知 的消耗速率与各自的分压有如下关系:
的消耗速率与各自的分压有如下关系: ,
, ,已知:
,已知: ,
, 、
、 分别为
分别为

 与
与 、
、 间的关系为
间的关系为