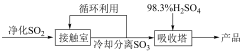
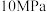工业制备硫酸的生产过程及相关信息如下。下列有关说法正确的是
温度/℃ | 不同压强下接触室中 | |
|
| |
450 | 99.2 | 99.7 |
550 | 94.9 | 97.7 |
工艺流程 |
| |
A.循环利用的物质是 |
B. 为放热反应 为放热反应 |
C.吸收塔中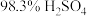 表现强氧化性 表现强氧化性 |
D.实际生产中,接触室中应采用温度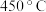 ,压强 ,压强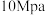 |
更新时间:2024-03-03 08:59:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
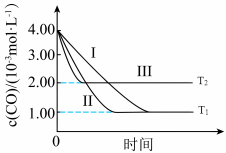
【推荐1】利用催化技术可将汽车尾气中的NO和CO转化: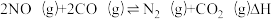 。初始时
。初始时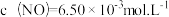 ,
,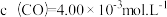 。在不同的催化剂比表面积(
。在不同的催化剂比表面积( )和不同温度下(T1、T2温度改变对催化剂活性的影响忽略),CO的浓度随时间的变化如图所示。下列有关说法正确的是
)和不同温度下(T1、T2温度改变对催化剂活性的影响忽略),CO的浓度随时间的变化如图所示。下列有关说法正确的是
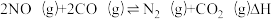 。初始时
。初始时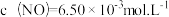 ,
,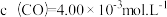 。在不同的催化剂比表面积(
。在不同的催化剂比表面积( )和不同温度下(T1、T2温度改变对催化剂活性的影响忽略),CO的浓度随时间的变化如图所示。下列有关说法正确的是
)和不同温度下(T1、T2温度改变对催化剂活性的影响忽略),CO的浓度随时间的变化如图所示。下列有关说法正确的是
| A.T1>T2 | B.△H<0 |
| C.催化剂比表面积(m2.g-1):I>Ⅱ | D.NO与CO的平衡转化率相等 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学反应C(s)+H2O(g) CO(g)+H2(g)△H>0达到平衡,下列叙述正确的是
CO(g)+H2(g)△H>0达到平衡,下列叙述正确的是
 CO(g)+H2(g)△H>0达到平衡,下列叙述正确的是
CO(g)+H2(g)△H>0达到平衡,下列叙述正确的是| A.减小压强,平衡向正反应方向移动 |
| B.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
| C.加入水蒸气使容器压强增大,平衡不移动 |
| D.加入固体碳,平衡向正反应方向移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】我国科学家研发的“液态阳光”计划是:通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制备甲醇。
主反应: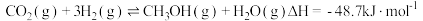
副反应:
将 和
和 按物质的量比
按物质的量比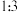 混合,以固定流速通过盛放
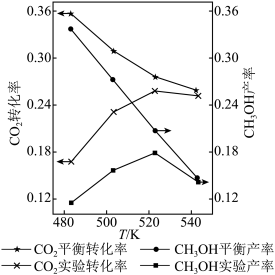
混合,以固定流速通过盛放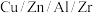 催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。下列说法
催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。下列说法不正确 的是
已知: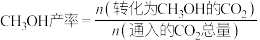
主反应:
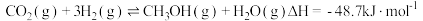
副反应:

将
 和
和 按物质的量比
按物质的量比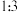 混合,以固定流速通过盛放
混合,以固定流速通过盛放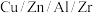 催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。下列说法
催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。下列说法已知:
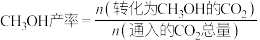

A.由图可知,催化剂活性最好的温度大约在 |
B. 升温到 升温到 ,主反应的反应速率受温度影响更大 ,主反应的反应速率受温度影响更大 |
C.为了提高 的平衡转化率和 的平衡转化率和 的平衡产率,可以选择低温、高压条件 的平衡产率,可以选择低温、高压条件 |
D.温度由 升到 升到 的实验产率降低的原因可能是:温度升高,主反应逆移程度大于副反应正移程度 的实验产率降低的原因可能是:温度升高,主反应逆移程度大于副反应正移程度 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
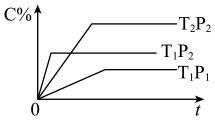
【推荐1】已知某可逆反应:mA(g) + nB(g) pC(g) ∆H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
pC(g) ∆H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
 pC(g) ∆H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
pC(g) ∆H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
| A.T1<T2 ,P1>P2 , m+n<P , Q<0 | B.T1>T2 , P1<P2 , m+n>P , Q>0 |
| C.T1<T2 , P1<P2 , m+n<P , Q>0 | D.T1>T2 , P1<P2 ,m+n>P ,Q<0 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在恒温时,一固定容积的容器内发生如下反应:2NO2(g)  N2O4(g),达平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后与第一次平衡时相比,下列说法正确的是
N2O4(g),达平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后与第一次平衡时相比,下列说法正确的是
 N2O4(g),达平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后与第一次平衡时相比,下列说法正确的是
N2O4(g),达平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后与第一次平衡时相比,下列说法正确的是| A.NO2的体积分数减小 | B.NO2的转化率减小 |
| C.化学反应速率不变 | D.气体的平均相对分子质量减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列选项中的原因或结论与现象不对应的是
| 选项 | 现象 | 原因或结论 |
| A | 在H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
| B | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 2NO2(g) N2O4(g)ΔH<0,平衡向生成NO2方向移动 N2O4(g)ΔH<0,平衡向生成NO2方向移动 |
| C | 在密闭容器中有反应:A+xB(g) 2C(g)达到平衡时测得c(A)为0.5 mol·L-1,恒温条件下将容器容积扩大到原来的两倍,测得c(A)为0.4 mol·L-1 2C(g)达到平衡时测得c(A)为0.5 mol·L-1,恒温条件下将容器容积扩大到原来的两倍,测得c(A)为0.4 mol·L-1 | A为非气体、x=1 |
| D | 向5mL 0.005mol·L-1FeCl3溶液中加入5mL 0.015mol·L-1 KSCN溶液,溶液呈红色,再滴加几滴1mol·L-1 KSCN溶液,溶液颜色加深 | 增大反应物浓度,平衡向正反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】工业上制备硫酸的一步重要反应是 在400~500℃下的催化氧化反应
在400~500℃下的催化氧化反应 △H<0。下列有关说法错误的是
△H<0。下列有关说法错误的是
 在400~500℃下的催化氧化反应
在400~500℃下的催化氧化反应 △H<0。下列有关说法错误的是
△H<0。下列有关说法错误的是A.实际生产中, 、 、 再循环使用提高原料利用率 再循环使用提高原料利用率 |
B.在实际生产中控制温度为400~500℃,温度过低速率慢,温度过高 转化率低 转化率低 |
C.为提高反应速率和平衡时 的转化率,实际生产中采用的压强越大越好 的转化率,实际生产中采用的压强越大越好 |
| D.要综合考虑影响速率与平衡的各种因素、设备条件和经济成本等,寻找适宜的生产条件 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】图为工业合成氨以及氨催化氧化制硝酸的流程示意图。下列说法不正确的是
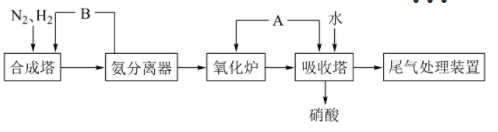

| A.物质B是未反应完全的氮气和氢气,通过循环投料,可以提高原料利用率 |
| B.物质A是空气,其中的O2在吸收塔中氧化NO,使之能被水充分吸收生成硝酸 |
C.为提高原料价格更高的 的转化率,应向合成塔通入过量的空气以提高N2浓度 的转化率,应向合成塔通入过量的空气以提高N2浓度 |
| D.尾气中的氮氧化物可使用碱性的Na2CO3溶液吸收,或使用NH3将氮氧化物还原为N2 |
您最近半年使用:0次

 的平衡转化率/
的平衡转化率/