回答下列问题。
(1)醋酸是常见的弱酸。
 醋酸在水溶液中的电离方程式为
醋酸在水溶液中的电离方程式为 ___________ 。
 下列方法中,可以使醋酸稀溶液中
下列方法中,可以使醋酸稀溶液中 电离程度增大的是
电离程度增大的是___________  填字母序号
填字母序号 。
。
a.滴加少量浓盐酸 b.微热溶液 c.加水稀释 d.加入少量醋酸钠晶体
(2)用 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。

 滴定醋酸的曲线是
滴定醋酸的曲线是___________  填“
填“ ”或“Ⅱ”
”或“Ⅱ” 。
。
 滴定开始前,三种溶液中由水电离出的
滴定开始前,三种溶液中由水电离出的 最大的是
最大的是___________ 。
 上述用
上述用 的
的 溶液滴定
溶液滴定 的盐酸,下列操作不正确的是
的盐酸,下列操作不正确的是___________ 。
A.用标准 溶液润洗碱式滴定管后,再装入标准碱溶液
溶液润洗碱式滴定管后,再装入标准碱溶液
B.用待测酸溶液润洗锥形瓶后,再装入待测酸溶液
C.滴定时两眼应注视滴定管中液面的变化,以免滴定过量
D.读数时,视线应与滴定管凹液面的最低点保持水平
(1)醋酸是常见的弱酸。
 醋酸在水溶液中的电离方程式为
醋酸在水溶液中的电离方程式为  下列方法中,可以使醋酸稀溶液中
下列方法中,可以使醋酸稀溶液中 电离程度增大的是
电离程度增大的是 填字母序号
填字母序号 。
。a.滴加少量浓盐酸 b.微热溶液 c.加水稀释 d.加入少量醋酸钠晶体
(2)用
 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。
 滴定醋酸的曲线是
滴定醋酸的曲线是 填“
填“ ”或“Ⅱ”
”或“Ⅱ” 。
。 滴定开始前,三种溶液中由水电离出的
滴定开始前,三种溶液中由水电离出的 最大的是
最大的是 上述用
上述用 的
的 溶液滴定
溶液滴定 的盐酸,下列操作不正确的是
的盐酸,下列操作不正确的是A.用标准
 溶液润洗碱式滴定管后,再装入标准碱溶液
溶液润洗碱式滴定管后,再装入标准碱溶液B.用待测酸溶液润洗锥形瓶后,再装入待测酸溶液
C.滴定时两眼应注视滴定管中液面的变化,以免滴定过量
D.读数时,视线应与滴定管凹液面的最低点保持水平
更新时间:2024-03-17 16:29:52
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知水的电离平衡曲线如图所示:回答下列问题:A、B、C、D四点Kw的关系是_______ .( …表示)。
…表示)。
 …表示)。
…表示)。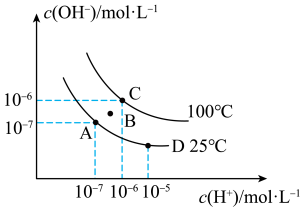
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在不同温度下的水溶液中c(H+)=x mol/L,c(OH-)=y mol/L,x与y的关系如图所示。
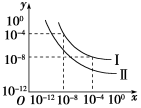
曲线Ⅰ代表的温度下,水的离子积为_______ ,曲线Ⅰ所代表的温度_______ (填“高于”、“低于”或“等于”)曲线Ⅱ所代表的温度。你判断的依据是_______ 。

曲线Ⅰ代表的温度下,水的离子积为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸溶液滴定待测的NaOH溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_________ 。直到因加入一滴盐酸后,溶液由黄色变为橙色,并______ 为止。
(2)若滴定开始和结束时,酸式滴定管中的液面如图示,则所用盐酸溶液的体积为_____ mL。

(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是_____ 。
A.酸式滴定管未用标准液润洗就直接注入标准盐酸溶液
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(1)用标准的盐酸溶液滴定待测的NaOH溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)若滴定开始和结束时,酸式滴定管中的液面如图示,则所用盐酸溶液的体积为

(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A.酸式滴定管未用标准液润洗就直接注入标准盐酸溶液
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如何除去酸式、碱式滴定管尖端处的气泡___________ ?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】食醋分为酿造醋和配制醋两种。国家规定食醋中总酸量不得低于3.5g/(100mL)。
(1)某研究小组利用滴定分析法测定某品牌食醋中 的含量,下列说法正确的是
的含量,下列说法正确的是__________ (填序号)。
A.用NaOH溶液滴定时反应的离子方程式为
B.食醋试样需稀释一定倍数后再进行滴定
C.用NaOH溶液滴定食醋,可使用酚酞或甲基橙作指示剂
D.若测得该品牌食醋中 的物质的量浓度为
的物质的量浓度为 ,则该食醋的总酸量为4.5g/(100mL)
,则该食醋的总酸量为4.5g/(100mL)
(2)常温下,用 的NaOH溶液分别滴定20.00mL
的NaOH溶液分别滴定20.00mL 的HCl溶液和20.00mL
的HCl溶液和20.00mL 的
的 溶液,得到两条滴定曲线,如图所示。
溶液,得到两条滴定曲线,如图所示。

①滴定 溶液的曲线是
溶液的曲线是________ (填“图1”或“图2”);滴定曲线中
_________ 。
②E点溶液呈__________ 性,该溶液中的溶质是_____________________________ 。
(1)某研究小组利用滴定分析法测定某品牌食醋中
 的含量,下列说法正确的是
的含量,下列说法正确的是A.用NaOH溶液滴定时反应的离子方程式为

B.食醋试样需稀释一定倍数后再进行滴定
C.用NaOH溶液滴定食醋,可使用酚酞或甲基橙作指示剂
D.若测得该品牌食醋中
 的物质的量浓度为
的物质的量浓度为 ,则该食醋的总酸量为4.5g/(100mL)
,则该食醋的总酸量为4.5g/(100mL)(2)常温下,用
 的NaOH溶液分别滴定20.00mL
的NaOH溶液分别滴定20.00mL 的HCl溶液和20.00mL
的HCl溶液和20.00mL 的
的 溶液,得到两条滴定曲线,如图所示。
溶液,得到两条滴定曲线,如图所示。
①滴定
 溶液的曲线是
溶液的曲线是
②E点溶液呈
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】弱电解质的电离平衡与日常生活、工农业生产等息息相关。回答下列问题:
Ⅰ.25℃时,部分弱酸的电离平衡常数如下表:
(1)H2S的二级电离平衡常数的表达式为___________ 。
(2)相同c(H+)浓度的HCOOH和HClO溶液中:c(HCOO-)___________ c(ClO-)。(填“>”、“<”或“=”)
(3)根据上述电离常数及物质的特性判断下列化学反应方程式错误的是___________ (填序号)。
①次氯酸与碳酸钠溶液的反应:HClO+ =ClO-+
=ClO-+
②少量CO2通入NaClO溶液中:CO2+H2O+ClO-=HClO+
③硫化氢气体通入NaClO溶液中:H2S+ClO-=HS-+HClO
④碳酸钠滴入足量甲酸溶液中:2HCOOH+ =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
⑤Na2CO3溶液通入少量H2S:2 +H2S=S2-+2
+H2S=S2-+2
Ⅱ.常压下,某化学兴趣小组取不同浓度、不同温度的醋酸进行各项内容的测定,得到下表实验数据。
已知:电离度d= ×100%
×100%
(4)温度升高,CH3COOH的电离平衡向___________ (填“左”或“右”)移动,能支持该结论的表中数据是___________ (填字母)。
a.c(H+) b.电离度 c.电离常数 d.c(CH3COOH)
(5)表中c(H+)基本不变的原因是___________ 。
Ⅰ.25℃时,部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | H2S | H2CO3 | HClO |
| 电离平衡常数 (25℃) | Ka=1.77×10-4 | Ka1=1.3×10-7 Ka2=7.1×10-15 | Ka1=4.4×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 |
(2)相同c(H+)浓度的HCOOH和HClO溶液中:c(HCOO-)
(3)根据上述电离常数及物质的特性判断下列化学反应方程式错误的是
①次氯酸与碳酸钠溶液的反应:HClO+
 =ClO-+
=ClO-+
②少量CO2通入NaClO溶液中:CO2+H2O+ClO-=HClO+

③硫化氢气体通入NaClO溶液中:H2S+ClO-=HS-+HClO
④碳酸钠滴入足量甲酸溶液中:2HCOOH+
 =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑⑤Na2CO3溶液通入少量H2S:2
 +H2S=S2-+2
+H2S=S2-+2
Ⅱ.常压下,某化学兴趣小组取不同浓度、不同温度的醋酸进行各项内容的测定,得到下表实验数据。
| 温度/℃ | c(CH3COOH)/mol·L-1 | 电离常数 | 电离度/% | c(H+)/mol·L-1 |
| 0 | 16.06 | 1.37×10-1 | 9.098 | 1.507×10-2 |
| 10 | 15.16 | 1.57×10-1 | 10.18 | 1.543×10-2 |
| 20 | 13.63 | 1.71×10-1 | 11.2 | 1.527×10-2 |
 ×100%
×100%(4)温度升高,CH3COOH的电离平衡向
a.c(H+) b.电离度 c.电离常数 d.c(CH3COOH)
(5)表中c(H+)基本不变的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】与化学平衡类似,电离平衡的平衡常数,叫做电离常数,几种弱酸的电离常数(25℃)如下表:
回答下列问题:
(1)上述4种酸中,酸性最弱的是___________ (用化学式表示),往 溶液中加入
溶液中加入 溶液,
溶液,___________ (填“能”或“不能”)发生反应,若能反应,则写出该反应的离子方程式___________ 。
(2)试写出草酸(H2C2O4)的第一步电离的电离方程式为:___________ 。
(3)水是一种极弱的电解质,在水的电离平衡中, 和
和 的关系如图所示:
的关系如图所示:
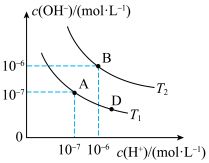
①A点水的离子积常数为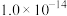 ,B点水的离子积常数为
,B点水的离子积常数为___________ ,造成水的离子积变化的因素是___________ 。
② 时,若某盐酸中
时,若某盐酸中 ,则由水电离产生的
,则由水电离产生的
___________ mol/L。
| 化学式 |  |  |  |  |
| 电离常数 |  | 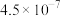 (第一步) (第一步) |  |  (第一步) (第一步) |
(1)上述4种酸中,酸性最弱的是
 溶液中加入
溶液中加入 溶液,
溶液,(2)试写出草酸(H2C2O4)的第一步电离的电离方程式为:
(3)水是一种极弱的电解质,在水的电离平衡中,
 和
和 的关系如图所示:
的关系如图所示:
①A点水的离子积常数为
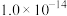 ,B点水的离子积常数为
,B点水的离子积常数为②
 时,若某盐酸中
时,若某盐酸中 ,则由水电离产生的
,则由水电离产生的
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】化学平衡移动原理同样也适用于其他平衡。已知在氨水中存在下列平衡:NH3+H2O⇌NH3·H2O⇌_______
(1)补充完题干中的电离方程式:NH3·H2O⇌_______ ,加热滴有酚酞的氨水,其颜色会_______ 。(填“深”或“浅”)
(2)向氨水中加入MgCl2固体时,平衡向_______ 移动,OH-的浓度_______ , 的浓度
的浓度_______ (填“减小”“增大”或“不变”)。
(3)向氨水中加入浓盐酸,平衡向_______ 移动,此时溶液中浓度增大的离子_______ 。
(4)向浓氨水中加入少量NaOH固体,平衡向_______ 移动,此时发生的现象是_______ 。
(5)常温下,NH3·H2O 的电离常数为2×10-5,则NH4Cl水溶液水解常数Kh=_______ 。
(6)0.1mol/LHCl的pH=_______ ,水电离出的c(OH-)=_______ ,此溶液中的电荷守恒表达式为_______ 。
(1)补充完题干中的电离方程式:NH3·H2O⇌
(2)向氨水中加入MgCl2固体时,平衡向
 的浓度
的浓度(3)向氨水中加入浓盐酸,平衡向
(4)向浓氨水中加入少量NaOH固体,平衡向
(5)常温下,NH3·H2O 的电离常数为2×10-5,则NH4Cl水溶液水解常数Kh=
(6)0.1mol/LHCl的pH=
您最近一年使用:0次




