五种短周期元素的某些性质如下表所示,其中W、Y、Z为同周期元素。
下列说法正确的是
| 元素代号 | X | W | Y | Z | Q |
| 原子半径/nm | 0.037 | 0.077 | 0.075 | 0.074 | 0.160 |
| 主要化合价 | +1 | +4、-4 | +5、-3 | -2 | +2 |
| A.X与W之间形成的分子为正四面体结构 |
| B.元素的第一电离能:W>Y>Z |
C.在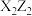 分子中,Z原子采用 分子中,Z原子采用 杂化 杂化 |
D.W元素原子轨道以 杂化形成的单质是共价晶体 杂化形成的单质是共价晶体 |
更新时间:2024-03-07 10:47:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】原子核外p能级、d能级等原子轨道上电子排布为“全空”“半满”“全满”的时候一般更加稳定,称为洪特规则的特例。下列事实不能作为这个规则的证据的是( )
| A.硼元素的第一电离能小于铍元素的第一电离能 |
| B.磷元素的第一电离能大于硫元素的第一电离能 |
C.基态铜原子的核外电子排布式为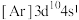 而不是 而不是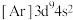 |
D.某种激发态碳原子的核外电子排布式为 而不是 而不是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】现有四种元素基态原子的电子排布式如下。则下列比较正确的是
① ;②
;② ;③
;③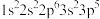 ;④
;④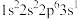
①
 ;②
;② ;③
;③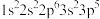 ;④
;④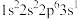
| A.第一电离能:③>①>④ | B.离子半径:④>①>② |
| C.电负性:①>②>④ | D.最高正化合价:①=③>④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】X、Y、Z、W均为短周期元素,其中X、Z、W在元素周期表中的相对位置如图所示,Y的最高价氧化物对应水化物是一种中强碱,且Y与Z位于同周期,原子序数比Z小2。
下列说法正确的是
| X | ||
| Z | W |
A.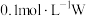 的含氧酸溶液的pH<1 的含氧酸溶液的pH<1 |
| B.X、W元素能组成直线形分子 |
| C.X、Z元素形成的单质的晶体类型相同 |
| D.化合物YXW3中含有离子键、极性键、非极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国科研团队对嫦娥五号月壤的研究发现,月壤中存在一种含“水”矿物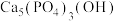 。下列化学用语或图示不正确的是
。下列化学用语或图示不正确的是
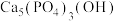 。下列化学用语或图示不正确的是
。下列化学用语或图示不正确的是A. 的电子式: 的电子式: | B.P原子的结构示意图: |
C. 的空间结构模型: 的空间结构模型: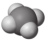 | D. 的VSEPR模型: 的VSEPR模型: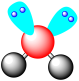 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】前三周期主族元素a、b、c、d的原子序数依次增大;a、c的氢化物分子的空间结构为V形;b在短周期元素中电负性最小。下列说法正确的是
| A.b2c2中不含非极性共价键 |
| B.b、c、d的简单离子半径由大到小的顺序为c>d>b |
| C.c、d的氧化物对应水化物的酸性由强到弱的顺序为d>c |
| D.c的单质在过量a的单质中燃烧,所得产物分子的空间结构为平面三角形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】光气(COCl2)是一种重要的有机中间体,其制备原理为: 。下列叙述正确的是
。下列叙述正确的是
 。下列叙述正确的是
。下列叙述正确的是| A.CHCl3是含有极性共价键的非极性分子 | B.H2O2中氧原子的杂化方式为sp2杂化 |
| C.COCl2的VSEPR模型为三角锥形 | D.HCl的沸点是同族氢化物中最低的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】S和O可组成一系列负二价阴离子,结构如图。下列说法正确的是
| 硫酸根 | 焦硫酸根 | 过二硫酸根 | 硫代硫酸根 |
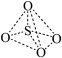 |  | 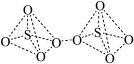 | 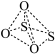 |
| A.电负性O>S,该系列离子中不存在非极性共价键 |
| B.焦硫酸钠溶于水所得溶液呈酸性 |
| C.硫酸根和硫代硫酸根空间构型均为正四面体 |
| D.过二硫酸根具有极强氧化性,原因是其中S元素处于+7价 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各物质中,按熔点由高到低的顺序排列正确的是
| A.CH4>SiH4>GeH4>SnH4 | B.KCl>NaCl>MgCl2>MgO |
| C.MgBr2<SiCl4<BN | D.金刚石>晶体硅>钠 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】部分短周期元素原子半径与原子序数的关系如图所示,下列说法错误的是
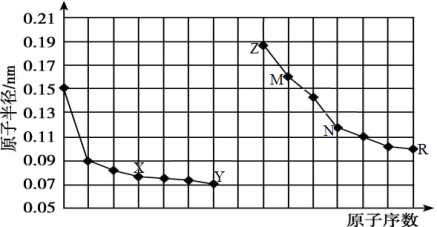

| A.最高价氧化物对应水化物的碱性:M<Z |
| B.组成单质的熔点:Z<M<N |
| C.Y、R 两种元素气态氢化物的还原性:Y>R |
| D.简单离子的半径:R>Y>M |
您最近一年使用:0次

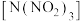 ,其结构如图所示。已知该分子中
,其结构如图所示。已知该分子中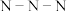 键角都是108.1°,下列有关说法不正确的是
键角都是108.1°,下列有关说法不正确的是
 萃取溴水中的
萃取溴水中的
 为正四面体形分子
为正四面体形分子 比
比 难转化成气态
难转化成气态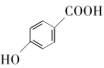 的沸点高于
的沸点高于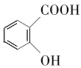
 分子不能形成氢键
分子不能形成氢键

