原子序数依次增大的五种元素的性质或结构信息如下表。
回答下列问题:
(1)T元素的原子结构示意图是___________ ,其三价阳离子的价电子轨道表示式为___________ 。
(2)五种元素中电负性最大与电负性最小的元素形成化合物的化学式为___________ ,基态W原子运动状态不同的电子数为___________ 。
(3)写出W元素与同周期相邻元素的第一电离能从大到小顺序:___________ ,Y元素与比其原子序数大8的元素,二者最高价氧化物对应的水化物酸性较强的是___________ (填化学式)。
(4)W的氢化物是有机化学反应的重要还原剂、火箭推进剂及氢燃料汽车中氢气的储存材料,遇水剧烈燃烧或爆炸,写出W的氢化物遇水释放出 的化学方程式:
的化学方程式:___________ 。
| 元素 | 原子结构和性质 |
| X | 基态原子s能级的电子总数是p能级电子总数的2倍 |
| Y | 其单质含有3对共用电子对 |
| Z | 大气中大量存在着两种单质,对人类生存都有重要意义 |
| W | 单质、最高价氧化物和最高价氧化物的水化物与盐酸或NaOH溶液都能反应 |
| T | 二价阳离子的电子排布式为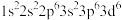 |
(1)T元素的原子结构示意图是
(2)五种元素中电负性最大与电负性最小的元素形成化合物的化学式为
(3)写出W元素与同周期相邻元素的第一电离能从大到小顺序:
(4)W的氢化物是有机化学反应的重要还原剂、火箭推进剂及氢燃料汽车中氢气的储存材料,遇水剧烈燃烧或爆炸,写出W的氢化物遇水释放出
 的化学方程式:
的化学方程式:
更新时间:2024/03/21 23:02:14
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】X、Y、Z、W、R是短周期元素,原子序数依次增大。非金属X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为_______ ;元素Z的离子结构示意图为_______ 。
(2)用电子式表示元素R氢化物的形成过程:_______ ;
(3)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为_______ 。
(4)元素W位于周期表的位置:_______ ,其非金属性比R弱,用原子结构的知识解释原因:_______ 。
(5)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与过量该氧化物反应的离子方程式:_______ 。
(1)元素X的最高价氧化物的电子式为
(2)用电子式表示元素R氢化物的形成过程:
(3)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为
(4)元素W位于周期表的位置:
(5)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与过量该氧化物反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F是核电荷数依次增大的六种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置______________________________________________
(2)F元素的最高价氧化物对应的水化物的化学式为___________________________________ 。
(3)元素C、D、E形成的简单离子半径由小到大的顺序________________________ (用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程:__________________________________________________ 。
C、D还可形成化合物D2C2,D2C2中含有的化学键是_________________________________________ 。
(5)C、E的氢化物,沸点由高到低顺序是:_______________________________ 。
(6)写出碳单质与E的最高价氧化物对应水化物浓溶液反应的化学方程式,并用单线桥标明电子的转移方向_______________ 。当转移电子为0.2mol时,标准状况下反应产生气体_______________ L。
(7)已知E单质和F单质的水溶液反应会生成两种强酸,其离子方程式为_________________ 。
(1)B在周期表中的位置
(2)F元素的最高价氧化物对应的水化物的化学式为
(3)元素C、D、E形成的简单离子半径由小到大的顺序
(4)用电子式表示化合物D2C的形成过程:
C、D还可形成化合物D2C2,D2C2中含有的化学键是
(5)C、E的氢化物,沸点由高到低顺序是:
(6)写出碳单质与E的最高价氧化物对应水化物浓溶液反应的化学方程式,并用单线桥标明电子的转移方向
(7)已知E单质和F单质的水溶液反应会生成两种强酸,其离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】元素①~⑩在周期表中的位置如表所示,回答下列问题:
(1)上述10种元素中,化学性质最不活泼的原子结构示意图为___________ ;与水反应最激烈的金属元素,其与水反应的化学方程式为___________ 。
(2)元素②的气态氢化物的电子式为___________ ;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是___________ (填化学式)。
(3)①②⑤元素的原子半径由小到大的顺序为___________ (用元素符号表示)。
(4)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式为___________ 。
(5)大气中的水蒸气在紫外线作用下会转化为活泼的 (羟基自由基,“·”表示1个电子)。
(羟基自由基,“·”表示1个电子)。 可看作催化剂,将
可看作催化剂,将 转化为
转化为 ,过程如下:
,过程如下: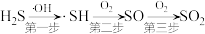 ,则第二步反应的方程式为
,则第二步反应的方程式为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)元素②的气态氢化物的电子式为
(3)①②⑤元素的原子半径由小到大的顺序为
(4)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式为
(5)大气中的水蒸气在紫外线作用下会转化为活泼的
 (羟基自由基,“·”表示1个电子)。
(羟基自由基,“·”表示1个电子)。 可看作催化剂,将
可看作催化剂,将 转化为
转化为 ,过程如下:
,过程如下: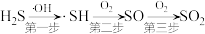 ,则第二步反应的方程式为
,则第二步反应的方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】废旧镍氢电池[主要含有大量的Ni、NiO、稀土金属(用RE表示)、Fe、Mg、Ca、 和
和 等],废旧镍氢电池中金属分离以及镍的回收流程如下。已知:
等],废旧镍氢电池中金属分离以及镍的回收流程如下。已知: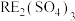 的溶解度大于
的溶解度大于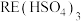 。
。
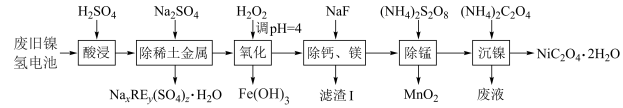
(1) 中S元素的化合价为
中S元素的化合价为_______ ,基态Ni原子的价层电子排布式为_______ ,“废液”中所含的主要盐的化学式为_______ 。
(2)Mn的第三电离能大于Fe的第三电离能的原因是_______ 。
(3)“酸浸”过程pH=2时稀土金属的浸出率最高,pH<2时浸出率低的原因是_______ 。
(4)“氧化”所发生反应的离子方程式为_______ 。
(5)“酸浸”后Mn元素都转化为 ,则“除锰”时发生反应的离子方程式为
,则“除锰”时发生反应的离子方程式为_______ 。
(6)“除钙、镁”步骤中,当溶液中 恰好完全沉淀时,滤液中
恰好完全沉淀时,滤液中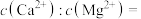
_______ 。常温时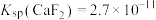 ,
,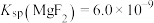 。
。
 和
和 等],废旧镍氢电池中金属分离以及镍的回收流程如下。已知:
等],废旧镍氢电池中金属分离以及镍的回收流程如下。已知: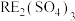 的溶解度大于
的溶解度大于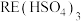 。
。
(1)
 中S元素的化合价为
中S元素的化合价为(2)Mn的第三电离能大于Fe的第三电离能的原因是
(3)“酸浸”过程pH=2时稀土金属的浸出率最高,pH<2时浸出率低的原因是
(4)“氧化”所发生反应的离子方程式为
(5)“酸浸”后Mn元素都转化为
 ,则“除锰”时发生反应的离子方程式为
,则“除锰”时发生反应的离子方程式为(6)“除钙、镁”步骤中,当溶液中
 恰好完全沉淀时,滤液中
恰好完全沉淀时,滤液中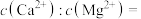
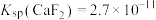 ,
,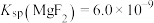 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素基态原子电子排布式为_______ 。
(2)用电子排布图表示F元素原子的价电子构型:_______ 。
(3)F、G元素对应的最高价含氧酸中酸性较强的酸的分子式为_______ 。
(4)离子半径:D+_______ B3-,第一电离能:B_______ C(填“<”“>”或“=”)
(5)A、C形成的一种“绿色”氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为_______ ,所含化学键类型_______
(6)写出E与D的最高价氧化物对应水化物反应的化学方程式:_______
(1)E元素基态原子电子排布式为
(2)用电子排布图表示F元素原子的价电子构型:
(3)F、G元素对应的最高价含氧酸中酸性较强的酸的分子式为
(4)离子半径:D+
(5)A、C形成的一种“绿色”氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为
(6)写出E与D的最高价氧化物对应水化物反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】有机物中的(C-H键较难断裂,活化C-H键是有机反应研究的热点之一、由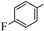 经两步反应合成
经两步反应合成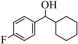 ,均需使C-H键活化,步骤如下:
,均需使C-H键活化,步骤如下:
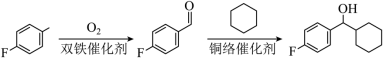
a.s区 b.d区 c.p区 d.ds区
(2)
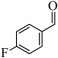 转化为
转化为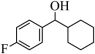 的过程中,C=O键中的
的过程中,C=O键中的 ”或“
”或“ ”)键断裂,发生加成反应,转化为C-O键。
”)键断裂,发生加成反应,转化为C-O键。(3)利用有机金属框架(MOF)构筑双铁催化剂,制备过程的核心结构变化如下。
注:FeII代表+2价铁,FeIII代表+3价铁。
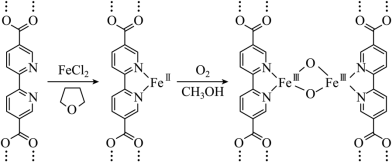
①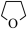 与
与 的相对分子质量相差较大,但二者的沸点却极为接近(相差1℃左右),原因有:ⅰ.
的相对分子质量相差较大,但二者的沸点却极为接近(相差1℃左右),原因有:ⅰ. 的极性强于
的极性强于 ;ⅱ.
;ⅱ.
(4)铜铬催化剂的主要成分是CuCl、CrCl2和CH3B(OH)2 (甲基硼酸)等,CH3B(OH)2能有效抑制副产物的生成。
①CH3B(OH)2中B的杂化轨道类型是
②已知:B(OH)3和CH3B(OH)2均为一元弱酸。推测Ka[B(OH)3]
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下图是元素周期表的一部分
(1)元素L的价电子排布图为__________ ,元素M的原子结构示意图为________ ,位于元素周期表五个区域中的_______ 区。上述元素中电负性最强的是_______ (用元素符号表示),C、D、E、F第一电离能的大小顺序为____________ (用元素符号表示)。
(2)D的氢化物和J氢化物沸点较高的是______ (填化学式),稳定性更强的是______ (填化学式)。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素I与元素B的单质有相似的性质。写出元素单质B与NaOH溶液反应的离子方程式___________________________ 。
(4)A、E、H、J四种元素的原子半径由大到小的排列顺序为___________________ ;E、F、H、K四种元素简单离子的半径由大到小的排列顺序为________________ 用元素符号表示)。
(5)能证明元素K比元素J的非金属性强的事实是______________ (填序号)。
A.常温下K单质的密度小于J单质的密度
B.K元素的气态氢化物比J元素的气态氢化物更稳定
C.K单质与氢气反应的程度比J单质与氢气反应的程度更剧烈
D.K元素的氧化物对应的水化物酸性强于J元素的氧化物对应的水化物
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| H | I | J | K | ||||||||||||||
| L | M | O |
(2)D的氢化物和J氢化物沸点较高的是
(3)某些不同族元素的性质也有一定的相似性,如上表中元素I与元素B的单质有相似的性质。写出元素单质B与NaOH溶液反应的离子方程式
(4)A、E、H、J四种元素的原子半径由大到小的排列顺序为
(5)能证明元素K比元素J的非金属性强的事实是
A.常温下K单质的密度小于J单质的密度
B.K元素的气态氢化物比J元素的气态氢化物更稳定
C.K单质与氢气反应的程度比J单质与氢气反应的程度更剧烈
D.K元素的氧化物对应的水化物酸性强于J元素的氧化物对应的水化物
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家利用锰簇催化剂(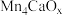 ,x代表氧原子数)解密光合作用。请回答下列问题:
,x代表氧原子数)解密光合作用。请回答下列问题:
(1)基态氧原子价电子排布式为___________ 。基态钙原子中,核外电子占据最高能层的符号是___________ 。
(2)在Mn、Cr中,第二电离能与第一电离能之差较小的是___________ (填“Mn”或“Cr”),理由是___________ 。
(3)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。 的配位数是
的配位数是___________ ,距离 最近的
最近的 有
有___________ 个。
②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在MnS晶胞坐标系中,1号 坐标为(0,0,0),3号
坐标为(0,0,0),3号 坐标为(1,1,1),则2号
坐标为(1,1,1),则2号 坐标为
坐标为___________ 。
③已知:MnS晶体的密度为 ,
, 为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为
为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为___________ pm(列出计算式即可)。
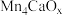 ,x代表氧原子数)解密光合作用。请回答下列问题:
,x代表氧原子数)解密光合作用。请回答下列问题:(1)基态氧原子价电子排布式为
(2)在Mn、Cr中,第二电离能与第一电离能之差较小的是
(3)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。

 的配位数是
的配位数是 最近的
最近的 有
有②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在MnS晶胞坐标系中,1号
 坐标为(0,0,0),3号
坐标为(0,0,0),3号 坐标为(1,1,1),则2号
坐标为(1,1,1),则2号 坐标为
坐标为③已知:MnS晶体的密度为
 ,
, 为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为
为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】前四周期元素结构信息见表,回答下列问题。
(1)A、B、C、E四种元素,第一电离能由大到小的顺序为_______ (用元素符号表示,下同)。A、B、C三种元素原子半径由大到小的顺序为_______ 。
(2)D在元素周期表中的位置_______ ,其基态原子的核外电子排布式为_______ 。
(3)写出B基态原子价电子的轨道式_______ 。
(4)E位于元素周期表的_______ 区,基态原子填有电子的轨道数为_______ 。
| 元素 | 结构信息 |
| A | 基态原子有6个原子轨道填充满电子,有3个未成对电子 |
| B | M层电子数比L层电子数少两个 |
| C | 基态原子有17个不同运动状态的电子 |
| D | 基态原子的价电子排布为3dx4s2,在常见化合物中其最高正价为+7 |
| E | 基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)D在元素周期表中的位置
(3)写出B基态原子价电子的轨道式
(4)E位于元素周期表的
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】2020年12月17日嫦娥五号返回器带回月球土壤样品。研究发现,月球土壤样品中存在铁、金、银、铅、锌、铜等矿物颗粒。请回答下列问题:
(1)基态Fe原子核外填充有电子的原子轨道数目为___________ ,基态 与
与 中未成对电子数之比为
中未成对电子数之比为___________ 。邻二氮菲(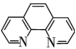 )中N原子可与
)中N原子可与 通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定
通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定 浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响
浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响___________ 。
(2)Zn在元素周期表中的位置为___________ ,其基态原子的M电子层中电子占据的最高能级是___________ 。
(3)我国科学家研究发现,十八胺在较高温度下具有一定的还原性,由于从十八胺中获得电子的能力不同,不同的金属盐在十八胺体系中反应可以得到不同的产物:
已知元素的电负性数据:
据此推测单一的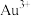 盐在十八胺体系中反应的产物为
盐在十八胺体系中反应的产物为___________ (写化学式)。
(1)基态Fe原子核外填充有电子的原子轨道数目为
 与
与 中未成对电子数之比为
中未成对电子数之比为 )中N原子可与
)中N原子可与 通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定
通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定 浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响
浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响(2)Zn在元素周期表中的位置为
(3)我国科学家研究发现,十八胺在较高温度下具有一定的还原性,由于从十八胺中获得电子的能力不同,不同的金属盐在十八胺体系中反应可以得到不同的产物:
| 单一金属盐 |  |  |
| 在十八胺体系中的产物 | ZnO | Ag |
| 元素 | Zn | Ag | Au |
| 电负性(鲍林标度) | 1.6 | 1.9 | 2.4 |
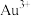 盐在十八胺体系中反应的产物为
盐在十八胺体系中反应的产物为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铁及其化合物广泛存在于人们的日常生活和工业生产中。回答下列问题:
(1)基态Fe原子的核外电子排布式是________ ,Ca元素与Fe元素同周期,灼烧 ,火焰为砖红色,节日中燃放的焰火配方中常含有Ca元素,灼烧Ca元素呈现特殊颜色的原因是
,火焰为砖红色,节日中燃放的焰火配方中常含有Ca元素,灼烧Ca元素呈现特殊颜色的原因是____
(2)人体内血红蛋白的结构简式如图所示:
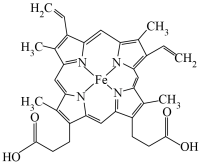
①组成血红蛋白的5种元素中,电负性由大到小的顺序是_________ ,C、N、O的第一电离能由大到小的顺序是_______ 。
②血红蛋白分子结构中N的杂化方式是_______ 。
③血红蛋白分子结构中含有配位键,为这些配位键提供孤电子对的元素是_______ (写元素符号,下同),提供空轨道的元素是______ 。
(3) 可应用于工业生产中的催化剂,其晶胞结构如图所示:
可应用于工业生产中的催化剂,其晶胞结构如图所示:

①已知电负性:Fe-1.83,Br-2.96,则 中含有的化学键类型为
中含有的化学键类型为_________ 。
② 晶胞中铁的配位数是
晶胞中铁的配位数是_________ ; 晶胞边长为a cm,则
晶胞边长为a cm,则 晶体密度的表达式为
晶体密度的表达式为_____________  (设阿伏加 德罗常数的值为NA)。
(设阿伏加 德罗常数的值为NA)。
(1)基态Fe原子的核外电子排布式是
 ,火焰为砖红色,节日中燃放的焰火配方中常含有Ca元素,灼烧Ca元素呈现特殊颜色的原因是
,火焰为砖红色,节日中燃放的焰火配方中常含有Ca元素,灼烧Ca元素呈现特殊颜色的原因是(2)人体内血红蛋白的结构简式如图所示:

①组成血红蛋白的5种元素中,电负性由大到小的顺序是
②血红蛋白分子结构中N的杂化方式是
③血红蛋白分子结构中含有配位键,为这些配位键提供孤电子对的元素是
(3)
 可应用于工业生产中的催化剂,其晶胞结构如图所示:
可应用于工业生产中的催化剂,其晶胞结构如图所示:
①已知电负性:Fe-1.83,Br-2.96,则
 中含有的化学键类型为
中含有的化学键类型为②
 晶胞中铁的配位数是
晶胞中铁的配位数是 晶胞边长为a cm,则
晶胞边长为a cm,则 晶体密度的表达式为
晶体密度的表达式为 (设阿伏加 德罗常数的值为NA)。
(设阿伏加 德罗常数的值为NA)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铜及其化合物的用途非常广泛。回答下列问题:
(1)实验室常用新制的 来检验醛基,反应原理为
来检验醛基,反应原理为 。
。
①基态铜原子的价电子排布式为___________ ,Cu成为阳离子时首先失去___________ 轨道上的电子。
② 中的中心原子的杂化轨道类型为
中的中心原子的杂化轨道类型为___________ ,HCHO分子中 键与
键与 键的个数之比为
键的个数之比为___________ 。
③上述反应中涉及的非金属元素的电负性由大到小的顺序为___________ (填元素符号)。
(2)黄铜矿(主要成分为 )是工业炼铜的主要原料,高温下灼烧黄铜矿,其发生的反应之一为
)是工业炼铜的主要原料,高温下灼烧黄铜矿,其发生的反应之一为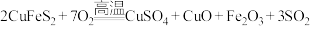 。
。
① 的空间结构为
的空间结构为___________ 。
② 中的中心原子S上的孤电子对数为
中的中心原子S上的孤电子对数为___________ 。
(3)磷化铜(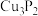 )用于制造磷青铜,某磷青铜的晶胞结构如图所示。
)用于制造磷青铜,某磷青铜的晶胞结构如图所示。

①该晶体中距离Cu原子最近的Cu原子有___________ 个。
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为___________ (用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值) 。
。
(1)实验室常用新制的
 来检验醛基,反应原理为
来检验醛基,反应原理为 。
。①基态铜原子的价电子排布式为
②
 中的中心原子的杂化轨道类型为
中的中心原子的杂化轨道类型为 键与
键与 键的个数之比为
键的个数之比为③上述反应中涉及的非金属元素的电负性由大到小的顺序为
(2)黄铜矿(主要成分为
 )是工业炼铜的主要原料,高温下灼烧黄铜矿,其发生的反应之一为
)是工业炼铜的主要原料,高温下灼烧黄铜矿,其发生的反应之一为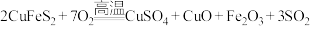 。
。①
 的空间结构为
的空间结构为②
 中的中心原子S上的孤电子对数为
中的中心原子S上的孤电子对数为(3)磷化铜(
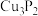 )用于制造磷青铜,某磷青铜的晶胞结构如图所示。
)用于制造磷青铜,某磷青铜的晶胞结构如图所示。
①该晶体中距离Cu原子最近的Cu原子有
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为
 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值) 。
。
您最近一年使用:0次



