按要求回答下列问题:
(1)下列B原子的电子排布式的状态中,能量最高的是________(用字母表示)。
(2)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,回答下列问题:
①基态Ge原子的简化的电子排布式为________ ,基态原子核外有________ 种空间运动状态。
②比较下列锗卤化物的熔点和沸点,分析呈现该变化规律的原因是________________________________ 。
③光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________ 。
(3)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子 的空间构型为
的空间构型为________ ,Na在空气中燃烧则发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为________ 光谱(填“发射”或“吸收”)。
(4)元素镍与镍钴合金的晶胞结构分别如图a、b所示:
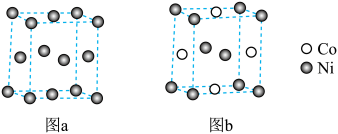
①镍钴合金若写作NixCo1-x,则图b合金中x=________
②已知晶胞(图a)的边长为m pm,设NA为阿伏加德罗常数的值,则镍的密度为________ g/cm3(列出计算式)。
(1)下列B原子的电子排布式的状态中,能量最高的是________(用字母表示)。
A. | B.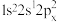 | C. | D.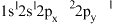 |
(2)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,回答下列问题:
①基态Ge原子的简化的电子排布式为
②比较下列锗卤化物的熔点和沸点,分析呈现该变化规律的原因是
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(3)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子
 的空间构型为
的空间构型为(4)元素镍与镍钴合金的晶胞结构分别如图a、b所示:

①镍钴合金若写作NixCo1-x,则图b合金中x=
②已知晶胞(图a)的边长为m pm,设NA为阿伏加德罗常数的值,则镍的密度为
更新时间:2024-03-28 14:41:11
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有一混合溶液,只可能含有以下离子中的若干种:H+、Na+、K+、Cl-、Ca2+、 、
、 ,取少量该混合溶液进行如下实验。
,取少量该混合溶液进行如下实验。
实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,火焰为黄色;
实验②:向混合溶液中加入足量BaCl2溶液后,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解,产生气泡;
实验④:向②过滤后的溶液加入硝酸银,产生白色沉淀。
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液中一定含有___________ (填离子符号,下同)
(2)由实验②③推断该混合溶液中一定含有___________ ,一定不含有___________ 。请写出实验③中反应的离子方程式:___________
(3)综合上述实验,是否能确定该混合溶液中含有Cl-:___________ (填“是”或“否”)。若“是”本空无需作答,若“否”请写出检验该混合溶液中Cl-的实验操作及现象:___________ 。
 、
、 ,取少量该混合溶液进行如下实验。
,取少量该混合溶液进行如下实验。实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,火焰为黄色;
实验②:向混合溶液中加入足量BaCl2溶液后,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解,产生气泡;
实验④:向②过滤后的溶液加入硝酸银,产生白色沉淀。
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液中一定含有
(2)由实验②③推断该混合溶液中一定含有
(3)综合上述实验,是否能确定该混合溶液中含有Cl-:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知化合物A、D、E、G焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多。A~H各物质的变化关系如下图所示。

(1)写出各步反应的化学方程式
反应①______________________________________
反应②______________________________________
反应③______________________________________
反应④______________________________________
反应⑤______________________________________
(2)上述反应中属于氧化还原反应的有__________________________ 。

(1)写出各步反应的化学方程式
反应①
反应②
反应③
反应④
反应⑤
(2)上述反应中属于氧化还原反应的有
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有A、B两种氧化物,焰色试验均为黄色,其转化关系如下图所示(其他物质均已略去)。请回答下列问题:
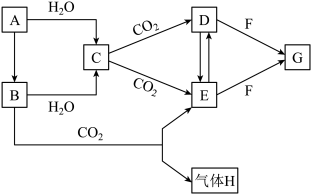
(1)写出A的化学式:___________ 。
(2)写出B→C的化学方程式:___________ 。
(3)B可与 反应生成E与气体H,该反应在生活中可用于
反应生成E与气体H,该反应在生活中可用于___________ 。
(4)有同学提议可用 溶液鉴别D与E,你认为该方案
溶液鉴别D与E,你认为该方案___________ (填“可行”或“不可行”),原因是___________ 。
(5)D与E可互相转化,请写出E→D的化学方程式:___________ 。
(6)若F为人体胃液中的主要成分,则G为___________ 。

(1)写出A的化学式:
(2)写出B→C的化学方程式:
(3)B可与
 反应生成E与气体H,该反应在生活中可用于
反应生成E与气体H,该反应在生活中可用于(4)有同学提议可用
 溶液鉴别D与E,你认为该方案
溶液鉴别D与E,你认为该方案(5)D与E可互相转化,请写出E→D的化学方程式:
(6)若F为人体胃液中的主要成分,则G为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】前四周期元素A、B、C、D、E、F的原子序数依次增大,部分信息如表所示。
回答下列问题:
(1)基态A原子电子云轮廓图为_______ 形。
(2)基态C原子核外电子占据_______ 个轨道。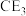 分子的空间结构为
分子的空间结构为_______ 。
(3)A、B、D、E能组成多种化合物,其中相对分子质量最小的手性分子是_______ (填结构式)。
(4)配合物 含
含_______ 种(填数字)配体,含1mol该配合物的水溶液最多能与_______ 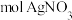 反应。
反应。
(5)化合物BD的沸点_______  (填“高于”或“低于”),原因是
(填“高于”或“低于”),原因是_______ 。
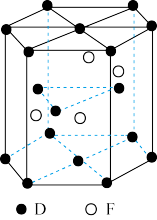
(6)F、D组成的一种晶体的晶胞结构如图所示,该晶体的化学式为_______ 。
| 代号 | 部分信息 |
| A | 元素正、负化合价的绝对值相等 |
| B | 目前公认的形成化合物种类最多的元素 |
| C | 气态氢化物能使湿润的红色石蕊试纸变蓝色 |
| D | 基态原子最外层电子排布式为 |
| E | 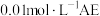 溶液的 溶液的 |
| F | 基态原子价层电子排布式为 |
(1)基态A原子电子云轮廓图为
(2)基态C原子核外电子占据
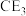 分子的空间结构为
分子的空间结构为(3)A、B、D、E能组成多种化合物,其中相对分子质量最小的手性分子是
(4)配合物
 含
含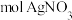 反应。
反应。(5)化合物BD的沸点
 (填“高于”或“低于”),原因是
(填“高于”或“低于”),原因是(6)F、D组成的一种晶体的晶胞结构如图所示,该晶体的化学式为

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有五种元素,其中A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)B元素基态原子中能量最高的电子的电子云在空间有_______ 个伸展方向,原子轨道呈_______ 形。
(2)E位于第_______ 族_______ 区,该元素原子的核外电子排布式为_______ 。
(3)已知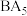 为离子化合物,写出其电子式:
为离子化合物,写出其电子式:_______ 。
(4)检验D元素的方法是_______ ,请用原子结构的知识解释产生此现象的原因:_______ 。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
C元素的第一至第四电离能如下: 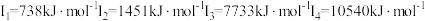 |
| D是前四周期中电负性最小的元素 |
| E在周期表的第七列 |
(2)E位于第
(3)已知
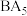 为离子化合物,写出其电子式:
为离子化合物,写出其电子式:(4)检验D元素的方法是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、L四种元素分别位于周期表中三个紧相邻的周期且原子序数依次增大,它们相关信息如下:X元素原子的价电子构型为nsnnp2n,Y和Z位于同一周期,最外层都有两个未成对电子,L元素原子的基态未成对电子数是同周期最多的元素。
请回答如下问题:
(1)L元素在周期表中的位置是_______________ ,该原子核外电子排布式是_______________ ,其最高正价氧化物对应的水氧化物的化学式是_______________ ;
(2)元素X与Y形成的化合物晶体类型是晶体_________ ,1mol该化合物含有的化学键数为___________ (用阿伏加德罗常数NA表示);
(3)元素M是周期表中电负性最强的元素,X与M形成的化合物XM2的分子几何构型是________ ,该化合物中X的原子的杂化轨道类型是____________ ;
(4)X与碳、氢、三种元素形成的相对分子质量最小的分子里有个____ δ键,____ 个π键;
(5)金属元素N与Z形成的离子化合物的晶胞结构如图,晶胞中Z离子数目为______ 。
请回答如下问题:
(1)L元素在周期表中的位置是
(2)元素X与Y形成的化合物晶体类型是晶体
(3)元素M是周期表中电负性最强的元素,X与M形成的化合物XM2的分子几何构型是
(4)X与碳、氢、三种元素形成的相对分子质量最小的分子里有个
(5)金属元素N与Z形成的离子化合物的晶胞结构如图,晶胞中Z离子数目为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】现有属于前4周期的元素A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价阳离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)D的元素名称___________ 。
(2)A、B、C三种元素电负性由大到小的顺序为___________ (用元素符号表示),第一电离能D___________ Al(填“>”、“<”或“=”)
(3)C元素原子的电子轨道表示式为_______ ,E元素在元素周期表中的位置_________ 。
(4)F元素位于元素周期表的_______ 区,其基态原子简化的电子排布式为________ 。
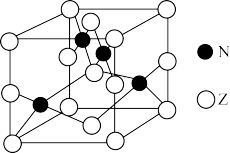
(5)B和G形成分子W的结构如图所示,化合物W的分子式为___________ ,B、G原子的杂化类型分别为___________ 、___________ 。
(1)D的元素名称
(2)A、B、C三种元素电负性由大到小的顺序为
(3)C元素原子的电子轨道表示式为
(4)F元素位于元素周期表的
(5)B和G形成分子W的结构如图所示,化合物W的分子式为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。请回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为___________ 。
(2)根据价层电子对互斥模型, 的空间构型为
的空间构型为 ___________ ,与 互为等电子体的离子、分子有
互为等电子体的离子、分子有 ___________ 、___________ (各写1个)。
(3)Sn的原子序数为50,与碳同主族,基态Sn原子的价电子排布图为___________ 。
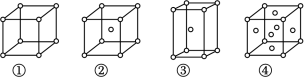
(4)金属铜在元素周期表___________ 区,采用下列 ___________ 堆积方式(填序号)。
(5)Cu2+可以与乙二胺(H2N﹣CH2CH2﹣NH2)形成配离子(如图)。H、O、N三种元素的电负性从大到小的顺序为___________ ,乙二胺分子中N原子成键时采取的杂化类型是 ___________ 。

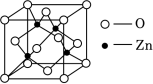
(6)锌与氧形成的ZnO晶体具有四种晶体结构,其中闪锌矿结构与金刚石相似,晶胞如图所示。该ZnO晶体熔点远远高于干冰,原因是___________ ,晶胞参数为apm,该晶体密度为 ___________ g•cm﹣3(写出表达式)。
(1)基态S原子的价电子中,两种自旋状态的电子数之比为
(2)根据价层电子对互斥模型,
 的空间构型为
的空间构型为  互为等电子体的离子、分子有
互为等电子体的离子、分子有 (3)Sn的原子序数为50,与碳同主族,基态Sn原子的价电子排布图为
(4)金属铜在元素周期表

(5)Cu2+可以与乙二胺(H2N﹣CH2CH2﹣NH2)形成配离子(如图)。H、O、N三种元素的电负性从大到小的顺序为

(6)锌与氧形成的ZnO晶体具有四种晶体结构,其中闪锌矿结构与金刚石相似,晶胞如图所示。该ZnO晶体熔点远远高于干冰,原因是

您最近半年使用:0次
【推荐3】2017年4月26日,海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为___________ ,同一周期中与基态Ni原子有相同的未成对电子数目的原子有___________ 种(填数字)。
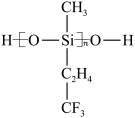
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图所示)。其O原子杂化方式为___________ 杂化,元素C、O、F、Si的电负性由大到小的顺序为___________ 。
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是___________ (填元素符号)
②根据价层电子对互斥理论,预测ClO3-的空间构型为___________ 形,写出一个C1O2-的等电子体的化学符号___________ 。
③已知HClO3酸性强于HClO,从结构上分析其原因是___________ 。
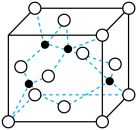
(4)海底金属软泥是在洋海底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。Zn2+与S2-形成的一种晶体结构如图所示(黑球表示Zn2+,白球表示S2-)。则该晶胞中六个面心的离子围成的立体图形为___________ 。已知该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,该晶体中Zn2+和S2-之间的最短距离为体对角线的 ,则该晶体中S2-和Zn2+之间的最短距离为
,则该晶体中S2-和Zn2+之间的最短距离为___________ nm。(写出计算式即可)
(1)镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图所示)。其O原子杂化方式为

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是
| 元素 | 氟 | 氯 | 溴 | 碘 |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
②根据价层电子对互斥理论,预测ClO3-的空间构型为
③已知HClO3酸性强于HClO,从结构上分析其原因是
(4)海底金属软泥是在洋海底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。Zn2+与S2-形成的一种晶体结构如图所示(黑球表示Zn2+,白球表示S2-)。则该晶胞中六个面心的离子围成的立体图形为
 ,则该晶体中S2-和Zn2+之间的最短距离为
,则该晶体中S2-和Zn2+之间的最短距离为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】建盏由建阳坯土、天然矿物釉烧制,含有SiO2、Al2O3、Fe2O3、FeO、CaO、TiO2等化学成分。
(1)现代化学可利用_______ 特征谱线来鉴定建盏中的元素。
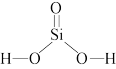
(2)建盏胎釉中含SiO2是硅酸的酸酐。硅酸结构式如图所示,硅原子的杂化方式_______ 。
(3)Fe2+与蛋白质链上咪唑环通过配位键连接形成的物质结构如图所示。A、W、X、Y为短周期前10号主族元素。四种元素的电负性由大到小的顺序为_______ (用元素符号表示)。
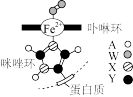
(4)元素Fe在周期表中的位置为_______ ;其第三电离能(I3)为2957 KJ· mol-1、第四电离能(I4)为5290 KJ· mol-1,I4远大于I3的原因为_______ 。
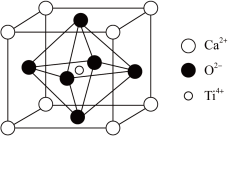
(5)建盏胎釉矿石中的钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的_______ 空隙中,在钙钛矿晶胞结构的另一种表示中,Ti4+处于各顶角位置,则O2-处于_______ 位置(选填“面心”“体心”或“棱心”)。已知晶胞密度为 ρ g∙cm-3,则两个O2-离子间的最短距离为_______ nm(阿伏加德罗常数的值为NA,列出表达式)。
(1)现代化学可利用
(2)建盏胎釉中含SiO2是硅酸的酸酐。硅酸结构式如图所示,硅原子的杂化方式

(3)Fe2+与蛋白质链上咪唑环通过配位键连接形成的物质结构如图所示。A、W、X、Y为短周期前10号主族元素。四种元素的电负性由大到小的顺序为

(4)元素Fe在周期表中的位置为
(5)建盏胎釉矿石中的钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】央视报道《王者归“铼”》:中国发现超级金属“铼”,飞机火箭上天全靠它,有望打破美国垄断。
(1)铼(Re)被称为类锰元素,与锰的外围电子结构数相同,已知Mn的外围电子排布式为3d54s2,写出75Re的外围电子排布式:______ ,其最高价氧化物的化学式为_______ 。
(2)铢合金可作为醇脱氢反应的催化剂:CH3OH HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是
HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是______ 和_______ 。C、H、O三种元素中,电负性最大的是______ (填元素符号)。
(3)实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O 2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。

上述反应中S2O82-断裂的共价键类型为___ (填“σ键”或“π键”),每生成0.3molMnO4-,过硫酸根中断裂的共价键数目为_____ NA。
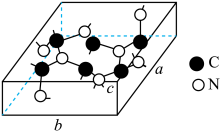
(4)科学家研制出一种新型的超硬材料,类似于金刚石的结构,但硬度比金刚石大,该晶体元素组成为C和N,其晶胞如图所示(图示原子都包含在晶胞内),则该晶胞所含氮原子的个数为____ 。已知晶胞参数分别为a nm、b nm、c nm,,该晶体的摩尔质量为Mg·mol-1,密度为ρg·cm-3,则阿伏加 德罗常数的数值为___ (用含a、b、c、ρ、M的代数式表示)。
(1)铼(Re)被称为类锰元素,与锰的外围电子结构数相同,已知Mn的外围电子排布式为3d54s2,写出75Re的外围电子排布式:
(2)铢合金可作为醇脱氢反应的催化剂:CH3OH
 HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是
HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是(3)实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O
 2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
上述反应中S2O82-断裂的共价键类型为
(4)科学家研制出一种新型的超硬材料,类似于金刚石的结构,但硬度比金刚石大,该晶体元素组成为C和N,其晶胞如图所示(图示原子都包含在晶胞内),则该晶胞所含氮原子的个数为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氮化硼(BN)晶体有多种结构。回答下列问题:
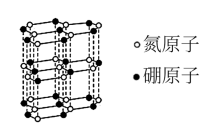
(1)六方氮化硼的结构与石墨相似(如图所示),具有层状结构,可作高温润滑剂。该晶体中存在的作用力类型有___________ ,六方氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为___________ 。
(2)六方氮化硼在高温高压下,可以转化为立方氮化硼(如图所示),立方氮化硼密度为 ,该c原子的坐标参数为
,该c原子的坐标参数为 ,e为(
,e为( ,
, ,0),f为(
,0),f为( ,0,
,0, )。
)。
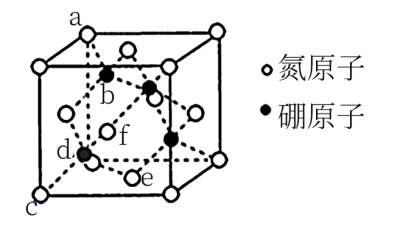
①由题干所给的坐标参数知,d原子的坐标参数为________ 。
②B原子填充在N原子的四面体空隙,且占据此类空隙的比例为________ 。
③a位置N原子与b位置B原子的距离为_______ cm。
(1)六方氮化硼的结构与石墨相似(如图所示),具有层状结构,可作高温润滑剂。该晶体中存在的作用力类型有

(2)六方氮化硼在高温高压下,可以转化为立方氮化硼(如图所示),立方氮化硼密度为
 ,该c原子的坐标参数为
,该c原子的坐标参数为 ,e为(
,e为( ,
, ,0),f为(
,0),f为( ,0,
,0, )。
)。
①由题干所给的坐标参数知,d原子的坐标参数为
②B原子填充在N原子的四面体空隙,且占据此类空隙的比例为
③a位置N原子与b位置B原子的距离为
您最近半年使用:0次



