室温下,某刚性密闭容器中按体积比1:2充入X(g)和Y(g),发生反应X(g)+ Y(g) P(g)+Q(g)。下图表示该反应的历程, M(g)和N(g)均是中间产物。下列说法错误的是
P(g)+Q(g)。下图表示该反应的历程, M(g)和N(g)均是中间产物。下列说法错误的是
 P(g)+Q(g)。下图表示该反应的历程, M(g)和N(g)均是中间产物。下列说法错误的是
P(g)+Q(g)。下图表示该反应的历程, M(g)和N(g)均是中间产物。下列说法错误的是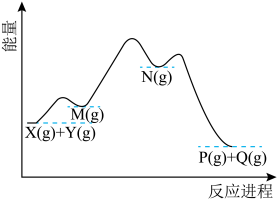
| A.反应的历程分3步进行 |
| B.反应过程中,N比M所能达到的最高浓度更大 |
| C.反应达到平衡时,升高温度, X的浓度增大 |
| D.若初始时,按体积比2:1充入X(g)和Y(g),其他条件不变,平衡时P(g)的百分含量不变 |
2024·河北石家庄·二模 查看更多[2]
更新时间:2024-04-13 16:05:36
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。对该反应的有关叙述正确的是


| A.该反应的正反应为吸热反应 |
| B.催化剂能改变反应的焓变 |
| C.催化剂不能降低反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知反应NO2(g)+CO(g)=NO(g) +CO2(g)的能量变化如图所示,下列说法正确的是
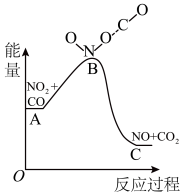

| A.图中A→B的过程为放热过程 |
| B.该反应为氧化还原反应 |
| C.1molNO2和1molCO的键能总和大于1molNO和1mol CO2的键能总和 |
| D.1molNO2(g)和1molCO(g)的总能量低于1mol NO(g) 和1mol CO2(g)的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】升高温度能加快反应速率地主要原因是( )
| A.活化分子的能量明显增加 | B.降低了反应的活化能 |
| C.增加了活化分子的百分数 | D.改变了化学反应的能量变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列说法正确的是
| A.增大反应物浓度,可以提高活化分子百分数 |
| B.通过压缩体积增大压强,可提高单位体积内活化分子数,从而提高反应速率 |
| C.升高温度能加快反应,可以提高反应热 |
| D.反应物分子的每一次碰撞都是有效碰撞 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】已知:N2(g)+3H2(g)  2NH3(g) △H=−92.4 kJ∙mol−1。在一个密闭容器内,加入反应物为N2和H2物质的量分别为1mol和3mol,在不同压强和温度下,反应达到平衡时,体系中NH3的物质的量分数如表:
2NH3(g) △H=−92.4 kJ∙mol−1。在一个密闭容器内,加入反应物为N2和H2物质的量分别为1mol和3mol,在不同压强和温度下,反应达到平衡时,体系中NH3的物质的量分数如表:
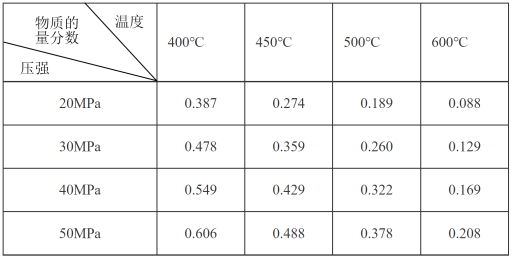
根据表中数据,下列说法正确的是
 2NH3(g) △H=−92.4 kJ∙mol−1。在一个密闭容器内,加入反应物为N2和H2物质的量分别为1mol和3mol,在不同压强和温度下,反应达到平衡时,体系中NH3的物质的量分数如表:
2NH3(g) △H=−92.4 kJ∙mol−1。在一个密闭容器内,加入反应物为N2和H2物质的量分别为1mol和3mol,在不同压强和温度下,反应达到平衡时,体系中NH3的物质的量分数如表:
根据表中数据,下列说法正确的是
| A.升高温度,平衡逆向移动,逆反应速率增大,正反应速率减小 |
| B.反应达到平衡时,放出的热量均等于92.4 kJ |
| C.在不同温度和压强下,反应达到平衡时,NH3的物质的量分数可以相等 |
| D.在400℃,50MPa条件下,在反应开始到平衡的时间为20min,则氨气反应速率为0.075mol·L−1·min−1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在密闭容器中进行反应:2A(g)+B(g) 3C(g) △H,不同温度下测得C的百分含量与时间的关系如图所示。下列判断正确的是
3C(g) △H,不同温度下测得C的百分含量与时间的关系如图所示。下列判断正确的是
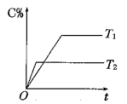
 3C(g) △H,不同温度下测得C的百分含量与时间的关系如图所示。下列判断正确的是
3C(g) △H,不同温度下测得C的百分含量与时间的关系如图所示。下列判断正确的是
| A.T1>T2 △H>0 | B.T1<T2 △H>0 |
| C.T1>T2 △H<0 | D.T1<T2 △H<0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】2NO(g)+O2(g) 2NO2(g) 分两步进行:2NO(g)
2NO2(g) 分两步进行:2NO(g)  N2O2(g)、N2O2(g)+O2(g)
N2O2(g)、N2O2(g)+O2(g)  2NO2(g),反应过程中的能量变化如图所示。往体积相等的刚性容器甲、乙中分别充入2mol NO(g)和1molO2(g),其中甲控制温度为T1,乙控制温度为T2测得甲、乙容器中n(NO2)随时间(t)的变化如表所示,下列说法不正确的是
2NO2(g),反应过程中的能量变化如图所示。往体积相等的刚性容器甲、乙中分别充入2mol NO(g)和1molO2(g),其中甲控制温度为T1,乙控制温度为T2测得甲、乙容器中n(NO2)随时间(t)的变化如表所示,下列说法不正确的是

 2NO2(g) 分两步进行:2NO(g)
2NO2(g) 分两步进行:2NO(g)  N2O2(g)、N2O2(g)+O2(g)
N2O2(g)、N2O2(g)+O2(g)  2NO2(g),反应过程中的能量变化如图所示。往体积相等的刚性容器甲、乙中分别充入2mol NO(g)和1molO2(g),其中甲控制温度为T1,乙控制温度为T2测得甲、乙容器中n(NO2)随时间(t)的变化如表所示,下列说法不正确的是
2NO2(g),反应过程中的能量变化如图所示。往体积相等的刚性容器甲、乙中分别充入2mol NO(g)和1molO2(g),其中甲控制温度为T1,乙控制温度为T2测得甲、乙容器中n(NO2)随时间(t)的变化如表所示,下列说法不正确的是 
 | 10min | 20min | ∞ |
| T1 | a1 | 0.6 | 1.0 |
| T2 | a2 | 0.3 | 0.8 |
| A.a₁>0.3 |
| B.反应过程中N2O2的浓度先增大后减小 |
| C.乙容器20 min 时 NO2物质的量较少的原因是乙中 N2O2的活化分子百分数较小 |
| D.平衡时从甲容器移走部分 NO2,重新平衡时甲中 NO2的体积分数可能与乙相等 |
您最近一年使用:0次