回答下列问题。
(1)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L‒1·min‒1,则以物质B表示此反应的化学反应速率为___________ 。
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为___________ 。
(3)①将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有___________ mol A,此时C的物质的量浓度为___________ 。
②能说明该反应已达到平衡状态的是_______ (填字母)。
a.v(A)=2v(B) b.容器内压强保持不变
c.3v逆(A)=v正(B) d.容器内混合气体的密度保持不变
③在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是_______ (填序号)。
①降低温度 ②加入催化剂 ③增大容器体积
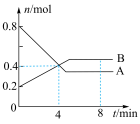
(4)在2 L的恒温恒容密闭容器内,某一反应中A、B气体的物质的量随时间变化的曲线如图所示,从反应开始至4 min时,B的平均反应速率为___________ ,该反应的化学方程式为___________ 。
(1)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L‒1·min‒1,则以物质B表示此反应的化学反应速率为
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为
(3)①将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)
 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有②能说明该反应已达到平衡状态的是
a.v(A)=2v(B) b.容器内压强保持不变
c.3v逆(A)=v正(B) d.容器内混合气体的密度保持不变
③在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入催化剂 ③增大容器体积
(4)在2 L的恒温恒容密闭容器内,某一反应中A、B气体的物质的量随时间变化的曲线如图所示,从反应开始至4 min时,B的平均反应速率为
更新时间:2024-04-15 09:57:56
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】以下是关于化学反应2SO2+O2⇌2SO3的两个素材情景:
素材1:某温度和压强下,2 升 密闭容器中,不同时间点测密闭体系中三种物质的物质的量
素材2:反应在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的物质的量分数,SO2的转化率越大,化学反应的限度越大)
根据两个素材回答问题:
(1)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应速率为_______ mol·L-1·s-1。
(2)根据素材2中分析得到,温度升高,SO2的转化率_______ (选填“增大”、“不变”或“减小”);压强增大,SO2的转化率_______ (选填“增大”、“不变”或“减小”)。
(3)在恒温恒容 的密闭容器中,发生反应2SO2(g)+O2(g)⇌2SO3(g),当下列物理量不再发生变化时,一定能证明2SO2(g)+O2(g) ⇌2SO3(g)达到平衡状态的是_______ (填序号)。
①混合气体的压强 ②混合气体的密度
③混合气体的总物质的量 ④混合气体的平均相对分子质量
素材1:某温度和压强下,
 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| SO2 | 1 | 0.7 | 0.5 | 0.35 | 0.2 | 0.1 | 0.1 | 0.1 |
| O2 | 0.5 | 0.35 | 0.25 | 0.18 | 0.1 | 0.05 | 0.05 | 0.05 |
| SO3 | 0 | 0.3 | 0.5 | 0.65 | 0.8 | 0.9 | 0.9 | 0.9 |
素材2:反应在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的物质的量分数,SO2的转化率越大,化学反应的限度越大)
 | 0.1 MPa | 0.5 MPa | 1 MPa | 10 MPa |
| 400 ℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 ℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 ℃ | 73.7 | 85.8 | 90.0 | 96.4 |
根据两个素材回答问题:
(1)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应速率为
(2)根据素材2中分析得到,温度升高,SO2的转化率
(3)在
①混合气体的压强 ②混合气体的密度
③混合气体的总物质的量 ④混合气体的平均相对分子质量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图1所示。根据图中数据,填写下列空白。
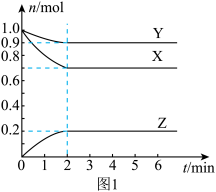
(1)该反应的化学方程式为________________________________________ 。
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=________ 。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________ 倍。
②若此时将容器的体积缩小为原来的 ,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________ (填“放热”或“吸热”)反应。
(4)上述反应在t1~t6内反应速率与时间图象如图2所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是________ (填字母)。

A.在t1时增大了压强
B.在t3时加入催化剂
C.在t4时降低了温度
D.t2~t3时X的转化率最高

(1)该反应的化学方程式为
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的
②若此时将容器的体积缩小为原来的
 ,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为(4)上述反应在t1~t6内反应速率与时间图象如图2所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是

A.在t1时增大了压强
B.在t3时加入催化剂
C.在t4时降低了温度
D.t2~t3时X的转化率最高
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列填空
(1)25℃时,将该pH=13Ba(OH)2溶液与pH=2的HCl溶液混合,若所得混合溶液pH=7,则Ba(OH)2溶液与HCl溶液的体积比为___________ 。
(2)二甲醚(分子式C2H6O)可作燃料电池的燃料,以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。请写出该电池中负极上的电极反应式是:___________ 。
(3)草酸分解所需燃料可以是CO,通过甲烷制备CO: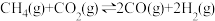
 。常温下,在2L的密闭容器中通入4molCH4气体和6molCO2气体发生反应,5min后达到平衡,测得CO气体的浓度为
。常温下,在2L的密闭容器中通入4molCH4气体和6molCO2气体发生反应,5min后达到平衡,测得CO气体的浓度为 。
。
①平衡时,该反应的平均反应速率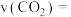
___________ 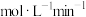 。
。
②在不改变反应混合物用量的前提下,为了提高CH4气体的转化率,可采取的措施是___________ 。
(4)含有Cr2O 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含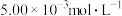 的Cr2O
的Cr2O 。为使废水能达标排放,做如下处理:
。为使废水能达标排放,做如下处理: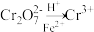 、
、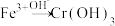 、
、 。若处理后的废水中残留的
。若处理后的废水中残留的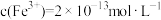 ,则残留的Cr3+的浓度为
,则残留的Cr3+的浓度为___________ mol/L(已知: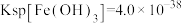 ,
,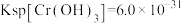 。
。
(1)25℃时,将该pH=13Ba(OH)2溶液与pH=2的HCl溶液混合,若所得混合溶液pH=7,则Ba(OH)2溶液与HCl溶液的体积比为
(2)二甲醚(分子式C2H6O)可作燃料电池的燃料,以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。请写出该电池中负极上的电极反应式是:
(3)草酸分解所需燃料可以是CO,通过甲烷制备CO:
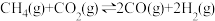
 。常温下,在2L的密闭容器中通入4molCH4气体和6molCO2气体发生反应,5min后达到平衡,测得CO气体的浓度为
。常温下,在2L的密闭容器中通入4molCH4气体和6molCO2气体发生反应,5min后达到平衡,测得CO气体的浓度为 。
。①平衡时,该反应的平均反应速率
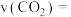
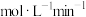 。
。②在不改变反应混合物用量的前提下,为了提高CH4气体的转化率,可采取的措施是
(4)含有Cr2O
 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含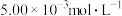 的Cr2O
的Cr2O 。为使废水能达标排放,做如下处理:
。为使废水能达标排放,做如下处理: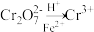 、
、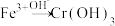 、
、 。若处理后的废水中残留的
。若处理后的废水中残留的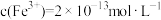 ,则残留的Cr3+的浓度为
,则残留的Cr3+的浓度为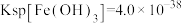 ,
,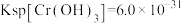 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知NO2和N2O4可以相互转化: 2NO2(g)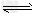 N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭容器中,物质浓度随时间变化关系如图所示,回答下列问题:
N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭容器中,物质浓度随时间变化关系如图所示,回答下列问题:
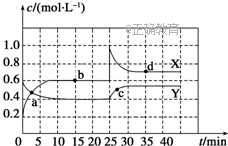
(1)图中共有两条曲线X和Y,其中曲线________ 表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是________ 。
(2)反应进行至25 min时,曲线发生变化的原因是_______________________ ;前10 min内用NO2表示的化学反应速率 (NO2)=
(NO2)=___________ mol/(L·min);
d点的平衡常数的数值是________________ (计算结果保留一位小数)。
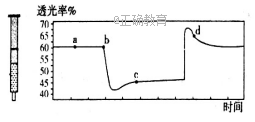
(3)恒温恒容条件下,下列选项一定可以判断反应2NO2(g)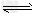 N2O4(g)达到平衡状态的依据有
N2O4(g)达到平衡状态的依据有_______ ;
a.混合气体颜色不变 b.混合气体的密度保持不变
c. (NO2)=2
(NO2)=2 (N2O4) d.混合气体的平均相对分子质量保持不变
(N2O4) d.混合气体的平均相对分子质量保持不变
达到平衡状态后,恒温恒容条件下再充入一定量NO2,[NO2]/[N2O4]比值___________ 选填“增大”、“减小”、“不变”)。
(4)将一定量的NO2充入注射器中后封口,下图是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是_____________
A.b点的操作是压缩注射器
B.c点与a点相比,C(NO2)增大,C(N2O4)减小
C.若不忽略体系温度变化,且没有能量损失,则b、c两点的平衡常数Kb>Kc
D.d点: (正)>
(正)>  (逆)
(逆)
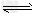 N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭容器中,物质浓度随时间变化关系如图所示,回答下列问题:
N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭容器中,物质浓度随时间变化关系如图所示,回答下列问题:
(1)图中共有两条曲线X和Y,其中曲线
(2)反应进行至25 min时,曲线发生变化的原因是
 (NO2)=
(NO2)=d点的平衡常数的数值是
(3)恒温恒容条件下,下列选项一定可以判断反应2NO2(g)
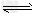 N2O4(g)达到平衡状态的依据有
N2O4(g)达到平衡状态的依据有a.混合气体颜色不变 b.混合气体的密度保持不变
c.
 (NO2)=2
(NO2)=2 (N2O4) d.混合气体的平均相对分子质量保持不变
(N2O4) d.混合气体的平均相对分子质量保持不变达到平衡状态后,恒温恒容条件下再充入一定量NO2,[NO2]/[N2O4]比值
(4)将一定量的NO2充入注射器中后封口,下图是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是

A.b点的操作是压缩注射器
B.c点与a点相比,C(NO2)增大,C(N2O4)减小
C.若不忽略体系温度变化,且没有能量损失,则b、c两点的平衡常数Kb>Kc
D.d点:
 (正)>
(正)>  (逆)
(逆)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)对于反应3X(g)+Y(g)⇌Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
①升高温度_______ ;②加入催化剂_______ ;
③保持容器的体积不变,减少气体Z的量:_______ ;
④保持容器的体积不变,增加气体Ar_______ ;
⑤保持压强不变,充入惰性气体_______ ;
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
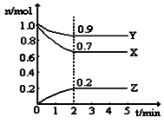
①该反应的化学方程式为_______ 。
②反应开始至2min,以气体Z表示的平均反应速率为_______ 。
③2min反应达平衡容器内混合气体的平均相对分子质量比起始时_______ (填“大”,“小”或“相等”,下同),混合气体密度比起始时_______ 。
(3)反应3A(g)+B(g)⇌2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(L·min)、②vC=0.5 mol/(L·min)、③vB=0.5 mol/(L·min),三种情况下该反应速率由大到小的关系是_______ 。(用序号表示)
①升高温度
③保持容器的体积不变,减少气体Z的量:
④保持容器的体积不变,增加气体Ar
⑤保持压强不变,充入惰性气体
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为
②反应开始至2min,以气体Z表示的平均反应速率为
③2min反应达平衡容器内混合气体的平均相对分子质量比起始时
(3)反应3A(g)+B(g)⇌2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(L·min)、②vC=0.5 mol/(L·min)、③vB=0.5 mol/(L·min),三种情况下该反应速率由大到小的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为_____________________ ;
(2)反应开始至2 min,气体Z的平均反应速率为_________ ;
(3)当反应达平衡时后:若X、Y、Z均为气体,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为_____ 反应(填放热或吸热)。

(1)该反应的化学方程式为
(2)反应开始至2 min,气体Z的平均反应速率为
(3)当反应达平衡时后:若X、Y、Z均为气体,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在一定条件下,向V L密闭容器中充入 和
和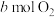 ,发生反应
,发生反应 。
。
(1)反应刚开始时,由于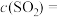
___________ ,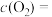
___________ ,而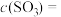
___________ ,所以化学反应速率___________ 最大,而___________ 最小(为零)(填“v(正)”或“v(逆)”)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为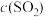
___________ (填“增大”“减小”或“不变”下同),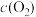
___________ ,而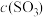
___________ ,从而化学反应速率v(正)___________ ,而v(逆)___________ 。
(3)当反应进行到时v(正)与v(逆)___________ 时,此时可逆反应达到最大限度,若保持外界条件不变时,混合物中各组分的物质的量、浓度、质量分数、体积分数及总压强都___________ 。
(4)以下是反应: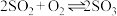 在不同条件下达到平衡状态时
在不同条件下达到平衡状态时 的转化率。
的转化率。
试回答下列问题:
①提高该化学反应限度的途径:___________ 。
②要实现 的转化率为93.5%,需控制的反应条件是
的转化率为93.5%,需控制的反应条件是___________ 。
 和
和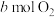 ,发生反应
,发生反应 。
。(1)反应刚开始时,由于
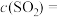
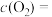
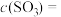
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为
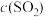
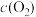
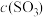
(3)当反应进行到时v(正)与v(逆)
(4)以下是反应:
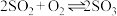 在不同条件下达到平衡状态时
在不同条件下达到平衡状态时 的转化率。
的转化率。压强 转化率 温度 | 0.1 MPa | 0.5 MPa | 1 MPa | 10 MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
①提高该化学反应限度的途径:
②要实现
 的转化率为93.5%,需控制的反应条件是
的转化率为93.5%,需控制的反应条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知Fe3+与 之间的反应是可逆反应:
之间的反应是可逆反应: 。某同学对该反应的可逆性进行实验。实验过程如下:
。某同学对该反应的可逆性进行实验。实验过程如下:
①将2mL0.004 KI溶液放入试管中,然后加入VmL0.004
KI溶液放入试管中,然后加入VmL0.004 FeCl3溶液并立即振荡。
FeCl3溶液并立即振荡。
②将充分反应后的①中溶液分成三份,分别放入A、B、C三个试管中,向A中加入3滴淀粉溶液,向B中加入3滴X溶液,向C中加入3滴蒸馏水。
回答下列问题:
(1)为达到预期实验目的,
_______ ,常用试剂X是_______ ,当A、B中溶液出现预期现象时,可确定该反应是可逆反应。
(2)假设实验①中V=2且忽略溶液体积的变化,反应经5s末时溶液颜色稳定不变且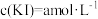 。则前5s内v(I2)=
。则前5s内v(I2)=_______ 。在图1的坐标系中画出用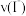 表示正、逆反应速率随时间的变化示意图
表示正、逆反应速率随时间的变化示意图_____ ;在图2的坐标系中画出c(Fe2+)随时间的变化图象______ 。


图1 图2
(3)若向C试管中加入少量固体KCl,振荡后静置,溶液颜色_______ (填“变深”“变浅”或“不变”)。
 之间的反应是可逆反应:
之间的反应是可逆反应: 。某同学对该反应的可逆性进行实验。实验过程如下:
。某同学对该反应的可逆性进行实验。实验过程如下:①将2mL0.004
 KI溶液放入试管中,然后加入VmL0.004
KI溶液放入试管中,然后加入VmL0.004 FeCl3溶液并立即振荡。
FeCl3溶液并立即振荡。②将充分反应后的①中溶液分成三份,分别放入A、B、C三个试管中,向A中加入3滴淀粉溶液,向B中加入3滴X溶液,向C中加入3滴蒸馏水。
回答下列问题:
(1)为达到预期实验目的,

(2)假设实验①中V=2且忽略溶液体积的变化,反应经5s末时溶液颜色稳定不变且
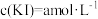 。则前5s内v(I2)=
。则前5s内v(I2)= 表示正、逆反应速率随时间的变化示意图
表示正、逆反应速率随时间的变化示意图

图1 图2
(3)若向C试管中加入少量固体KCl,振荡后静置,溶液颜色
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】500℃时,在2L的密闭容器中,SO2和足量的O2在催化剂的条件下发生反应:2SO2+O2 2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
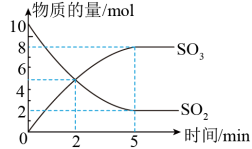
(1)在前5min内,以SO2的浓度变化表示的化学反应速率是____ mol/(L·min)。加快反应速率的措施有____ (至少提出两条)。
(2)该反应在____ (填2或5)min达到限度。
(3)反应达到平衡状态的依据是____ 。
A.单位时间内消耗1molSO2,同时生成1molSO3
B.SO2的浓度与SO3浓度相等
C.SO2的浓度与SO3浓度均不再变化
(4)用微观示意图的形式表示上述反应:____ 。

 2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
(1)在前5min内,以SO2的浓度变化表示的化学反应速率是
(2)该反应在
(3)反应达到平衡状态的依据是
A.单位时间内消耗1molSO2,同时生成1molSO3
B.SO2的浓度与SO3浓度相等
C.SO2的浓度与SO3浓度均不再变化
(4)用微观示意图的形式表示上述反应:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】自然界的矿物,岩石的成因和变化受到许多条件的影响。地壳内每增加1 km,压强增大约25000~30000kPa,在地壳内SiO2和HF存在以下平衡:SiO2(s) +4HF(g)⇌SiF4(g)+ 2H2O(g)。
(1)写出SiF4的结构式:________ 。
(2)以上反应在地壳的那个区域先达平衡________ (选填编号,下同)。
a.地壳表层 b.地壳深层
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,________ 。
a.2v正(HF)=v逆(H2O) b.v正(H2O)=2v逆(SiF4)
c.SiO2 的质量保持不变 d.反应物不再转化为生成物
(4)若反应的容器容积为2.0 L,反应时间 8.0 min,容器内气体的密度增大了0.12g/L,在这段时间内HF的平均反应速率为_______ 。
(1)写出SiF4的结构式:
(2)以上反应在地壳的那个区域先达平衡
a.地壳表层 b.地壳深层
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,
a.2v正(HF)=v逆(H2O) b.v正(H2O)=2v逆(SiF4)
c.SiO2 的质量保持不变 d.反应物不再转化为生成物
(4)若反应的容器容积为2.0 L,反应时间 8.0 min,容器内气体的密度增大了0.12g/L,在这段时间内HF的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在2L密闭容器内,t℃时发生反应: 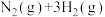 ⇌
⇌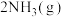 ,在体系中,
,在体系中, 随时间的变化如表:
随时间的变化如表:
(1)上述反应在第5min时, 的转化率为
的转化率为_______ ;
(2)用 表示从0~2min内该反应的平均速率
表示从0~2min内该反应的平均速率 =
=_______ ;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为_______ 。(用字母填空,下同);
a.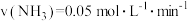 b.
b.
c. d.
d.
(4)下列表述能作为反应达到化学平衡状态的标志是_______ 。
a.反应速率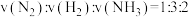
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内生成n mol 的同时,生成3n mol
的同时,生成3n mol 
f. 消耗=
消耗= 消耗
消耗
g.单位时间内3mol H-H键断裂的同时6mol N-H键也断裂
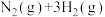 ⇌
⇌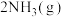 ,在体系中,
,在体系中, 随时间的变化如表:
随时间的变化如表:| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
 的物质的量(mol) 的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
 的转化率为
的转化率为(2)用
 表示从0~2min内该反应的平均速率
表示从0~2min内该反应的平均速率 =
=(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为
a.
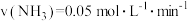 b.
b.
c.
 d.
d.
(4)下列表述能作为反应达到化学平衡状态的标志是
a.反应速率
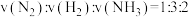
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内生成n mol
 的同时,生成3n mol
的同时,生成3n mol 
f.
 消耗=
消耗= 消耗
消耗g.单位时间内3mol H-H键断裂的同时6mol N-H键也断裂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应速率和限度与生产、生活密切相关。
(1)某同学为了探究锌与硫酸反应过程中的速率变化,在 400mL 稀硫酸中加入足量的锌粉,标况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大_______ min(填“0~1”、“1~2”、“2~3”、“3~4”、“4~5”), 原因是________ 。
②求 3~4 分钟时间段以盐酸的浓度变化来表示的该反应速率________ 设溶液体积不变)。
(2)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回 答下列问题:
①硫酸铜溶液可以加快氢气生成速率的原因是_______ 。
②实验室中现有 Na2SO4、MgSO4、Ag2SO4、K2SO4等 4 种溶液,可与实验中 CuSO4溶液起相似作用的是_______ 。
③要减慢上述实验中气体产生速率,可采取的合力措施有_______ 、_______ (答两种)。
(3) 某温度下在 4 L 密闭容器中,X、Y、Z 三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是_______ 。
②该反应达到平衡状态的标志是_______ (填字母)
A.Y 的体积分数在混合气体中保持不变 B.X、Y 的反应速率比为 3:1
C.容器内气体压强保持不变 D.容器内气体的总质量保持不变E.生成 1 mol Y 的同时消耗 2 mol Z
③2 min 内 Y 的转化率为_______ 。
(1)某同学为了探究锌与硫酸反应过程中的速率变化,在 400mL 稀硫酸中加入足量的锌粉,标况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 100 | 210 | 464 | 576 | 620 |
①哪一时间段反应速率最大
②求 3~4 分钟时间段以盐酸的浓度变化来表示的该反应速率
(2)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回 答下列问题:
①硫酸铜溶液可以加快氢气生成速率的原因是
②实验室中现有 Na2SO4、MgSO4、Ag2SO4、K2SO4等 4 种溶液,可与实验中 CuSO4溶液起相似作用的是
③要减慢上述实验中气体产生速率,可采取的合力措施有
(3) 某温度下在 4 L 密闭容器中,X、Y、Z 三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②该反应达到平衡状态的标志是
A.Y 的体积分数在混合气体中保持不变 B.X、Y 的反应速率比为 3:1
C.容器内气体压强保持不变 D.容器内气体的总质量保持不变E.生成 1 mol Y 的同时消耗 2 mol Z
③2 min 内 Y 的转化率为
您最近一年使用:0次



